| 内容要旨 | | 昆虫にとって重要な情報伝達物質としてフェロモンが知られている。集合フェロモン、警報フェロモン、道しるベフェロモンなどその伝達する情報によって分類されているが、その中の一つに性フェロモンがある。 昆虫の性フェロモン研究は、1959年にA.Butenandtらがbombykolをカイコガの性フェロモンとして単離したことに始まる。それ以降150種以上の昆虫の性フェロモンが構造決定されており、それぞれ極微量で、種特異的に作用しており、昆虫にとって重要な情報伝達物質であることは疑いない。このように昆虫にとって重要な物質を、ヒトが有効に利用できれば昆虫の生態制御、ひいては害虫の防除に適用できるものとなる。 フェロモンは極微量で生物活性を示すため、天然に産する性フェロモンもやはり極微量でしかない。そのため構造確認、活性本体の究明はもとより、その実用に関しても合成化学の果たす役割は大きい。ここでは生化学的手法を用いて、小麦の貯穀害虫であるHessia flyの性フェロモンとチャオビゴキブリの性フェロモンの光学活性体合成を行なった。 1)Hessian Flyの性フェロモン(S,E)-1-methyl-9-dodecenyl acetateの合成 1991年にFosterらにより、Hessian flyの雌が産卵管より分泌する性フェロンが単離され、(S,E)-1-methyl-9-dodecenyl acetate(5)と構造が決定された。その後Millarらにより(S)-propylene oxideを出発物質として合成されるに至りその構造が確定していた。 今回Hessian flyの性フェロモンである(S,E)-1-methyl-9-dodecenyl acetate(5)をアセト酢酸エチルのパン酵母還元により容易に光学活性体が得られる(S)-3-ヒドロキシブタン酸エチル(1)より合成することとした。 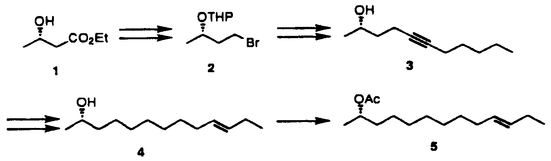 常法によりアセト酢酸エチルをパン酵母により不斉還元し、(S)-3-ヒドロキシブタン酸エチル(1)(96.4%e.e.)を調製した。この(S)-3-ヒドロキシブタン酸エチルを文献に従って、既知の臭化物(2)へと導いた。 この臭化物の炭素鎖を1-ヘプチンにより伸長し、次に酸処理することによりアルコール体(3)を得た。さらにアセチレンジッパー反応を行ない三重結合を炭素鎖の末端へと移動させた後、ジアニオンを調製し、ヨウ化エチルによりエチル化して炭素鎖をさらに2炭素伸長させた。そして水素化アルミニウムリチウムにより三重結合を二重結合へと還元し(S,E)-10-tridecen-2-ol(4)を得た。この段階で3,5-ジニトロ安息香酸エステルとして再結晶により精製し、最後にアセチル化することによりHessian flyの性フェロモンである(S,E)-1-methyl-9-dodecenyl acetate(5)を合成した。 文献既知の臭化物2より8工程通算収率13.4%で5を合成した。光学純度は4のアルコールを(S)-2-acetoxypropanoate誘導体へと導きガスクロマトグラフィーにより95.5%e.e.であると決定した。 2)チャオビゴキブリの性フェロモンである5-(2,4-dimethylheptyl)-3-methyl-2H-pyran-2-one(supellapyrone)の合成 チャオビゴキブリ(brownbanded cockroach,Supella longipalpa)の雌が分泌する性フェロモンである5-(2,4-dimethylheptyl)-3-methyl-2H-pyran-2-one(supellapyrone)は -パイロン環を有し、昆虫由来の天然物としては珍しい構造をしている。 -パイロン環を有し、昆虫由来の天然物としては珍しい構造をしている。 ラセミ、ジアステレオマー混合物の合成により平面構造およびその活性は確認されている。また合成されたラセミ、ジアステレオマー混合物は天然物とほぼ同様の活性を有することも確認されている。しかし活性本体の絶対立体配置は確定しておらず、その解明をすべく合成を行なった。 a)ラセミ体の合成 実際の合成としては側鎖部分の合成段階とパイロン環の合成段階に分けられる。天然に産するポリプロピオネート化合物では隣あうメチル基がsynである化合物が多くみられるため、supellapyrone(11)でも側鎖にみられる2つのメチル基はsynであると考え、最初にラセミ体の合成に着手した。 まず側鎖部分の合成は次のように行なった。メシトールを原料とし、高圧下Raney-Niを用いて水素添加し、続いてアルコール部分をJones酸化することにより、メチル基がすべてsynのトリメチルシクロヘキサノンへと変換した。さらにBaeyer-Villiger酸化することでラクトンへと導き、このラクトンを加メタノール分解することによりヒドロキシエステル(6)へと変換した。生じた水酸基をトシル化した後、水素化アルミニウムリチウムにより脱トシルオキシと同時にエステル部分を還元してアルコール体を得た。このアルコール体を対応するヨウ化物(7)へと変換した。   -パイロン環部分は次のように構築した。すなわちマロン酸ジエチルをNaOMe存在下ヨウ化物(7)でアルキル化し、次にエノレートとした後、還流下水素化アルミニウムリチウムで還元することによりアリルアルコールを得た。このアリルアルコールを活性二酸化マンガンで酸化することにより -パイロン環部分は次のように構築した。すなわちマロン酸ジエチルをNaOMe存在下ヨウ化物(7)でアルキル化し、次にエノレートとした後、還流下水素化アルミニウムリチウムで還元することによりアリルアルコールを得た。このアリルアルコールを活性二酸化マンガンで酸化することにより , ,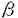 -不飽和アルデヒド(8)とした。 -不飽和アルデヒド(8)とした。 この , ,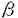 -不飽和アルデヒドにフェニルチオマロン酸ジエチルをMichael付加したのち、炭酸ナトリウム水溶液を用いて鹸化し、さらに脱炭酸することによりアルデヒドカルボン酸(9)を得た。このアルデヒドカルボン酸(9)をp-トルエンスルホン酸存在下ベンゼン中で加熱還流することで環化生成物(10)を得た。 -不飽和アルデヒドにフェニルチオマロン酸ジエチルをMichael付加したのち、炭酸ナトリウム水溶液を用いて鹸化し、さらに脱炭酸することによりアルデヒドカルボン酸(9)を得た。このアルデヒドカルボン酸(9)をp-トルエンスルホン酸存在下ベンゼン中で加熱還流することで環化生成物(10)を得た。 次に3位にメチル基を導入するために、10をリチウムヘキサメチルジシラジドによりリチオエノラートとし、ヨウ化メチルによりメチル化して、最後にフェニルチオ基をm-クロロ過安息香酸により酸化し、脱フェニルスルホニルすることにより目的化合物であるsupellapyrone(11)を油状物質として得た。 合成物のNMR及びIRスペクトルは天然物とよく一致し、天然体のsupellapyroneは側鎖部分にsyn-ジメチル基を有していることが確認され、当初の予測が妥当であったことが判明した。 b)光学活性体の合成 光学活性体の合成では、合成中間体の酵素による光学分割を行うことにより、光学活性原料を調製することとした。 2級の水酸基を有する6の酵素分割を行うべく、種々の酵素のスクリーニングを行なった。その結果リパーゼAKが収率および光学純度について良好な結果を与えた。そこで反応スケールを試料調製に用いる程度にしたところ、反応速度は低下したが、分割の結果得られるアセテートおよびアルコールの光学純度の顕著な低下は見られず、試料調製に関しては支障はなかった。  こうして調製した光学活性体(2R,4S,6S)-6および(2S,4R,6R)-12を加メタノール分解した後の(2S,4R,6R)-6を用いてラセミ体と同様の手法で光学活性体の合成を行なった。 c)パイロン環と側鎖との直接カップリングの試み パイロン環を合成の最終段階に構築する方法は、収率の点不満が残された。そこで側鎖部分とパイロン環部分のパラジウム触媒を用いたクロスカップリングを検討した。 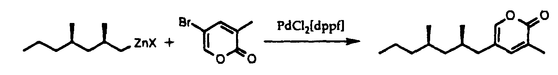 反応性の高い有機リチウム試薬およびGrignard試薬をこのクロスカップリングに用いるとパイロン環が崩壊し目的物は得られなかったが、反応性のやや低い有機亜鉛化合物を用いることにより反応を行なった。 3)結論 Hessian flyの性フェロモン(S,E)-1-methyl-9-dodecenyl acetateとチャオビゴキブリの性フェロモンである5-(2,4-dimethylheptyl)-3-methyl-2H-pyran-2-one(supellapyrone)を合成した。 4)文献1)Biosci.Biotech.Biochem.,(1993),57,1967-1968(森 謙治と共著)2)Nat.Prod.Lett.,in press(森 謙治と共著)3)Proc.Japan Acad.,70B,143-145(森 謙治と共著) |
| 審査要旨 | | 本論文は昆虫にとって重要な情報伝達物質であるフェロモンの光学活性体の合成を生化学的手法を用いて行なった報告である。フェロモンは極微量で生物活性を示すため、天然に産する性フェロモンもやはり微量であり、そのため構造確認、活性本体の究明はもとより、その実用に関しても合成化学の果たす役割は大きい。著者は以下に示すように小麦の貯穀害虫であるHessian Flyの性フェロモン(1)と、同じく貯蔵穀物に対する害虫であるチャオビゴキブリの性フェロモン(2)の光学活性体合成を行なった。 序論で研究の背景を概観した後、第1章ではHessian Flyの性フェロモンである(S,E)-1-メチル-9-ドデセニルアセタート(1)をアセト酢酸エチルの酵母還元により容易に光学活性体が得られる(S)-3-ヒドロキシブタン酸エチル(3)より合成した。途中5の再結晶により精製を行なっている。文献既知の臭化物(4)より8工程通算収率13.4%で1を合成した。 第2章ではチャオビゴキブリ(brownbanded cockroach,Supella longipalpa)の性フェロモンである5-(2,4ジメチルヘプチル)-3-メチル-2H-ピラン-2-オン(スペラパイロン)のラセミ体合成について述べている。このスペラパイロンは、ラセミ・ジアステレオ混合物の合成により平面構造およびその活性は確認されていたが、絶対立体配置は確定しておらず、その解明をすべく合成を行なった。スペラパイロンの側鎖部分の置換メチル基がsynであると仮説を述べた後、メシトール(6)を出発原料とし高圧下水素添加することでその側鎖部分の合成を行なっている。 -パイロン環部分の合成は順次炭素骨格を構築し、最後に芳香化することでその合成を行なっている。合成されたラセミ体のスペクトルデータは先の側鎖置換基がsynであるとの仮説に妥当性を付与した。 -パイロン環部分の合成は順次炭素骨格を構築し、最後に芳香化することでその合成を行なっている。合成されたラセミ体のスペクトルデータは先の側鎖置換基がsynであるとの仮説に妥当性を付与した。 第3章ではスペラパイロンの光学活性体合成を行なった。ラセミ体合成の中間体を酵素による光学分割に供し、光学活性原料を調製している。種々の酵素のスクリーニングは2級水酸基を有するヒドロキシエステル(7)を基質として不斉アシル化を検討した。その結果リパーゼAKが生成物の収率および光学純度について良好な結果を与えた。光学分割により生じた化合物の絶対立体配置の決定は既知化合物へと変換して確認している。調製した光学活性体(-)-7、および(+)-8を加メタノール分解した後の(+)-7を用いてラセミ体とほぼ同様の手法で光学活性体の合成を行なった。生物活性試験の結果(2R,4R)-スペラパイロンがその活性本体であることが判明した。 以上本論文はHessian Flyの性フェロモンである(S,E)-1-メチル-9-ドデセニルアセタートとチャオビゴキブリの性フェロモンである5-(2,4-ジメチルヘプチル)-3-メチル-2H-ピラン-2-オン(スペラパイロン)の両鏡像体の合成を、生化学的手法を用いて行なったものである。光学活性体合成において生化学的手法を用いることの有用性を示したもので、学術上、応用上、貢献するところが少なくない。よって審査員一同は、申請者に博士(農学)の学位を授与してしかるべきものと判定した。 |