生物がその成長の課程で様々な組織や器官に分化していく現象は、農業や医療における応用上極めて興味深く、多くの研究者が様々な方面からその解明に取り組んでいる。しかしこの問題にはまだまだ未知の部分が多く、そのメカニズムを知るには至っていない。そのような状況の中、分化を直接引き起こす化学物質が次第に発見されてくるようになった。それらについて構造活性相関などの地道な研究を重ねることで、メカニズムの解明という大きな目標に少しずつでも近づいていくことができるのではないだろうか。有機合成化学の分野からこの問題の解決に加担することを考え、それら重要な鍵となると思われる物質の化学合成による供給の研究を開始した。いかに純粋な形で、そして効率良く調製することができるか。そのことを念頭に、以下に挙げる物質について合成研究を行なった。
第一章バシディファーキノン 菌類の分化や形態形成に温度や光といった要因が効いていることは古くから知られているが、最近の研究ではそこから一歩進んで、ある特定の化学物質がそれらの活動の発現に深く関わっていることが分かってきている。
菌類の分化の典型的な例として子実体の形成があり、この現象を指標としたスクリーニングにより、いくつかの種について活性を呈する物質が発見されている。バシディファーキノン1も同様の経緯で発見された物質であり、アミスギタケ(Favolus arcularius)の子実体形成を誘導する物質として、放線菌の一種であるStreptomyces B-412から単離された。
1は5環性の物質であり、高度に置換されたベンゼン環を含むアントラキノン骨格を中心としている。構造活性相関の研究をにらみ、基本となる部分2とカップリング・パートナー3とに分け、3をさしかえることにより様々な可能性に対応できるようにしたい。このような事情を考慮して、とりあえず基本部分である2の合成を目指し、以下のように合成研究を進めた。

光学活性な2の調製が目的なので、原料には光学活性体の入手可能なマンデル酸メチル4を用いた。4の水酸基を保護し、エステルを還元して得られたアルデヒドにWittig反応を行なって、5とした。5を塩基処理、シリル化でジエンとし、アセチレンジカルボン酸メチルとのDiels-Alder反応で、環化物6とした。6のシリルエノールエーテル部分に1炭素増炭反応を施すなどして、7を得た。芳香環を形成するため様々な手法を試みたが、結局3段階でスルホキシド8にまでもってきた。現在8から先の合成を進行中だが、スルホキシドの熱脱離で芳香化した後、環の巻き直しで9(2の一候補)を得る予定である。

第二章ジャスモン酸類 ジャスモン酸類は元来ジャスミン、ラン等の香気成分として単離、構造決定されたものである。最初の発見から既に60年以上経ているが、植物界での普遍的な分布が知られるにも関わらず、その存在意義については長い間不明であった。1970年代に入って成長抑制や老化促進などの活性を示すことが報告され、最近ではバレイショやキクイモの塊茎の形成を誘導するといった特異な活性を有することが分かってきた。

ジャスモン酸類の合成は現在までに数多く報告されており、特にジャスモン酸メチル10bについては工業化されている合成法もあるが、活性物質としての役割が注目されてきている今日、構造活性相関や代謝経路等の研究材料に耐えうる光学的に純粋な標品の調製が求められている。このような要求に答えるべく、 -ヒドロキシエビジャスモン酸(ツベロン酸)を中心に、周辺の関連ジャスモン酸類の合成研究に着手した。
-ヒドロキシエビジャスモン酸(ツベロン酸)を中心に、周辺の関連ジャスモン酸類の合成研究に着手した。
(1)共通中間体の合成 合成を始めるにあたり、多くのジャスモン酸類の合成に共通に用いることのできる中間体18の調製を行なった。
合成原料として、光学活性なジクロルラクトン15(99.6% e.e.)を用いた。9を脱クロル化、還元、アセタール化の3段階で16とした。二重結合部分をエポキシ化、その位置選択的な還元的開環、生じたアルコールの酸化で、ケトン17とした。このものにHorner-Emmons型の増炭反応、オレフィンの立体選択的水素添加で、中間体18を得た。15から8段階、51%であった。
同様に15の鏡像体から41%の収率で18の鏡像体を得た。

(2)エピジャスモン酸メチル エピジャスモン酸メチル11bは最も強いジャスミン芳香を持つことで知られているが、最近の研究からキクイモの塊茎形成を誘導することも分かっている。
18を酸加水分解してヘミアセタールとした後、Wittig反応で側鎖を導入し、硝酸銀含浸シリカゲルクロマトグラフィーで精製して、(Z)-オレフィン側鎖を持ったラクトン19を得た。ラクトンをアルカリ加水分解し、即座にジアゾメタンでエステル化して、ヒドロキシエステル20とした。最後にクロム酸を用いて注意深く酸化し、目的化合物である天然型エピジャスモン酸メチル11bを得た。18から5段階、50%の収率であった。
同様に18の鏡像体から48%の収率で、非天然型エピジャスモン酸メチルent-11bを得た。
合成した11bの両胸像体を生物活性試験に供したところ様々な知見が得られたが、詳細は論文中に記載する。

(3)ツベロン酸メチル( -ヒドロキシエピジャスモン酸メチル)
-ヒドロキシエピジャスモン酸メチル) バレイショの塊茎形成誘導物質として新規に発見されたツベロン酸12a、そしてそのメチルエステル12bやグルコシド12cなどの一連の化合物群は、塊茎を形成する植物に普遍的に存在するものと考えられている。
18を酸加水分解した後Wittig反応を行なったが、オレフィンの幾何選択性が好ましくなかったため、別のルートを考えた。18のアセタールを外すと同時にチオアセタール保護、ヒドロキシエステルのラクトン化で21とした。チオアセタールを落とし、生じたアルデヒドに即座にWittig反応を行なって、選択的に(Z)-オレフィンを導入した。側鎖の水酸基の保護をより温和に落とせるものにかけ替えて22とした後、ラクトンのアルカリ加水分解、ジアゾメタン処理で23とした。最後にPDCで酸化、水酸基の脱保護で、目的化合物である天然型ツベロン酸メチル12bを得た。中間体18から10段階、15%の収率であった。
同様の方法で、現在18の鏡像体から非天然型ツベロン酸メチルent-6bを調製中である。

(4)ジャスミンケトラクトンおよびエピジャスミンケトラクトン ジャスミンケトラクトン14の発見は古く、既に50年前に香気成分としてその存在が指摘されている。14とそのエピマーであるcis-ジャスミンケトラクトン13は、ツベロン酸12aと類似の官能基を揃えているため、その比較検討は構造活性相関の研究への一助となるであろう。
18から出発し、Wittig反応で選択的に側鎖を導入するなどして、24とした。水酸基を保護した後、一級アルコールの保護基のみを選択的に除去し、さらにエステルをアルカリ加水分解してヒドロキシカルボン酸25とした。25をマクロラクトン化して26とし、最後に二級アルコールの脱保護と酸化で天然型エピジャスミンケトラクトン13を得た。中間体18から14段階、3.2%の収率であった。さらに13を塩基処理で異性化し、熱力学的により安定なジャスミンケトラクトン14を得た。13から90%の変換率であった
同様の方法で、現在18の鏡像体から非天然型エピジャスミンケトラクトンent-13と非天然型ジャスミンケトラクトンent-14を調製中である。

(5)ツベロン酸メチルグルコシド 前述のようにツベロン酸メチルグルコシド12dはバレイショの塊茎形成誘導物質としてツベロン酸グルコシド12cと共に新規に発見された物質であるが、この系統の活性物質としては最初に発見されたものである。12c自体はその自らのカルボン酸としての酸性により非常に不安定であり調製は困難だが、12dは比較的安定なため研究材料として適していると思われる。一連のジャスモン酸類の合成で得た知見をもとに、現在12dの合成を行なっている。
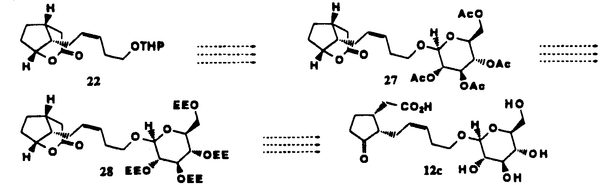
18から出発し、Wittig反応で選択的に側鎖を導入するなどして、22とした。水酸基の保護を外し、アセチル保護されたグルコースとグリコシドを形成させて27とする。アルカリ加水分解でラクトンの開環と脱アセチル化を行ない、酸処理でラクトンの再形成、糖部分の水酸基により温和に落とせる保護基をかけて28とする。ラクトンのアルカリ加水分解、メチルエステル化、アルコールの酸化と糖部分の脱保護で、目的化合物である12dを得る予定である。
以上述べてきた通り、光学活性なジャスモン酸類の合成に有用な共通中間体15から、エピジャスモン酸メチル11bの両胸像体、ツベロン酸メチル12b、ジャスミンケトラクトン14、エピジャスミンケトラクトン13の天然体を合成した。また現在ツベロン酸メチルグルコシド14dを調製中であり、それぞれの両胸像体の調製が完了し次第、生物活性試験に供する予定である。