海洋生物から医薬などの生化学資源を探索・開発しようという研究は、1970年代から活発になった。特に、資源の乏しいわが国では、豊富な海の未利用資源の有効利用は重要な課題である。これまでは、抗菌・抗カビ性、抗腫瘍活性、抗炎症活性などの割合手軽に試験できる活性物質の探索が主流であったが、最近、より特異性の高いアッセイ法を用いて、医薬素材を探そうとする試みが、海洋生物を対象として行われるようになった。 このような状況の下に、本研究では、炎症やがんなどの疾病に関与するインターロイキン6(IL-6)レセプターおよび脳障害にかかわるN型カルシウムチャネルに作用する物質を海綿から探索して海綿、ひいては、海洋生物の医薬資源としての可能牲を探った。その結果、IL-6レセプター阻害物質として新規の長鎖アミド配糖体を、さらに、Ca2+チャネル作用物質として脂肪酸とポリアミンのアミドをそれぞれ単離・構造決定することができた。その概要は以下の通りである。 (1)インターロイキン6(IL-6)のレセプターへの結合阻害物質の探索 日本各地で採集した海綿について、IL-6レセプターに対するアンタゴニスト活性を調べたところ、八丈島産海綿Erylus placentaに顕著な活性が認められたので、活性物質の単離と構造の解明を試みた。凍結海綿(1.3kg)をエタノール抽出し、抽出液を濃縮後、1NNH4OHでpHを9に調整した。これを順次エーテルおよびn-ブタノールで抽出した。活性が認められたプタノール可溶画分を、ゲル濾過、シリカゲルカラムなどで分画後、逆相HPLCで精製して3つの活性成分、erylusamine A(1、収量14.5mg)、B(2、11.2mg)およびC(3、8.4mg)を得た。Erylusamine BおよびCは、それぞれ66および33 g/mLでIL-6のレセプターへの結合を50%阻害した。 g/mLでIL-6のレセプターへの結合を50%阻害した。 まず、erylusamine B(2)について、NMRを中心とする機器分析によって構造決定を試みた。分子式は、HRFABMSおよび13C NMRから、C62H108N2O24と決定した。また、1H NMRおよびHOHAHAスペクトルから、長鎖脂肪酸および4つの糖ユニットの存在が示唆されたため、アグリコン部と糖部にわけてさらに詳しく構造解析を行った。 アグリコン部には、2本体のCOSYおよびHMBCより、N,N-ジメチル-1,5-ペンタンジアミンユニットが含まれることが判明した。一方、erylusamine Bを温和な条件下で加水分解したところ、C34H68N2O4の分子式を持つジオール体を得た。1Hおよび13C NMRから、このジオール体には2つのオキシメチン、長いメチレン鎖、アミド、ケトンおよびN,N-ジメチル-1.5-ペンタンジアミンユニットが存在することが明らかとなった。さらに、FABMSのフラグメントイオンを解析することにより、ケトンと2つの水酸基は、14、22および23位にそれぞれ結合していることがわかった。2つの水酸基が隣接することは、アセトニド体に変換されることからも確かめられた。 次いで、COSYおよびHOHAHAスペクトルのクロスピークを各アノメリックプロトンを始点として解析した結果、4つのペントースユニットの存在が明らかとなった。そこで、デカップリング差スペクトルなどを用いて、1H-1H結合定数を詳細に解析して糖の同定を試みたところ、2つのキシロース(A環とB環)および2つのアラビノース(C環とD環)の存在が判明した。また、アノメリックプロトンは7.4-7.7Hzの結合定数をもつことから、全て 結合していると判断した。なお、C環の2、3および4位とD環の4位のメチンプロトンはいずれも低磁場シフトしていることから、これらの水酸基はアセチル化されていることが明らかとなった。 結合していると判断した。なお、C環の2、3および4位とD環の4位のメチンプロトンはいずれも低磁場シフトしていることから、これらの水酸基はアセチル化されていることが明らかとなった。 アグリコン部と糖部の結合は、HMBCの相関ピークにより、アグリコン部の23位の水酸基に糖のA環がグリコシド結合していることが示唆された。したがって、erylusamine Bの構造は、長鎖脂肪族ジヒドロキシケト酸とN,N-ジメチル-1,5-ペンタンジアミンのアミドに一部アセチル化されたL-アラビノースとD-キシロース各2個からなる糖鎖が結合した新規な構造である2と決定した。同様に、erylusamine AおよびCについても構造決定を行い、その構造を1および3と決定した。  最後に、erylusamine B(2)の立体化学について検討した。まず、糖については、加水分解物をパートリフルオロアセチルメチルグリコシド誘導体に導き、キラルGC分析を行って、アラビノースはL型、キシロースはD型と決定した。同様に、erylusamine AおよびCの糖部分も同じ絶対立体配置をもつと決定した。次に、アグリコン部分のジオールをアセトニドに導き、NOE実験を行って、ジオールの相対立体配置をsynと決定した。さらに、Eu(fod)3の存在下、CDスペクトルを測定したところ、負のコットン効果が観測されたので、ジオールの絶対立体配置は、22S、23Sと決定できた。 Erylusamine類は、全く新しい範疇にはいる化合物であり、IL-6のレセプターへの結合を阻害する最初の天然物質である。 (2) -コノトキシンのN型Ca2+チャネルへの結合阻害物質の探索 -コノトキシンのN型Ca2+チャネルへの結合阻害物質の探索 N型Ca2+チャネル阻害剤として知られる -コノトキシンは、巻貝のアンボイナガイConus geographusから得られたポリペプチドである。この毒の125I標識体を用いたスクリーニングにおいて、八丈島産海綿Erylus placentaに強い結合阻害作用が認められたので、活性物質の解明を試みた。凍結海綿(1kg)のエタノール抽出物を水とエーテル、ついでn-ブタノールと分配した。阻害活性が認められたn-ブタノール層のメタノール可溶画分を、Sephadex LH-20を用いるゲル濾過で分画する一方、メタノール不溶画分を遠心液液向流分配で分画した。それぞれから得られた活性画分を主にHPLCを用いて精製後、最終的に陰イオン交換樹脂を用いて塩酸塩として活性物質4を得た。 -コノトキシンは、巻貝のアンボイナガイConus geographusから得られたポリペプチドである。この毒の125I標識体を用いたスクリーニングにおいて、八丈島産海綿Erylus placentaに強い結合阻害作用が認められたので、活性物質の解明を試みた。凍結海綿(1kg)のエタノール抽出物を水とエーテル、ついでn-ブタノールと分配した。阻害活性が認められたn-ブタノール層のメタノール可溶画分を、Sephadex LH-20を用いるゲル濾過で分画する一方、メタノール不溶画分を遠心液液向流分配で分画した。それぞれから得られた活性画分を主にHPLCを用いて精製後、最終的に陰イオン交換樹脂を用いて塩酸塩として活性物質4を得た。 4は異なる脂肪酸からなる混合物であり、これ以上の分離ができなかったため、混合物のまま構造決定を行った。CF3CO2D存在下、低温で測定した1Hおよび13C NMRデータより、窒素と結合した多数のメチレンシグナルが観測されたので、本物質はポリアミン系化合物と推定された。さらに、N-ジメチル基のシグナルおよびそれに結合したメチレン基のシグナルが低磁場シフトしていることより、2つのアンモニウムイオンの存在が示唆された。一方、この化合物はFABMSでm/z773に(M+H)+イオンピーク、m/z723に(M+H-CH3Cl)+に相当するフラグメントイオンピークを与えた。これらのことから、この物質は2価に荷電していると考えられた。さらに、HRFABMSおよび各種NMRを検討して分子式をC44H94Cl2N6O2と決定した。さらに、FAB MS/MSの解析により、アンモニウムイオンの両隣で開裂したと思われる娘イオンピークが観測され、対称性のよい化合物であると推定された。また、13C NMRでアミドのカルボニルのシグナルが観測されたこと、1H NMRにおいて、アミドのプロトンのシグナルが観測されなかったこと、および窒素に結合したメチルシグナルが観測されたことより、ポリアミン部に脂肪酸が結合し、そのアミド基の窒素はメチル化されていると考えられた。このことは、酸加水分解で得られたポリアミンのFABMSおよびNMRデータからも確認された。 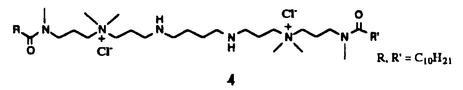 次に、脂肪酸の組成を調べるため、4を酸加水分解し得られた脂溶性画分をジアゾメタンでメチル化後、GC-MSで分析した。マススペクトルのフラグメンテーションパターンから次に示す5種類の脂肪酸が存在するものと考えられた。 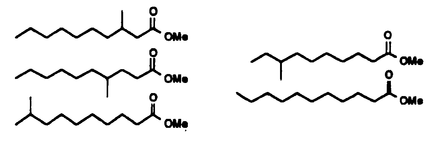 以上の結果、活性物質は、2つの陽電荷を持つポリアミンの両末端にC11脂肪酸が結合した構造4と推定した。この構造の確認を行うため、putrescinを出発物質とし、下記の方法で全合成を行った。まず、ポリアミン部をputrescinからシアノエチル基による伸張を繰り返すことにより構築し、酸クロライドを用いてポリアミン部の両末端にアシル基を導入した。さらに、2通りのメチル化後、最終的にアミンの脱保護により全合成を達成した。アシル基としては枝分かれのないn-ウンデカノイル基を用いた。  合成品の、1Hおよび13C NMRスペクトルは脂肪酸部を除いて天然物とよく一致を示した。また、両者のFABMSにおける主なフラグメントイオンビークは同一であった。天然品および合成品は、それぞれIC50 1.1 g/mLおよび4.7 g/mLおよび4.7 g/mLで g/mLで -コノトキシンのレセプターへの結合を阻害した。この活性物質は、ポリアミンで、現在知られているただ1つの阻害剤 -コノトキシンのレセプターへの結合を阻害した。この活性物質は、ポリアミンで、現在知られているただ1つの阻害剤 -コノトキシンとは異なるタイプのものであった。 -コノトキシンとは異なるタイプのものであった。 以上、八丈島産海綿Erylus placentaから2種のレセプター作用物質を単離し、その構造を明らかにできた。得られた化合物はいずれも新しいタイプの化合物であり、海洋生物が新しい医薬素材の探索源として有望であることを示している。 |