生体内には多種のヘムタンパク質が存在しており、これらは、(1)cytochrome P450(以下P450)、各種peroxidase等の酸化酵素、(2)cytochrome c(cyt.c)、cytochrome b5等の電子伝達系構成成分、(3)hemoglobin、myoglobinといった酸素運搬・貯蔵体の3種類に大別される。また酸化酵素の中にあってもP450は、芳香環及び飽和炭化水素の水酸化反応も触媒する特異なヘムタンパク質であり、この高い酸化活性は多方面から注目されている。筆者は、全てのヘムタンパク質は活性中心にヘムを有しており、その機能はアポタンパク質により制御されていることに着目し、P450以外の入手容易なヘムタンパク質に修飾を加えることによってP450様の反応性を発現させ、有用なP450 Mimicsを創製するとともに、P450の高い酸化活性発現の要因を検討することを目的とした。修飾の方法としては固定化をとりあげ、ガラスビーズにコーティングしたpoly( -methyl-L-glutamate)を担体として、cyt.c、horseradish peroxidase(HRP)等を共有結合法により固定化した。修士論文では、buffer中での基質酸化反応において、固定化によりcyt.c及びHRPのN-脱メチル化、sulfideの酸化等の活性が増大することを明らかにした。今回は、有機溶媒中での固定化ヘムタンパク質による芳香環及び飽和炭化水素の水酸化反応について発表する。これらはP450以外のヘムタンパク質ではほとんど進行しない点で興味深い反応であり、また多くの小分子P450化学モデル系を用いた場合でも効率は低い。有機溶媒中での酵素反応については、近年水と混和しない有機溶媒にごく少量の水を懸濁させた不均一な反応系(微水系)の研究が盛んになりつつあり、これまでに加水分解酵素によるペプチド・エステル合成等が行われている。P450の基質である炭化水素類の反応の場合、有機溶媒中で基質濃度を高くできることは大きな利点となり得る。そこで微水系を反応系として固定化ヘムタンパク質による炭化水素類の水酸化反応を行い、その活性を検討した。 -methyl-L-glutamate)を担体として、cyt.c、horseradish peroxidase(HRP)等を共有結合法により固定化した。修士論文では、buffer中での基質酸化反応において、固定化によりcyt.c及びHRPのN-脱メチル化、sulfideの酸化等の活性が増大することを明らかにした。今回は、有機溶媒中での固定化ヘムタンパク質による芳香環及び飽和炭化水素の水酸化反応について発表する。これらはP450以外のヘムタンパク質ではほとんど進行しない点で興味深い反応であり、また多くの小分子P450化学モデル系を用いた場合でも効率は低い。有機溶媒中での酵素反応については、近年水と混和しない有機溶媒にごく少量の水を懸濁させた不均一な反応系(微水系)の研究が盛んになりつつあり、これまでに加水分解酵素によるペプチド・エステル合成等が行われている。P450の基質である炭化水素類の反応の場合、有機溶媒中で基質濃度を高くできることは大きな利点となり得る。そこで微水系を反応系として固定化ヘムタンパク質による炭化水素類の水酸化反応を行い、その活性を検討した。 1.芳香環水酸化反応 Free及び固定化したcyt.c:20 nmol、またはHRP:3 nmol、[oxidant]=20 mM、0.1M K-Pi(pH7.0):0.2〜1%(v/v)をbenzene 1ml中で懸濁させ、37℃で20分間撹拌し、benzeneの水酸化反応を行った。それぞれの場合のphenol生成量をTable 1に示す。Cyt.cでは、酸化剤の種類によらず、free cyt.cは活性を示さなかったが、固定化cyt.cは水酸化活性を示した。HRPでは、freeHRPは、H2O2を酸化剤として用いた場合のみbenzeneの水酸化活性を示し、m-chloroper-oxybenzoic acid(mCPBA)を用いた場合は活性を示さなかった。固定化HRPは、H2O2、mCPBAのどちらを用いた場合も活性を示した。特にmCPBAを用いた場合の固定化HRPのturnover数は30であり、通常のbuffer系でのP450のturnover数6.2の4.8倍となった。本来HRPのヘムはひろくアポタンパク質に覆われていると考えられている。従ってfree HRPでは、mCPBA分子が比較的かさ高いためにアポタンパク質に阻まれてヘム鉄に接近することができなかったのに対し、固定化HRPでは、固定化によりHRPのconformationが変化してヘムの第6配位子側の空間が広くなり、mCPBAのヘム鉄への接近が可能になったものと思われる。なおどの場合でもphenol以外の生成物はほとんど見られなかった。また、buffer中([benzene]=2mM、[oxidant]=1mM)で反応を行ったところ、固定化cyt.c、固定化HRPの場合とも反応は進行しなかった。反応系中のbuffer contentと固定化HRPの活性との関係をFig.1に示す(固定化cyt.cでも同様の結果が得られた)。少量のbufferを加えた場合、固定化HRPの活性は、bufferを全く加えない場合の約2倍に増大した。微水系では一般的に、添加した少量の水が酵素分子に水和してタンパク質のconformationをflexibleにすることが酵素活性の発現に重要な役割を果たしていると考えられている。Fig.1の結果から、固定化HRPの場合も同様に少量のbufferの存在が重要であることが示された。また、さらにbuffer添加量を増していくと活性の低下が見られた。これは固定化HRP周辺の水量が多くなりすぎて基質であるbenzeneがヘム鉄に接近しにくくなるためと思われる。  Table 1 Hydroxylation of Benzene by Cyt.c and HRP Table 1 Hydroxylation of Benzene by Cyt.c and HRP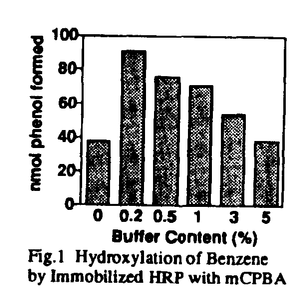 Fig.1 Hydroxylation of Benzene by Immobilized HRP with mCPBA Fig.1 Hydroxylation of Benzene by Immobilized HRP with mCPBA 2.飽和炭化水素酸化反応 次に、CH2Cl2を反応溶媒とし、飽和炭化水素であるadamantaneの酸化反応について同様に検討した(cyt.c:20 nmol、HRP:3 nmol、[adamantane]=200 mM、[H2O2]=20 mM)。結果をTable 2に示す。この結果から、固定化cyt.c、固定化HRPとも、P450と同様にadaman-taneのような飽和炭化水素の水酸化反応を進行させることが示された。この反応における固定化HRPの活性はbuffer系でのP450の活性に匹敵していた。Cyclohexane自身を溶媒として同様に酸化反応を行ったところ、固定化cyt.c、固定化HRPとも酸化活性を示した。またbuffer中([cyclohexane]=5 mM、[H2O2]=1 mM)ではこの反応は進行しなかった。 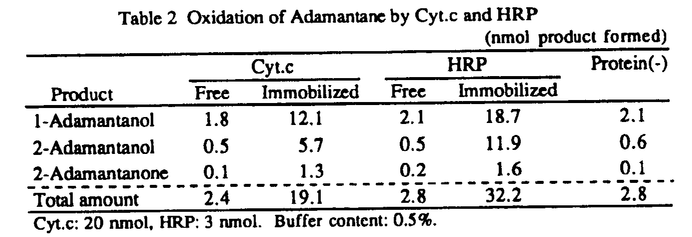 Table 2 Oxidation of Adamantane by Cyt.c and HRP Table 2 Oxidation of Adamantane by Cyt.c and HRP 3.反応機構の検討 P450は酸化活性種の酸素原子を基質に導入する特性を有している。そこで、固定化cyt.c、固定化HRPの場合の水酸化生成物の酸素原子の由来について検討した。Benzeneの水酸化の場合は、固定化cyt.c、固定化HRPとも約60〜70%が酸化剤由来、すなわち酸化活性種由来、残りは溶存酸素由来であり、水分子由来のものは無かった。Adamantaneの水酸化の場合は、ほとんど全てが酸化剤由来であった。これらの結果から、固定化cyt.c、固定化HRPは、微水系における芳香環及び飽和炭化水素の水酸化反応において、P450と同様酸化活性種の酸素原子を基質に導入する活性を有していることが示された。また固定化cyt.cを用いてtoluene-4-dの水酸化反応を行ったところ、生成物であるp-cresolには19%の重水素が保持されていた(Fig.2)。この結果から、固定化cyt.cによる芳香環水酸化反応において、P450と同様、NIH shiftが起きていることも示された。  Fig.2 Hydroxylation of Toluene-4-d by Immobilized Cyt.c Fig.2 Hydroxylation of Toluene-4-d by Immobilized Cyt.c 4.固定化によるタンパク質のconformation変化 固定化によりタンパク質のconformationにどのような変化が生じたかを検討するため、固定化cyt.cのESRスペクトル及びUV/Vis反射光スペクトルを測定した。Free cyt.cのヘム鉄は、第5配位子であるHisのimidazoleだけでなく、MetのS原子を第6配位子として有しており、ESRスペクトルではlow spinヘム鉄のシグナルが観測される。しかし固定化cyt.cのESRスペクトルではlow spinヘム鉄のシグナルは観測されず、代わってhigh spinヘム鉄のシグナルが観測された。またfree cyt.cは695 nmにFe-S配位由来の吸収を持つが、固定化cyt.cではこの吸収は見られず、625 nmにhigh spin cyt.cの吸収が見られた。これらの結果から、固定化によりcyt.cのconformationが変化し、比較的はずれやすい第6配位子であるMetのS原子がはずれヘム鉄がlow spinからhigh spinに変化したこと、従ってヘムの第6配位子側に基質や酸化剤が取り込まれる空間が生じたことが考えられる。 結論 以上述べたように、筆者はcyt.c、HRPといったP450以外のヘムタンパク質に不溶性担体への共有結合による固定化という修飾を施し、その基質酸化活性について検討した。その結果、微水系という特殊な有機溶媒反応系において、固定化cyt.c、固定化HRPが、従来のP450 Mimicsでは効率の低かった芳香環及び飽和炭化水素の水酸化反応を進行させることを見い出した。また、酸化活性種由来の酸素原子の基質への導入やNIH shift等、反応機構の点でもP450に類似していることが示された。ESRスペクトル、反射光スペクトル等から示唆された固定化によるタンパク質のconformation変化、つまりヘムの第6配位子側の空間が大きく広がり、酸化剤や基質を取り込みやすくなったという点、また微水系の利用によりbuffer中の場合よりも基質濃度を格段に高くすることが可能となった点等が、固定化ヘムタンパク質における炭化水素類水酸化活性の発現に結びついたものと考えられる。これらの結果は、P450以外のヘムタンパク質でも、タンパク質の修飾や適当な反応条件の設定により、機能を変換してP450と同様の反応性を発現させることが可能であるということを示しており、ヘムの機能を制御するアポタンパク質の役割を考える上で興味深い知見である。 |