本論文は3章からなり、新しいチオール保護基の開発と抗腫瘍性化合物FR901228の合成研究について述べたものである。第一章はベンジル型チオール保護基を用いたFR901228の合成研究、第二章は新しいチオール保護基の開発、第三章はフタルイミドメチル基をチオール保護基として用いたFR901228の合成研究について述べている。 第一章では、メルカプト基の保護基としてベンジル型の保護基を用いて、FR901228の合成研究を行った結果について述べている。これにより単環性の化合物1は得られたが、メルカプト基の保護基であるベンジル基を除去する際、エステル結合の開裂が先に起こり、より穏やかな条件下で除去できる保護基を用いることが必要であることがわかった(Scheme 1)。 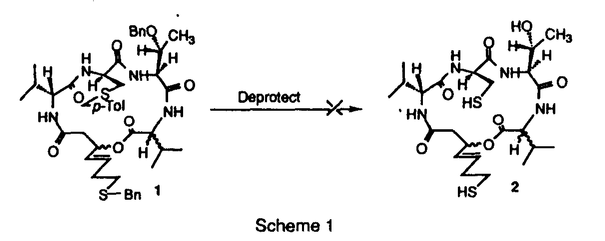 Scheme 1 Scheme 1 また本章において、二価のスズトリフラートを用いるアルドール反応を利用して、FR901228の非ペプチド部分である3-ヒドロキシ-7-メルカプト-4-ペンテン酸の光学活性体を合成する試みについても述べられている。 第二章では、FR901228の合成に利用可能な新しいメルカプト基の保護基として、フタルイミドメチル(Pim)基を開発した結果について述べた。Pim基は、ペプチド合成に広く利用されているメルカプト基の保護基であるアセトアミドメチル(Acm)基と類似したタイプの保護基であり、Acm基がその導入に強酸性条件を必要とするのに対し、Pim基はチオールにトリエチルアミン存在下ハロメチルフタルイミドを作用させることにより容易に導入できる(式1)。またAcm基と異なり、酸性度の高いアミドプロトンを持たないことから、金属エノラートを利用するアルドール反応など塩基性条件を必要とする反応も阻害しない利点がある。またPim基はヒドラジンを作用させた後、酢酸水銀(II)あるいは酢酸銅(II)を作用させることにより容易に除去できることを見出した(式2)。さらに、ジチオール化合物にPim基とAcm基の二つの保護基を導入したものから、Acm基だけを選択的に除去することも可能である。以上のように、Pim基はメルカプト基の保護基としてペプチド合成分野のみならず、有機合成一般にも利用できる優れた保護基と考えられる。 第三章では、第二章で述べたPim基をメルカプト基の保護基として用いたFR901228の合成研究について述べている。 まず、非ペプチド部分に -アミノデヒドロブタン酸部位を含むペプチド部分を導入し、続いて環化反応を行いマクロリド構造をもつ単環性の化合物を得ることができた。しかし、この化合物からメルカプト基の保護基を除去することができなかった。これは -アミノデヒドロブタン酸部位を含むペプチド部分を導入し、続いて環化反応を行いマクロリド構造をもつ単環性の化合物を得ることができた。しかし、この化合物からメルカプト基の保護基を除去することができなかった。これは -アミノデヒドロブタン部位の二重結合がメルカプト基と反応しているのではないかと考え、次に合成の最後の段階でトレオニン部位の脱水反応を行うアプローチの検討を行った。その結果、メルカプト基の保護基としてPim基を用いることにより、FR901228の基本骨格であるジスルフィド結合を含む二環性デプシペプチド骨格を初めて構築することができた。(Scheme 2)。 -アミノデヒドロブタン部位の二重結合がメルカプト基と反応しているのではないかと考え、次に合成の最後の段階でトレオニン部位の脱水反応を行うアプローチの検討を行った。その結果、メルカプト基の保護基としてPim基を用いることにより、FR901228の基本骨格であるジスルフィド結合を含む二環性デプシペプチド骨格を初めて構築することができた。(Scheme 2)。  Scheme 2 Scheme 2 以上、本著者はAcm型の新しいチオール保護基としてPim基を開発し、Acm基の問題点を解決することによって、ペプチド合成分野のみならず有機合成一般にも応用できるチオールの保護基を開発している。また、これを用い、FR901228の基本骨格であるジスルフィド結合を含む二環性の大環状デプシペプチドを構築することにも成功している。この業績は有機合成化学の分野に貢献すること大である。なお、本研究は岩澤伸治氏との共同研究であるが論文提出者の寄与は十分であると判断する。従って、博士(理学)を授与できると認める。 |