多糖類の逐次配列分析法として、酵素法や質量分析計を用いる方法が報告されているが、これらは感度、特異性、価格などの点で各々難点がある。一方、化学的反応に基づく一般的な逐次配列分析法は未だ開発されていない。洪は、アミノナフタレンスルホン酸類を誘導体化試薬として用い、この目的を達成しようとした。即ち、1)本試薬類のアミノ基を介して還元性オリゴ糖の還元末端にUV及び蛍光標識し、2)標識体のスルホン酸基により還元末端側のグリコシド結合を分子内反応により切断、標識化単糖を遊離後、3)これをHPLC分析に付し同定する、4)この1)〜3)のサイクルを繰り返すことにより還元性オリゴ糖の遂次配列が可能であると考えた。本研究では、試薬として溶解性に優れる8-アミノ-2-ナフタレンスルホン酸(ANS)を取り上げ検討した。 1ANSによる誘導体化反応条件検討とHPLC分離条件検討 マルトテトラオースを還元糖のモデル化合物に用い、誘導体化反応条件を検討したところ、シッフ塩基生成反応は、pH6.8、104℃、70分間の条件で完了した。一方、シッフ塩基の還元剤としては水素化ホウ素ナトリウムに比べ、シアノ水素化ホウ素ナトリウムの方が高い反応収率を与え、後者による還元反応は90℃、120分で完了した。 このようにして得られた種々の還元糖のANS誘導体について逆相HPLCによる分離を検討し、D-グルコースとそのオリゴマーについては0.2%ブタノール含有10mMリン酸ナトリウム緩衝液(pH3.8)を、D-ガラクトース、D-マンノースなどの単糖類に対しては0.1%ブタノール含有10mMリン酸ナトリウム緩衝液(pH3.8)を移動相とすることにより良好な分離が得られた。 2ANS化還元性オリゴ糖の配列分析 マルトテトラオースをモデルとし、標識化後、1段階目の切断反応及び回収について種々条件検討を行ったが、糖の回収率が10%以下であり、次の段階の配列分析を行うことが困難であった。これは、誘導体中のスルホン酸基が分子内に共存する第二アミノ基との間でイオン対を形成し、スルホン酸がグリコシド結合切断に働かないためではないかと推定された。そこで、クロロギ酸メチル(MocCl)によりANS化還元性オリゴ糖をメトキシカルボニル(Moc)化させ、アミノ基のプロトン化を抑えることによりスルホン酸基の反応性を高める方法について検討した。 Moc-ANS化マルトトリオース(40mM)を各種比率の1-ブタノール-DMSO(8:2〜4:6)中で90℃、90分間加熱し、1段階目の切断反応率と残存する糖の回収率を求めたところ、遊離Moc-ANS化グルコース生成率及び残存二糖の回収率として各々12.9〜45.1%、及び4.4〜26.9%が得られ、ANS化オリゴ糖を直接切断反応に付した時より回収率の向上がみられた。さらにスルホン酸基によるグリコシド結合の切断反応を分子内で選択的に起こすべく、Moc-ANS化マルトトリオースの濃度を著しく低く設定し検討した。また、反応溶媒の1-ブタノールに代えて低極性のジオキサンを用いた。濃度を45 M、ジオキサン-DMSO(7:3)、反応を30分とし、110〜140℃温度範囲で、切断反応率、回収率などを検討したところ、140℃では切断反応率75%、回収率54.7%であり、切断反応率、回収率がかなり向上したことが明かでありMoc化の有効性が証明された。しかし、非特異な切断も生じていることが判明し、さらに条件の検討が望まれる。 M、ジオキサン-DMSO(7:3)、反応を30分とし、110〜140℃温度範囲で、切断反応率、回収率などを検討したところ、140℃では切断反応率75%、回収率54.7%であり、切断反応率、回収率がかなり向上したことが明かでありMoc化の有効性が証明された。しかし、非特異な切断も生じていることが判明し、さらに条件の検討が望まれる。 他の還元性オリゴ糖としてラクトース(Gal- (1→4)-Glu)、4-0- (1→4)-Glu)、4-0-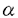 -D-ガラクトピラノシル-D-ガラクトピラノース(Gal- -D-ガラクトピラノシル-D-ガラクトピラノース(Gal-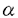 (1→4)-Gal)についてMoc-ANS体を45 (1→4)-Gal)についてMoc-ANS体を45 Mの濃度で、ジオキサン-DMSO(7:3)中、切断反応を140℃、30分間行って配列分析を試みたところ、各サイクルで還元末端側の1残基目に相当するANS化単糖が検出でき、本法による還元性オリゴ糖の逐次配列分析の可能性が示唆された。 Mの濃度で、ジオキサン-DMSO(7:3)中、切断反応を140℃、30分間行って配列分析を試みたところ、各サイクルで還元末端側の1残基目に相当するANS化単糖が検出でき、本法による還元性オリゴ糖の逐次配列分析の可能性が示唆された。 以上、本研究は未完成ではあるが、還元性オリゴ糖の化学的逐次配列分析法への一つの取り組み方を提示したものであり、薬学領域の分析化学の発展に寄与すること大であり、博士(薬学)に価するものと判断した。 |