光増感反応は素反応過程の追跡や励起会合体の構造など物理化学的視野から詳細に研究が行われているものの、有機合成手法としての応用例は非常に限られている。筆者はキラルな1,4-ジシアノベンゼン誘導体を合成し、ジアステレオ選択的な不斉光増感反応の開発を試みた。また、種々の置換1,4-ジシアノベンゼン誘導体の合成法を開発し、これらを用いて光電子移動反応の効率化について検討を行った。
1不斉光増感反応の開発 最近、不斉光増感剤を用いた不斉反応の開発が試みられているが、良い不斉収率が達成されている例はほとんど知られていない。筆者は、分子内に反応基質を保持できるような不斉光増感剤を開発し、これを用いて不斉光増感反応の開発を試みることとした。すなわち、キラルな光増感剤1に反応基質を共有結合により繋ぐことを考え、(R)-(+)-プレゴンより9段階でジシアノフェニルメントール誘導体1を合成した。

次に光増感剤1と3,3-ジフェニル-2-プロペン-1-オールを炭酸エステル2へ誘導し、分子内光増感反応によるメタノールの付加反応を試みた。すなわち、ベンゼン-アセトニトリル混合溶媒中、室温で高圧水銀灯を用いて光照射(300nm≦hv≦320nm)したところ、anti-Markovnikov型付加反応が進行し、対応する炭酸エステル3が61:39のジアステレオマー生成比で得られることがわかった。

さらにフェニルメントール誘導体1をクロトン酸エステル4へ誘導し、クロトン酸部分へのジアステレオ選択的な分子間光アミノメチル化反応を試みた。すなわち、4をジエチル(トリメチルシリルメチル)アミン(5)存在下メタノール-アセトニトリル混合溶液に室温で高圧水銀灯を用いて光照射(300nm≦hv≦320nm)したところ、光アミノメチル化反応が進行し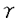 -アミノエステル6がジアステレオマー生成比70:30で得られることがわかった。
-アミノエステル6がジアステレオマー生成比70:30で得られることがわかった。

対照実験として、光増感剤として1,4-ジシアノベンゼン7の存在下フェニルメントールより誘導されるクロトン酸エステルと5との反応を、同様の条件で行ったが、生成物は得られなかった。このことから増感剤に導入されたアルキル置換基が、電子移動反応に大きな影響をもつことが示唆された。
2一重項光増感反応における1,4-ジシアノベンゼン誘導体の置換基効果 光電子移動反応では反応基質から増感剤への電子移動は通常十分に速いが、増感剤のアニオンラジカルから反応基質のカチオンラジカルへの逆電子移動が副反応として存在するため、一般に反応効率は高くない。また、逆電子移動過程に関して、反応基質の置換基効果は報告例があるが、増感剤については詳細には調べられていない。筆者は先に見い出した電子移動反応における増感剤のアルキル置換基効果を詳細に検討するために、種々のメチル置換1,4-ジシアノベンゼン誘導体の合成法の開発を行った。1,4-ジシアノベンゼンの2位置換体の合成法として、1,4-ジシアノベンゼンのリチオ化を検討したところ、THF中-95℃でリチウム 2,2,6,6-テトラメチルピペリジドを作用させるとリチオ化が進行し、続いて種々の求電子剤を作用させると、2位置換1,4-ジシアノベンゼンが良い収率で得られることがわかった。

また、ジおよびテトラメチル置換1,4-ジシアノベンゼンは以下のように合成できる。すなわち、メチル置換p-ヒドロキノンを出発物質として用い,このものをジトリフラートとした後、下記の条件下シアノ化を行うと、メチル置換1,4-ジシアノベンゼン9、10が良好な収率で得られる。

次に、合成した種々の1,4-ジシアノベンゼン誘導体(7〜10)を増感剤とし、6,6-ジフェニル-1,4-ジオキサスピロ[4.5]デカン(12)の6,6-ジフェニルヘキサン酸メチル(13)への光開裂反応を試みたところ、顕著な置換基効果を見出すことができた。増感剤7を用いた場合にはエステル13の収率が25%であるのに対し、増感剤8を用いた場合には95%と向上した。また、光照射時間を3時間と短縮した場合、エステル13の収率は8、9を増感剤とするとそれぞれ43%、65%となり、モノおよびジ置換1,4-ジシアノベンゼンほど反応が速く進行することがわかった。これに対しテトラメチル-1,4-ジシアノベンゼン(10)を用いた場合、反応は進行しなかった。この理由として、10の励起状態での酸化力が十分ではないことが考えられる。
 図表
図表 また、5-メチル-3-フェニル-2,3-デヒドロベンゾフラン(15)の光増感酸化反応を、種々の1,4-ジシアノベンゼン誘導体の存在下アセトニトリル-メタノール中で光照射下試みたところ、この場合にも増感剤のアルキル置換基効果が明らかになった。
 図表
図表 この光増感剤のアルキル置換基効果として、反応基質から光増感剤への一電子移動過程の逆反応である光増感剤のアニオンラジカルから反応基質のカチオンラジカルへの逆電子移動が遅くなるために、反応が効率良く進行したと考えられる。