分子進化の中立説において、大部分の分子進化は事実上中立的な進化をしていることが示されている。機能がない配列などで中立的に進化している場合、進化速度は突然変異率に依存して決まっており、遺伝子などの場合、その遺伝子にかがる機能上の制約から一般に進化速度はこれより低くなる。ごくまれに、逆に進化速度が中立的に期待される値より大きな場合がある。このような加速された進化は突然変異率の上昇、遺伝子変換、あるいは正の淘汰などの結果と考えられる。生物の個体レベルでの適応的な進化という観点から、このような加速された進化の研究は非常に興味深い。この論文において私は加速進化の二つの実例を研究した。 一つは免疫グロブリンアルファ遺伝子のヒンジ領域において見いだされた加速進化である。免疫グロブリンには一般的に変異が多くみられるが、我々の過去の研究から、ヒト上科において免疫グロブリンC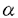 遺伝子のヒンジ領域が進化的に非常に多様性に富むことが示されていた。旧世界猿の同領域を比較したところ、その配列はヒト上科のものと全く異なっていることが示された。この非常に速い進化の様相を明らかにするため、複数種のマカク属およびヒヒ属の末梢血由来のDNAをテンプレートに用いてPCRをおこない、その配列を直接塩基配列決定法により決定、比較した。この実験中、多くのサンプルがヒンジ領域でヘテロ接合となっていることが判明したため、SSCP法によりその多型度の検討をおこなった。この結果、多くの種で複数の対立遺伝子が見いだされ、ヘテロ接合度が確かに高くなっていることが示された。25の独立のサンプルからこのヒンジ領域の塩基配列を決定し、詳細な解析を行った。配列上の類似度から、これらの対立遺伝子は2群に分けられた。一方はヒンジ領域が基本的に23塩基で構成され、もう一方はヒンジ領域が基本的に29塩基で構成されていた。両者ともに、さらに複数塩基が挿入した対立遺伝子の存在も確認された。塩基置換はヒンジ領域の前半部分に集中してみられ、隣接したイントロンおよびCH2ドメインにはこのような高頻度の置換は観察されなかった。さらに、非常に興味深いことに、ヒンジ領域に観察された塩基置換数とアミノ酸置換数は非常に近い値であった。このことは、塩基置換の多くがアミノ酸置換に関わっていたこと、すなわち非同義置換であったことを示す。単純にペアワイズ比較を対立遺伝子間総当たりで行い、(非同義置換/同義置換)の値の平均を計算すると、マカク属間で5.1、ヒヒ属を含めると3.3という値を得た。一般的な遺伝子におけるこの値の平均値は0.19前後であることがLiらにより示されていることから、遺伝子における値としてはヒンジ領域におけるこの値は突出している。さらにより厳密に正淘汰進化の可能性を検証するため、対立遺伝子間の最大節約法による系統樹を作成し、系統樹全体での座位あたりの置換数を同義置換および非同義置換について計算した。その結果、非同義置換/同義置換の値は2.0で、統計学上有意な差は出ないものの非同義置換が同義置換を上回っていることが示された。次に相対的な進化速度の検証を行った。ヒンジ領域はイントロンとCH2ドメインに接している。6対立遺伝子の配列を用いてイントロンとヒンジ領域間で相対的な進化速度の比較を行ったところ、ヒンジ領域では約17倍の置換が起きていることが明らかになった。イントロンでは中立的な進化が起きており、この値よりも高い置換速度であるということは、ヒンジ領域では何らかの非中立的な要素が作用していることを示唆する。加えて、CH2ドメインとヒンジ領域とで非同義置換/同義置換の値を比較したところ、ヒンジ領域が約17倍の値を示した。CH2ドメインの値は0.15と、一般的な遺伝子における値と同様であったことから、やはりヒンジ領域において非同義置換の速度が加速されていることを支持する結果が得られた。次に、一つの種内の多型度およびヘテロ接合度を調べるため、アカゲザル12サンプルおよびカニクイザル20サンプルを用いて、SSCP解析を行った。結果は各々の種内においても非常に多くの多型が観察され、調べられたうち半数以上の個体がヘテロ接合であった。以上の結果を総合すると、非同義置換が同義置換をかなり上回っていること、相対的な置換速度が周辺領域のイントロンおよびCH2ドメインより加速されていること、さらに、種内においても多くの配列バリエーションが保持されていることから考えて、ヒンジ領域において起きている加速進化は、配列バリエーションを増やす方向に起きた正淘汰進化である可能性が高いと結論した。その原因となる要素については現在のところ判明しておらず、この遺伝子がコードする分泌性IgA抗体の機能進化とその環境要因との関係に関する研究が待たれる。 遺伝子のヒンジ領域が進化的に非常に多様性に富むことが示されていた。旧世界猿の同領域を比較したところ、その配列はヒト上科のものと全く異なっていることが示された。この非常に速い進化の様相を明らかにするため、複数種のマカク属およびヒヒ属の末梢血由来のDNAをテンプレートに用いてPCRをおこない、その配列を直接塩基配列決定法により決定、比較した。この実験中、多くのサンプルがヒンジ領域でヘテロ接合となっていることが判明したため、SSCP法によりその多型度の検討をおこなった。この結果、多くの種で複数の対立遺伝子が見いだされ、ヘテロ接合度が確かに高くなっていることが示された。25の独立のサンプルからこのヒンジ領域の塩基配列を決定し、詳細な解析を行った。配列上の類似度から、これらの対立遺伝子は2群に分けられた。一方はヒンジ領域が基本的に23塩基で構成され、もう一方はヒンジ領域が基本的に29塩基で構成されていた。両者ともに、さらに複数塩基が挿入した対立遺伝子の存在も確認された。塩基置換はヒンジ領域の前半部分に集中してみられ、隣接したイントロンおよびCH2ドメインにはこのような高頻度の置換は観察されなかった。さらに、非常に興味深いことに、ヒンジ領域に観察された塩基置換数とアミノ酸置換数は非常に近い値であった。このことは、塩基置換の多くがアミノ酸置換に関わっていたこと、すなわち非同義置換であったことを示す。単純にペアワイズ比較を対立遺伝子間総当たりで行い、(非同義置換/同義置換)の値の平均を計算すると、マカク属間で5.1、ヒヒ属を含めると3.3という値を得た。一般的な遺伝子におけるこの値の平均値は0.19前後であることがLiらにより示されていることから、遺伝子における値としてはヒンジ領域におけるこの値は突出している。さらにより厳密に正淘汰進化の可能性を検証するため、対立遺伝子間の最大節約法による系統樹を作成し、系統樹全体での座位あたりの置換数を同義置換および非同義置換について計算した。その結果、非同義置換/同義置換の値は2.0で、統計学上有意な差は出ないものの非同義置換が同義置換を上回っていることが示された。次に相対的な進化速度の検証を行った。ヒンジ領域はイントロンとCH2ドメインに接している。6対立遺伝子の配列を用いてイントロンとヒンジ領域間で相対的な進化速度の比較を行ったところ、ヒンジ領域では約17倍の置換が起きていることが明らかになった。イントロンでは中立的な進化が起きており、この値よりも高い置換速度であるということは、ヒンジ領域では何らかの非中立的な要素が作用していることを示唆する。加えて、CH2ドメインとヒンジ領域とで非同義置換/同義置換の値を比較したところ、ヒンジ領域が約17倍の値を示した。CH2ドメインの値は0.15と、一般的な遺伝子における値と同様であったことから、やはりヒンジ領域において非同義置換の速度が加速されていることを支持する結果が得られた。次に、一つの種内の多型度およびヘテロ接合度を調べるため、アカゲザル12サンプルおよびカニクイザル20サンプルを用いて、SSCP解析を行った。結果は各々の種内においても非常に多くの多型が観察され、調べられたうち半数以上の個体がヘテロ接合であった。以上の結果を総合すると、非同義置換が同義置換をかなり上回っていること、相対的な置換速度が周辺領域のイントロンおよびCH2ドメインより加速されていること、さらに、種内においても多くの配列バリエーションが保持されていることから考えて、ヒンジ領域において起きている加速進化は、配列バリエーションを増やす方向に起きた正淘汰進化である可能性が高いと結論した。その原因となる要素については現在のところ判明しておらず、この遺伝子がコードする分泌性IgA抗体の機能進化とその環境要因との関係に関する研究が待たれる。 もう一つは単一アミノ酸の繰り返し構造の増幅が高度のGC圧により加速されている可能性に関するものである。POU因子はホメオドメインを含む転写調節タンパクで、クラスIIIPOU遺伝子群は脳神経系の発生分化に重要な役割を持っている。私は様々な動物種のクラスIIIPOU遺伝子の配列を比較しその進化を調べた。この目的のため、全長の配列が決定されていなかったヒトBrain-1のゲノム配列を決定した。近隣結合法により作成された9種19配列の遺伝子系統樹から、脊椎動物に4つのクラスIIIPOU遺伝子グループの存在が示された。これら4つのグループ(Brain-1,Brain-2,Brain-4,Scip)のアラインメントから、ほ乳類の遺伝子に特徴的な配列構造が見いだされた。Brain-1において、ヒトとマウスのアミノ酸配列はほとんど同一であった。これに対して、ゼブラフィッシュのBrain-1ホモローグでは、いくつかのギャップが観察された。これらのギャップはいずれもほ乳類においてグリシン、アラニン、プロリンの単一アミノ酸反復配列が存在している領域であった。ほかのグループには同じ位置にはこれらのアミノ酸配列は存在しておらず、系統樹上から考えて、これらのアミノ酸反復配列は遺伝子が重複して各グループがわかれたのち、主としてほ乳類の系統で挿入されたものと考えられる。同様に、Brain-2,Scipグループにおいても、ほ乳類遺伝子にそれぞれ独立な、前途以外にグルタミン、ヒスチジンの単一アミノ酸反復配列の挿入が観察された。これに対して、Brain-4遺伝子ではほ乳類とそれ以外の遺伝子の配列はほぼ同一であり、単一アミノ酸反復配列は存在せず、他の3グループのようなギャップは見いだされない。これらのグループの間の差違として、私はGC含量の違いに注目した。GC含量は一般的にほ乳類や鳥類では幅が大きく、その他の脊椎動物では比較的均一である。クラスIIIPOU遺伝子において、Brain-1,Brain-2およびScip遺伝子のGC含量をコドンの第三位置で調べたところ、ほ乳類では非常に高く、その他のアミノ酸反復配列を持たない脊椎動物では比較的低い値を示した。これに対して、Brain-4ではほ乳類、その他の脊椎動物ともに比較的低いGC含量であった。これらの関係を示したものが図1である。GC含量と反復配列含量の間には正の相関関係が存在する。反復配列を構成するアミノ酸のコドンはいずれもGC含量の高い配列である。高いGC圧のかかった環境下でGC含量の高いアミノ酸配列が挿入され、それが何らかの機構で増幅されたと推測できる。またクラスIIIPOU遺伝子でみいだされたアミノ酸反復配列はヒトとマウス間でそのアミノ酸配列の組成および長さ両方においてよく保存されている。このことは、ほ乳類の系統において増幅したアミノ酸配列に機能的な制約がかかって保存されてきた可能性を示唆する。ここで観察されたGC含量とグリシン、アラニン、プロリン,グルタミン、ヒスチジンのアミノ酸反復配列との正の相関関係が一般的に成り立つかどうかを検証するため、データベースでこれらの反復配列を含むヒトの遺伝子を検索し、そのGC含量の分布を調べた。その結果、その分布は一峰性分布を示し、その平均値は57%であった(図2)。ヒトでは一般に遺伝子のGC含量は幅広く分布し、その平均値は約50%程度であることから、これらの反復配列を含むヒトの遺伝子群の分布が高GC%に偏っていることが確認された。以上のデータから、単一アミノ酸反復配列の出現と増幅が、高GC圧の下で加速されている可能性が示唆された。免疫グロブリンC 遺伝子における加速された塩基置換の例とクラスIIIPOU遺伝子に代表される偏ったアミノ酸配列の反復配列増幅の加速進化の例は、高等脊椎動物のゲノムが遺伝子配列において柔軟かつダイナミックに変化していることを示している。 遺伝子における加速された塩基置換の例とクラスIIIPOU遺伝子に代表される偏ったアミノ酸配列の反復配列増幅の加速進化の例は、高等脊椎動物のゲノムが遺伝子配列において柔軟かつダイナミックに変化していることを示している。  図表図1 GC含量とリピート含量との相関関係 / 図2 アミノ酸リピートを含む遺伝子のGC含量の分布 図表図1 GC含量とリピート含量との相関関係 / 図2 アミノ酸リピートを含む遺伝子のGC含量の分布 |