人類にとって最大の脅威の一つとしては癌があげられる。長年の努力により、特定の癌については治療法が確立されつつあるものの、固形癌のように既製の抗癌剤が有効でない場合も少なくない。従って、新しい構造と作用機序を持つ抗癌剤の開発が急務となっている。このような観点から、陸上生物とは生息環境が異なり、かつ未開拓な海洋生物から抗癌剤を開発する試みが、1970年代から活発になった。その結果、didemnin B,bryostatin1などの有望な化合物が発見され、海洋生物の医薬資源としての重要性が証明された。 このような背景の下で、本研究では細胞毒性スクリーニングで強い活性が認められた伊豆半島産群体ホヤRitterella tokioka Kott,1992から活性成分の単離と構造解析を試みたところ、ritterazine A-Zと命名した26種のステロイド二量体を得ることができた。さらに、最も活性の強かったritterazine Bについて化学変換を行い、構造-活性相関に関して検討した。概要は以下の通りである。 1単離 伊豆半島下田市田牛で採集したホヤをエタノールで抽出後、P388マウス白血病細胞対する細胞毒性を指標に活性物質の分離・構造決定を行った。すなわち、抽出液の酢酸エチル可溶部を、90%メタノール/ヘキサンおよび60%メタノール/ジクロロメタンで分配した。得られたジクロロメタン相をアセトニトリル-水系のODSフラッシュクロマトグラフィーで分画したところ、70%アセトニトリルで溶出される画分に活性が集中した。さらにSephadex LH-20によるゲルろ過およびODS-HPLCを用いて精製し、ritterazine(リッテラジン)A-MそしてT-Z(1-13,20-26)と命名した細胞毒性物質を得ることができた。また、ODSフラッシュクロマトグラフィーでメタノールで溶出される画分から、ritterazine N-S(14-19)を分離した。 2構造決定 Ritterazine A(1)は無色の固体[[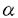 ]D+112.0°(c0.1,MeOH)]で、その分子式を高分解能FABマススペクトルからC54H76N2O10と決定した。1H NMRおよび13C NMRスペクトルから1つの三置換オレフィン、1つのオキシメチン、9つのメチル基および1つのケトン( ]D+112.0°(c0.1,MeOH)]で、その分子式を高分解能FABマススペクトルからC54H76N2O10と決定した。1H NMRおよび13C NMRスペクトルから1つの三置換オレフィン、1つのオキシメチン、9つのメチル基および1つのケトン( 221.2)の存在が示唆された。次に、各種二次元NMR(1H-1H COSY,DQF COSY,and HMQC)スペクトルを解析することにより6個の部分構造を導くことができた。さらに、これらをHMBCスペクトルによってつないで、1の平面構造を得た。なお、構造上重要な14位のスピロ炭素の存在はNMRの解析により確認できた。すなわち、18位のメチルプロトン( 221.2)の存在が示唆された。次に、各種二次元NMR(1H-1H COSY,DQF COSY,and HMQC)スペクトルを解析することにより6個の部分構造を導くことができた。さらに、これらをHMBCスペクトルによってつないで、1の平面構造を得た。なお、構造上重要な14位のスピロ炭素の存在はNMRの解析により確認できた。すなわち、18位のメチルプロトン( 1.30)はCOSYスペクトルで水酸基( 1.30)はCOSYスペクトルで水酸基( 5.28)と遠隔カップリングを示し、かつHMBCスペクトルにおいて13位( 5.28)と遠隔カップリングを示し、かつHMBCスペクトルにおいて13位( 80.9),14位( 80.9),14位( 69.3)および17位( 69.3)および17位( 61.7)の炭素との間にクロスピークを与えた。一方、11位( 61.7)の炭素との間にクロスピークを与えた。一方、11位( 2.35,2.14)および15位( 2.35,2.14)および15位( 2.08,2.24)のメチレンプロトンとケトン( 2.08,2.24)のメチレンプロトンとケトン( 221.2)の間、ならびに11位の 221.2)の間、ならびに11位の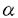 プロトン( プロトン( 2.35)と14位( 2.35)と14位( 69.3)の四級炭素の間に1H-13C遠隔結合が認められることから,転位ステロイド骨格の存在が示された。分子左側は通常のステロイド骨格であった。分子式、UV[ 69.3)の四級炭素の間に1H-13C遠隔結合が認められることから,転位ステロイド骨格の存在が示された。分子左側は通常のステロイド骨格であった。分子式、UV[ max287nm( max287nm( 8580),MeOH]および13C NMRスペクトル( 8580),MeOH]および13C NMRスペクトル( 149.2,149.2,149.0,148.7)から、二つのステロイド骨格がピラジン環を介して結合している化合物であることが判明した。各ステロイドユニットの相対立体配置は主に結合定数とNOESYスペクトルの詳細な解析から明らかにした。なお、2つのステロイド環のピラジン環を介した結合様式は、15N-HMBCスペクトルにおいて1位とN2位、1’位とN3位のプロトンと窒素間にクロスピークが観測されたことから、X線結晶構造解析で構造が明らかにされたインド洋産半索動物Cephalodiscus gilchristi由来のcephalostatin 1 と同じことが判明した。Ritterazine D(4)は1の22-エピ体、一方ritterazine E(5)は4の28-メチル体とそれぞれ決定できた。 149.2,149.2,149.0,148.7)から、二つのステロイド骨格がピラジン環を介して結合している化合物であることが判明した。各ステロイドユニットの相対立体配置は主に結合定数とNOESYスペクトルの詳細な解析から明らかにした。なお、2つのステロイド環のピラジン環を介した結合様式は、15N-HMBCスペクトルにおいて1位とN2位、1’位とN3位のプロトンと窒素間にクロスピークが観測されたことから、X線結晶構造解析で構造が明らかにされたインド洋産半索動物Cephalodiscus gilchristi由来のcephalostatin 1 と同じことが判明した。Ritterazine D(4)は1の22-エピ体、一方ritterazine E(5)は4の28-メチル体とそれぞれ決定できた。 Ritterazine B(2)の分子式は高分解能FABマススペクトルからC54H78N2O9と決定した。1H NMR、13C NMRおよび各種二次元NMRを詳細に解析した結果、ritterazine Aと同様な構造をもつことが明らかとなった。各ステロイドユニットの相対立体配置は結合定数とNOESYデータから決定した。2つのステロイド環のピラジン環を介した結合様式は、15N-HMBCスペクトルの測定とN-メチル誘導体のN-メチル基と1位および4’位との間のNOEから1と同じと結論した。Ritterazine C(3)は2と同一の分子式を有し、類似したNMRスペクトルを与えることからその異性体であることが示唆された。NMRおよびFAB-MS/MSスペクトルを詳細に検討した結果、末端の6員環スピロケタールが5員環スピロケタールに変化した構造をとることが判明した。実際、2を重クロロホルム中に放置したところ、約50%が3に変換した。さらに3の絶対立体配置を新Mosher法を用いて決定した。従って、2の絶対立体配置も3と同一と結論できた。Ritterazine F(6)は2の22-エピ体、ritterazine G(7)は6の14-デヒドロ体、ritterazine H(8)は2の12-ケト体、ritterazine I(9)は6の12-ケト-14ヒドロキシル体とそれぞれ決定した。 Ritterazine J(10)は分子式C54H76N2O11をもち、もっとも高度に酸化された同族体であった。左半分の構造は2と同じであるが、右半分については14位に二重結合、17位に水酸基が存在し、末端が5,6スピロケタールとなっていた。Ritterazine K(11)は10の7’-デヒドロキシル体、ritterazine L(12)は11の17-デヒドロキシル体、およびritterazine M(13)は12の22-エピ体とそれぞれ明らかにできた。 Ritterazine N(14)は1の左半分が転位したステロイド骨格で、ritterazine O(15)は14の22’-エピ体、ritterazine P(16)は14の右半分が2と同一、ritterazine Q(17)は16の22’-エピ体、ritterazine R(18)は3の7’,17’,26’-デヒドロキシル-14’-ヒドロ体、そしてritterazine S(19)は18の22’-エピ体とそれぞれ結論された。 3構造-活性相関 主成分で最も強い活性(IC50=0.15ng/mL)を持つritterazine B(2)を、HCI/MeOHで処理すると17’位の脱水生成物27が得られ、その活性は2300ng/mL(IC50)と約1/10000に低下した。一方、LiAIH4/AlCl3で還元するとF’環が開環したセコ体28が得られ、その活性は240ng/mL(IC50)と約1/1000に低下した。また、PCC/Al2O3で酸化すると、1当量では12位が酸化された12-ケト体8が、過剰量ではさらに7’位が酸化された7’-ketoritterazine H(29)が得られた。面白いことに12’位は酸化されなかった。両者はほぼ同じ細胞毒性を示した。 以上の結果より、ritterazineの活性には17’位の水酸基と左末端の5,6スピロケタールが最も重要であるとが考えられる。また1の7’,17’-デヒドロキシル体であるritterazine T(20)、20の12’-ケト-14’-ヒドロキシル体のritterazine U(21)と16の左末端が5,6スピロケタールとなったritterazine V(22)、20の左末端がスピロ[5,5]となったritterazine W(23)と23の22’-エピ体、ritterazine X(24)の活性が弱いことは、17’位の水酸基の重要性を支持している。しかし、2の7’,17’-デヒドロキシル体のritterazine Y(25)はIC50=3.5ng/mLの活性を示し、酸条件で処理した脱水生成物27と比較すると17’位の水酸基の有無ではなく、この部分のコンフォメーションおよびフレキシビリィティが重要な意味をもつものと推察される。一方、9-13のように分子内に2つの5,6スピロケタールが存在すと活性が弱く、12位が酸化された8と9、および転位ステロイド骨格をもつ1-5がほぼ同程度の活性をもつなど、構造と活性の関係はかなり複雑である。さらに、右半分が1、左半分が27と酷似したritterazine Z(26)は23と比較して活性が極度に弱かった。1の左半分が転位したステロイド骨格を有する14の活性が弱いことを考慮すると、cephalostatin1の17位と23位の水酸基を含む末端のスピロ環部分が大切であるとの結論が導かれる。 以上、伊豆半島産群体ホヤRitterella tokioka Kott,1992から、強い細胞毒性を示すステロイド二量体ritterazine類を単離・構造決定するとともに、構造-活性相関に検討を加え、海洋無脊椎動物の抗癌剤としての有用性を示すと同時に、抗癌剤開発にとって重要な知見を得ることができた。  |