1970年代初めから活発になった海洋生物の二次代謝産物の研究の結果、陸上生物にはない新規な骨格や生物活性を持つ化合物が多く発見され、海洋生物の生化学資源としての有用性が明らかになった。特に、海綿は著しい生物活性と特異な構造をもつ化合物を含むことが多く、抗腫瘍物質などの医薬素材探索の最良のターゲットとなっている。 このような状況の下に、本研究では、新しい抗腫瘍物質の探索と開発を目的として細胞毒性試験で顕著な活性が認められた3種の海綿から活性物質の単離と構造決定を行ったところ、11種の新規化合物を得ることができた。概要は以下の通りである。 1.熱海産Discodermiakiiensisからのdiscodermin類の単離と構造決定 1993年熱海で採集した海綿D.kiiensisにP388マウス白血病細胞に対する顕著な細胞毒性が認められたので、活性成分の単離と構造決定を試みた。凍結海綿(5.0kg)をエタノールで抽出後、細胞毒性を指標に活性成分の分離・精製を試みた。すなわち、濃縮液を水とエーテル、次いで水とn-ブタノールで分配した。活性が認められたn-ブタノール層をODSフラッシュクロマトグラフィーおよびSephadex LH-20を用いるゲルろ過で分画後、最終的に逆相HPLCで精製してdiscodermin E-H(1-4)と命名した4種の活性成分を得た。 Discodermin E(1)はFABMSにおいてm/z1709に(M+H)+イオンピークを与え、1Hおよび13CNMRスペクトルからペプチドと推定された。そこで、アミノ酸分析および2次元NMRより構成アミノ酸を調べたところ、各1モルのAsn、Ala、Leu、Pro、Phe、Arg、Cys(O3H)および2モルのThrに加え、異常アミノ酸t-Leu2モル、MeGln、Sarおよびkynurenine(Kyn)各1モルを含むことがわかった。まず、NMRによる各アミノ酸の同定を次のようにして行った。すなわち、DMSO-d6中で測定したDQF-COSYおよびHOHAHAスペクトルからアミノ酸残基内のスピン系の解析を行い、また、側鎖に4級炭素を含むt-LeuおよびMeGlnとSarのN-メチル基はNOESYとHMBCにより帰属した。さらに、MeGlnとAsnの側鎖のアミドプロトンは、カルボニル炭素が結合したメチレンプロトンとのNOESYクロスピークによって確かめ、異常アミノ酸のKynの存在は二次元NMRおよび標品との13CNMRデータの比較により決定した。これらのアミノ酸配列はアミドプロトンと隣接アミノ酸の プロトンあるいはアミドプロトンとのNOESYスペクトルのクロスピークによって決定した。ところで、discodermin Eはニンヒドリン試薬に陰性で、N末端がブロックされている環状構造を持つものと予測された。事実、N末端アミノ酸のAla残基のアミドプロトンと160.3ppmの炭素の間にHMBCでクロスピークが観測されたので、discodermin EのN末端にホルミル基が結合していることが判明した。さらに、Thr(1)の プロトンあるいはアミドプロトンとのNOESYスペクトルのクロスピークによって決定した。ところで、discodermin Eはニンヒドリン試薬に陰性で、N末端がブロックされている環状構造を持つものと予測された。事実、N末端アミノ酸のAla残基のアミドプロトンと160.3ppmの炭素の間にHMBCでクロスピークが観測されたので、discodermin EのN末端にホルミル基が結合していることが判明した。さらに、Thr(1)の プロトンとSarのカルボニル炭素間にHMBCクロスピークが認められることから、Thr(1)の水酸基がC末端のカルボニル基とエステル結合していると結論した。 プロトンとSarのカルボニル炭素間にHMBCクロスピークが認められることから、Thr(1)の水酸基がC末端のカルボニル基とエステル結合していると結論した。 アミノ酸残基の絶対立体化学はdiscodermin Eの酸加水分解物をMarfey誘導体に導いた後、HPLC分析を行って決定した。また、discodermin Eを脱ホルミル化後、4回エドマン分解に付し得られたデカペプチトを酸加水分解後にMarfey誘導体に導きならびHPLC分析して、4番目と5番目のアミノ酸残基をそれぞれD-t-LeuおよびL-t-Leuと決定した。 同様に解析して、discodermin F(2)は既知のdiscodermin AにおけるD-t-Leuの代りにD- -MeIleが、discodermin G(3)はD-Alaの代りに -MeIleが、discodermin G(3)はD-Alaの代りに -aminobutyric acid(Aba)が、さらにdiscodermin H(4)はL-Pheの代りにL-Tyrが置き換わった構造をもつことを明らかにした。なお、NOESY実験および脱ホルミル体のアミノ酸配列分析から、discodermin Aの構造は12番目と13番目のアミノ酸配列が逆の構造に訂正するであることを示すことができた。 -aminobutyric acid(Aba)が、さらにdiscodermin H(4)はL-Pheの代りにL-Tyrが置き換わった構造をもつことを明らかにした。なお、NOESY実験および脱ホルミル体のアミノ酸配列分析から、discodermin Aの構造は12番目と13番目のアミノ酸配列が逆の構造に訂正するであることを示すことができた。 Discodermin E-HはP388マウス白血病細胞に対してそれぞれ0.02、0.1、0.4および0.1 g/mLの濃度で細胞毒性を示した。 g/mLの濃度で細胞毒性を示した。 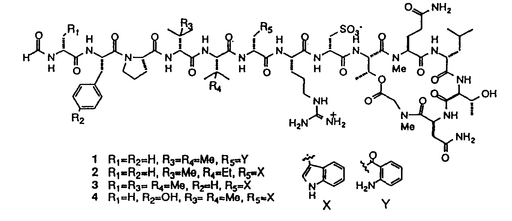 2.屋久島産Hyrtios cf.erectusからのscalarane型セスタテルペン類の単離と構造決定 次に、屋久島産H.cf.erectusの脂溶性画分に強い細胞毒性が認められたので、活性物質の単離・構造決定を試みた。凍結海綿(1.2kg)のエタノール抽出物を水とエーテルで二層分配した。活性が試められたエーテル層をKupchan法により溶媒分画して得られたCCl4およびCH2Cl2層を、Sephadex LH-20を用いるゲルろ過で分離した。強い活性を示す画分からは、既知のaltohyrtin類が得られた。さらにゲルろ過でaltohyrtin類の後から溶出する活性画分を逆相HPLCで精製したところ、3種のscalarane型セスタテルペン5-7を単離した。 5-7は1H NMRのピークの重なりが激しいため、CDCl3/CD3OD(3:1)およびDMSO-d6中で各種2次元NMRを測定し構造決定を試みた。化合物5の分子式は高分解能FABMSおよび13CNMRのデータからC25H38O4と決定した。1HNMRから5つのシングレットメチル,3つのオキシメチンおよび1つのオレフインプロトンの存在が示唆された。さらに、2次元NMRスペクトルより4環性炭素骨格が明らかとなった。また、COSYスペクトルで20位のプロトンは18位および16位のプロトンとのロングレンジカップリングを示し、さらに13C NMRとUV[217nm(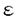 7800)]データから、 7800)]データから、 , , -不飽和- -不飽和- -ラクトンの存在が示唆された。また、20位のプロトンから18位と16位の炭素へHMBCクロスピーク認められることから、ラクトン還がD-環に結合していることが明らかになった。一方、DMSO-d6中でのCOSYスペクトルから、12位と16位に水酸基が結合していることがわかった。 -ラクトンの存在が示唆された。また、20位のプロトンから18位と16位の炭素へHMBCクロスピーク認められることから、ラクトン還がD-環に結合していることが明らかになった。一方、DMSO-d6中でのCOSYスペクトルから、12位と16位に水酸基が結合していることがわかった。 化合物5の立体化学はプロトン間の結合定数値の解析とNOESY実験から明らかにした。16位と15 位の結合定数が11Hzで、いずれもアキシアルであることがわかったので、5は16-epi-16-O-deacetylscalarolbutenolideである。 位の結合定数が11Hzで、いずれもアキシアルであることがわかったので、5は16-epi-16-O-deacetylscalarolbutenolideである。 化合物6の1H NMRスペクトルは、2.10ppmにアセチルのメチルシグナルが存在し12位のプロトンが5に比べ1.38ppm低磁場シフトしていること以外は5のスペクトルと類似していた。また、FABMSから6の分子量は5より42だけ大きいことが示唆されたので、6は5の12位の水酸基がアセチル化された12-O-acetyl-16-epi-16-O-deacetylscalarolbutenolideと決定した。 化合物7は6と同じ分子式を与えたが、1H NMRデータが大きく異なることから別種の炭素骨格をもつことが示唆された。13C NMRデータを検討したところ、化合物7はscalarinのデータとC12およびC21を除いてよい一致を示すことがわかった。そこで各種二次元NMRデータに基づき構造研究を行ったところscalarinの12位のアセトキルシ基が欠落し、21位の炭素がアセトキシル化されていることが判明した。さらにNOESYデータの解析から、相対立体配置を決定した。化合物5-7は、P388細胞に対して0.4,2.1および0.9 g/mLの濃度で細胞毒性を示した。 g/mLの濃度で細胞毒性を示した。 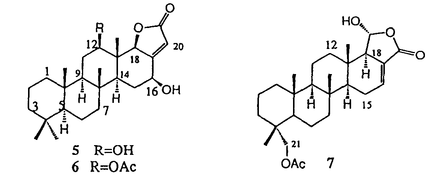 3.馬毛島産Stelletta globostellataからのトリテルペンglobostellatic acid類の単離と構造決定 1993年に馬毛島で採集した海綿Stelletta globostellata(Carter,1883)の脂溶性画分に強い細胞毒性が認められたので活性成分の単離および構造決定を試みた。凍結海綿(1.0kg)をエタノールで抽出後、n-ヘキサンと90%MeOHで二層分配を行った。さらに、90%MeOH画分をODSフラッシュクロマトグラフィー、Sephadex LH-20によるゲルろ過および逆相HPLCで精製して4つの活性成分、globostellatic acids A-D(8-11)を得た。 化合物8の分子式をFABMSおよび13C NMRからC32H43O7Naと決定した。1H NMRから5つのシングレットメチル、2つのビニルメチルおよび5つのオレフィン水素の存在が認めされた。また、13CNMRおよびUVスペクトルデータからmalabaricaneあるいはisomalabaricane骨格をもつものと推定された。COSYおよびHMBCスペクトルより共役ポリエン鎖と3環性炭素骨格の存在が認められたので、さらに詳しく構造解析を行った。すなわち、3環性炭素骨格については、COSYから得られた3つの部分構造を3つのシンダレットメチルから観測されるHMBCクロスピークの情報に基づいて連結することができた。さらに、HMBCデータから24位のカルボキシル基は4位の炭素に、そして12位のケトンは11位の炭素に結合していることが明らかになった。一方、COSYおよびHMBCデータから側鎖にケトンと共役したポリエンが存在し、末端にジメチルカルビノール基が存在すること、ならびにそのケトンが4置換オレフインと結合することが示された。HMBCスペクトルより26位と28位のメチルプロトンからそれぞれ13位の炭素にクロスピークが認められたことから、側鎖と四置換二重結合の結合様式が明らかとなった。側鎖の二重結合の幾何異性は結合定数値およびNOESYデータから16E,18Eおよび20Eと決定した。また、26位と28位のメチル基の間にNOEが認められることから13位の二重結合はZ型と結論した。 3環性部分の立体化学は、B環の13C NMRのケミカルシフト値とNOESYデータからisomalabaricane型であることがわかった。すなわち、B環中のメチン炭素のケミカルシフト値の文献値との比較および26位のメチルと5位および1位の プロトンの間ならびに27位のメチルと9位のプロトン間にNOESYスペクトルでクロスピークが認められたことから、トランスーシスートランス型の立体配置をとることがわかった。さらに24位のメチルと5位のプロトン間にNOESYでクロスピークが認められたこと、ならびに3位と2位のプロトン間のカップリング定数が小さいことから、A環部の立体化学が明らかとなった。同様に、化合物9-11について二次元NMRを中心に構造解析を行い、相対立体配置を含めた構造を決定することができた。 プロトンの間ならびに27位のメチルと9位のプロトン間にNOESYスペクトルでクロスピークが認められたことから、トランスーシスートランス型の立体配置をとることがわかった。さらに24位のメチルと5位のプロトン間にNOESYでクロスピークが認められたこと、ならびに3位と2位のプロトン間のカップリング定数が小さいことから、A環部の立体化学が明らかとなった。同様に、化合物9-11について二次元NMRを中心に構造解析を行い、相対立体配置を含めた構造を決定することができた。 化合物8-11はP388マウス白血病細胞に対し0.1,0.1,0.46および0.1 g/mLの濃度で細胞毒性を示した。 g/mLの濃度で細胞毒性を示した。  以上、新しい構造と作用機序をもつ抗腫瘍物質の探索と開発を目的とし研究を行った結果、日本沿岸産の海綿3種から、11種の新規細胞毒性物質を単離・構造決定することができ、海綿が医薬資源の探索源としで有望であることを示すことができた。 |