| 1.はじめに ヒト正常体細胞は、培養系において有限分裂寿命を示す。この現象は1961年にHayflickとMoorheadによって報告され、細胞老化と定義されている。細胞老化が個体老化の原因であるという根拠はないが、両者の間には相関関係があるとされる。その理由として、1)細胞の示す分裂回数は、その供給者の年齢に反比例する 2)動物種の寿命は、その培養細胞の分裂寿命と正の相関を示す 3)早老症患者から採取した細胞は、著しく分裂寿命が短いこと等が挙げられる。細胞老化の仮説は数多く存在するが、「遺伝的プログラム説」と細胞内に蓄積した障害が原因であるとする「擦り切れ説」の二つに大別される。最近では、遺伝子説の方が主流になりつつあるといえる。また、遺伝解析により、細胞老化は若い細胞に対して遺伝的に優性であり、細胞の不死化(図1)は未知遺伝子の劣性変異により生じることが明らかになってきている。 ヒト正常繊維芽細胞は約60回しか分裂できないが、SV40T抗原遺伝子によっトランスフォームさせると、さらに約20回の分裂寿命の延長を示す。この細胞からは極めてまれな頻度で不死化細胞が出現する(図1)。 延命期の細胞およびSV40T抗原を産生する不死化細胞(図1)において、T抗原を不活性化させると、細胞老化が誘導される。この結果から、細胞老化はSV40T抗原によりバイパスされる細胞老化のステップ(M1)と延命期の細胞の分裂が停止するステップ(M2)が存在するという「二段階説」が提唱された。実際、ヒト正常繊維芽細胞TIG3を温度感受性SV40T抗原でトランスフォームしたのち樹立された不死化細胞株SVts7-1およびSVts8は、許容温度(35℃)では正常に分裂するが、非許容温度(40℃)におくと速やかにかつ不可逆的に分裂能力を失う。この系は、簡便な細胞老化誘導のモデル系として、細胞老化の研究にしばしば採用されている。この系を用いて、細胞老化を制御することを試み、さらに細胞老化の誘導に係わる因子を検索した。  図1.ヒト繊維芽細胞の老化と不死化正常胎児細胞は約60回分裂すると、分裂を停止する(M1)。DNA腫瘍ウイルスを感染させると、約20回の分裂寿命の延長を示したのち、分裂を停止する(M2)。ウイルス感染細胞に劣性突然変異が生じると、無限分裂能を獲得した不死化細胞が出現する。2.細胞老化の制御 図1.ヒト繊維芽細胞の老化と不死化正常胎児細胞は約60回分裂すると、分裂を停止する(M1)。DNA腫瘍ウイルスを感染させると、約20回の分裂寿命の延長を示したのち、分裂を停止する(M2)。ウイルス感染細胞に劣性突然変異が生じると、無限分裂能を獲得した不死化細胞が出現する。2.細胞老化の制御 まず、上記の細胞老化の誘導系において、SVts8細胞を40℃に移したとき、T抗原が速やかに失活し、p53タンパク質がT抗原から遊離することを確認した。次に、細胞老化のマーカーとして注目されているタンパク質、モータリンの挙動を解析した。モータリンはHSP70熱ショックタンパク質ファミリーの一員であり、分裂寿命が有限な細胞では細胞質に均一に分布し、不死化細胞では四つの相補性グループに対応して核膜周辺に局在する四つの異なるパターンを示す。SVts8細胞は35℃では核膜周辺に存在するグループAのパターンを示したが、非許容温度で3〜4日間培養すると、有限寿命型の細胞質分布のパターンを示した。これらの細胞を許容温度に戻しても不死化型へは戻らず、細胞の分裂能力の喪失とモータリンの挙動は一致した。 次に、種々の薬剤をSVts7-1およびSVts8細胞へ投与し、細胞老化の誘導への影響を調べた。シクロヘキシミドは明瞭に老化誘導を阻害したことから、細胞老化の誘導には新生タンパク質が必要なことが示唆された。次に、プロテインキナーゼ阻害剤の効果を調べた。KT5823に代表される幾つかの阻害剤が細胞老化の誘導をほぼ完全に阻止した。それらの阻害特異性を調べると、cGMP依存プロテインキナーゼ(Gキナーゼ)を共通に阻害することが明らかになった(表1)。 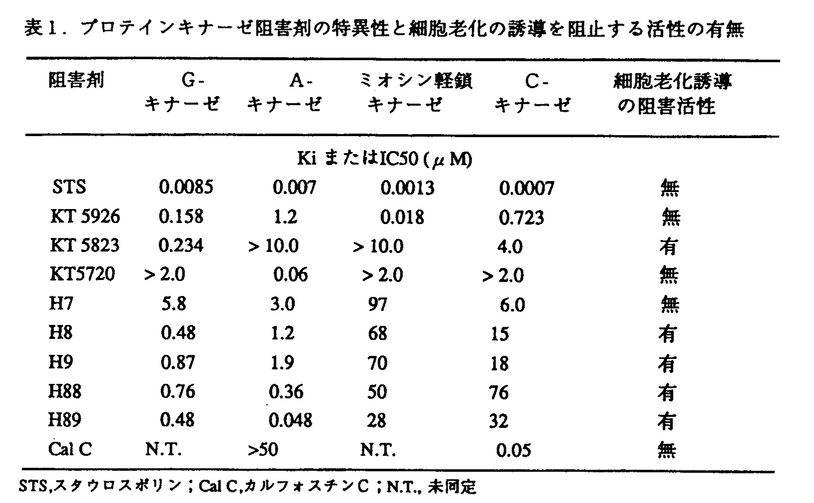 表1.プロテインキナーゼ阻害剤の特異性と細胞老化の誘導を阻止する活性の有無 表1.プロテインキナーゼ阻害剤の特異性と細胞老化の誘導を阻止する活性の有無 また、チロシンキナーゼ阻害剤として知られるゲニステイン、ハービマイシンA、セリン/スレオニンホスファターゼ阻害剤として知られるオカダ酸は効果を示さなかった。これらの結果は、細胞老化にシグナル伝達系が存在することを初めて示唆するとともに、それはGキナーゼが媒介する可能性を示した。 3.cGMP依存プロテインキナーゼの解析 Gキナーゼには、二種類のアイソザイム(タイプI&II)が知られている。そこで、まだヒトよりクローン化されていなかったタイプII遺伝子のクローン化およびその構造決定を行い、Gキナーゼの細胞老化誘導への関与を調べた。Gキナーゼで高度に保存された領域の塩基配列をもとにPCRプライマーを設計し、RT-PCR法によりヒト正常TIG3細胞からcDNA断片を取得した。それをプローブとして同細胞より作製したcDNAライブラリーをスクリーニングし、全長cDNAを単離した。タイプIIcDNAは、762アミノ酸ををコードしていると考えられ、マウスおよびラットホモローグと高い相同性を示した。また、タイプII遺伝子座はFISH解析によって4番染色体上(q21)にマップされ、10番染色体上に位置するタイプI遺伝子とは遺伝的に連関していないことが明かとなった。 ヒト正常繊維芽細胞TIG1.TIG3、WI38細胞におけるタイプIおよびII遺伝子の発現を調べた。両遺伝子の発現とも細胞老化および細胞周期の移行に伴って有意な変動を示さなかった。一方、SV40T抗原でトランスフォームした細胞では、タイプI遺伝子の発現は顕著な変動を示さなかったが、タイプII遺伝子の発現は失われていた。したがって、タイプII遺伝子の発現はT抗原により抑制されることが明かとなった。また、種々の不死化細胞株においても、タイプII遺伝子は発現していなかった。しかし、SVts8細胞での遺伝子発現を調べたり、アンチセンス法を用いた細胞老化の誘導の制御を試みたが、タイプII遺伝子が老化誘導に直接関与するという結果は得られなかった。 4.細胞老化に関与する細胞内因子の検索 阻害剤の細胞内標的を同定することを試みた。KT5823は化学的に不活性な蛍光物質であるので、光化学的に細胞内タンパク質と結合させ、HPLCによって解析したが、有望な結果が得られなかった。そこで、やや特異性の低いH-9をリガンドとしたアフィニティーカラムを作製し、H-9に特異的に結合するタンパク質を解析した。SVts8細胞から核および細胞質タンパク質を抽出し、H-9に結合するタンパク質をSDS-ゲル電気泳動で分離したが、老化誘導に伴って量的に変動するタンパク質は検出できなかった。次に、H-9に結合するタンパク質のリン酸化レベルの変動を調べた。アフィニティーカラムから溶出したタンパク質をSDS-ゲル電気泳動で分離し、抗リン酸化セリン/スレオニン/チロシンに対する各抗体をプローブとしてウエスタンブロット解析を行った。抗リン酸化チロシン抗体では差を検出できなかったが、抗リン酸化セリンまたはスレオニン抗体を用いたとき、35℃で明瞭に検出されたある特定のタンパク質のリン酸化が、40℃で著しく減少していた。このことより、T抗原の不活性化により、ある種のホスファターゼが誘導され、それが上記のタンパク質を脱リン酸化する可能性が示唆された。現在、これらのタンパク質の精製を行っており、老化誘導のシグナル伝達系への関与に興味がもたれる。 また、前述したように老化誘導には新規のタンパク質合成が必要なこと、さらに、T抗原の不活性化によりp53/pRb転写調節因子の機能が回復することなどから考えて、本老化誘導系においてもある特定のタンパク質が誘導される可能性が高いと思われた。そこで、ビオチン-フェノール法を用いたcDNAサプトラクションを行ない、40℃において特異的に発現する遺伝子のクローン化を試みた。その結果、mRNAレベルの誘導を示す数個の新規cDNAクローンを取得した。現在これらのクローンの解析を行なっている。 以上のように、細胞老化に関与すると考えられるシグナル伝達系の解明にはまだほど遠いが、幾つかの新しいアプローチによって、細胞老化の誘導と密接に関連するタンパク質因子およびcDNAクローンが発見された。今後、それらの解析が進めば、細胞老化の分子機構が明らかになることが期待される。 |