学位論文要旨
| No | 112083 | |
| 著者(漢字) | 熊本,卓哉 | |
| 著者(英字) | ||
| 著者(カナ) | クマモト,タクヤ | |
| 標題(和) | キラルリチウムアルコキシドを用いたアキラルホスホネートのエナンチオ選択的不斉Horner-Wadsworth-Emmons反応の開発 | |
| 標題(洋) | ||
| 報告番号 | 112083 | |
| 報告番号 | 甲12083 | |
| 学位授与日 | 1996.03.29 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(薬学) | |
| 学位記番号 | 博薬第748号 | |
| 研究科 | 薬学系研究科 | |
| 専攻 | ||
| 論文審査委員 | ||
| 内容要旨 | Horner-Wadsworth-Emmons反応は,ホスホネートと,アルデヒドやケトンなどのカルボニル化合物から,炭素-炭素2重結合を構築する反応である.カルボニル化合物として,4-tert-butylcyclohexanoneなどのプロキラルケトンを用いた場合,得られる化合物は軸不斉を有するため,本反応を不斉反応としてとらえることができる.すでにいくつかの例が報告されているが,いずれもキラルなホスホネートを用いたジアステレオ選択的不斉反応である. ところで我々は,methyl phenylacetateとmethyl acrylateのエナンチオ選択的不斉Michael付加反応において,キラル塩基として,リチウムを含む5員環キレート構造をとりうるキラルリチウム2-アミノアルコキシドが有効であることを報告した1.この反応では,キラルな外部配位子,すなわちキラルアミノアルコールが,アキラルなリチウムエノラートに配位することにより,エノラートのエナンチオ面を識別することが可能なキラルな錯体が形成されている,と考えられる.この概念はアキラルホスホネートを用いる不斉反応にも適用できると考え,キラル塩基としてキラルリチウム2-アミノアルコキシドを用いた,アキラルホスホネートとプロキラルケトンのエナンチオ選択的不斉Horner-Wadsworth-Emmons反応の開発を試みた. キラルリチウムアルコキシド(4a)のtoluene溶液にホスホネート(2a-b)を加えた後,4-tert-butylcyclohexanone(1)と反応させ,対応するオレフィンを得た.ホスホネートとして2aを用いた場合,化学収率は低く,不斉も誘起されなかった.一方,2bを用いると反応は速やかに進行し,わずかではあるが不斉誘起がみられた(Scheme1,Table1). 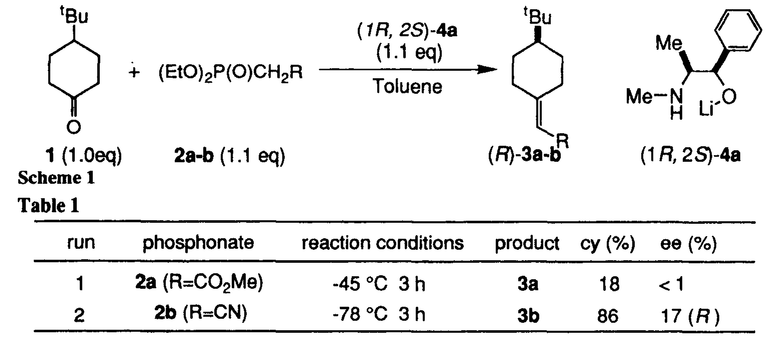 次に,4aの窒素上の置換基の効果を調べた.置換基がよりかさ高くなるにつれて不斉収率が向上し,4dを用いたときに化学収率92%で,52%eeの(R)-3bが得られた.4dより,さらにかさ高い置換基を有するアルコキシド(4e,4f)でも,同等の不斉収率を示した.3座,および4座配位型のアルコキシドでは不斉収率は低下した.一方,分子内配位子を有しない5では,不斉は誘起されなかった(Scheme2,Table2). 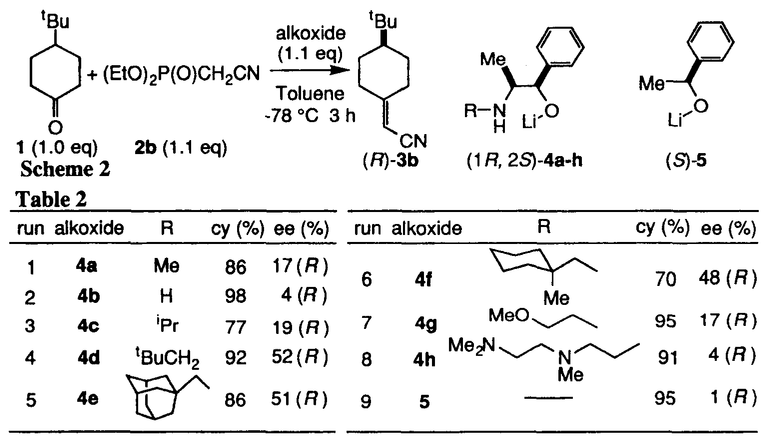 本反応の不斉収率は,用いる溶媒に顕著な影響を受ける. 4dを用いた場合,tolueneが最も良い結果を与えた.Et2Oを用いると不斉収率は低下し,THF,DMEでは不斉は誘起されなかった.また,tolueneを用いたときに,外部配位子としてHMPA1.0当量を添加すると,不斉収率の低下が見られた.溶媒の配位能が高くなるにつれて不斉収率が低下することから,配位能の高い溶媒中では,ホスホネートのリチウム塩が溶媒和され,不斉誘起に有効な,キラルアミノアルコールとの錯体の形成が妨げられている,と考えることができる(Scheme3,Table3). 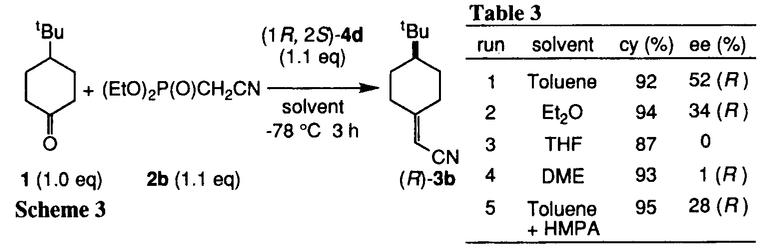 生成物が 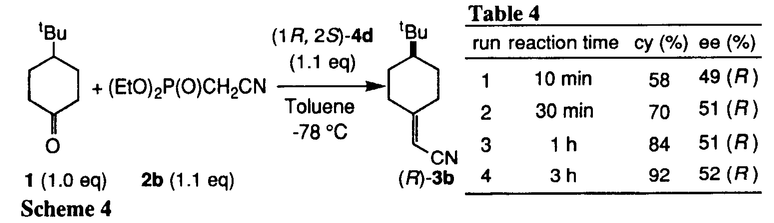 本反応は,アルドール反応と,アルドール体からホスフェートが脱離する反応の2段階の反応からなる. まず,アルドール反応におけるエナンチオ選択性を調べることと,アルドール中間体の合成の目的で,TMSClによるアルドール体の捕捉を試みた.しかし,所望のアルドール体は得られず,(R)-3bをわずかに得るのみであった(化学収率33%,7%ee)(Scheme5). 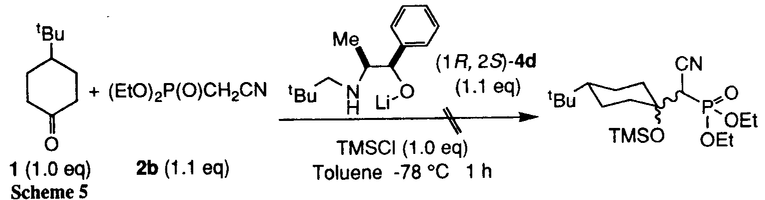 一方,脱離反応については,アルドール体を別途合成し,キラル塩基で処理することにより検討することとした.アルドール体((±)-6)は,THF中,ホスホネートのマグネシウム塩から合成した.(±)-6の相対配置は,同じ条件下で合成し,1H-NMRで同様の化学シフトを示す4-phenyl誘導体のX線結晶構造解析の結果より,tert-butyl基と水酸基がcisであると推定される.(±)-6を1.1当量の4dで処理すると,化学収率89%で,52%eeの(R)-3bが得られた(Scheme6). 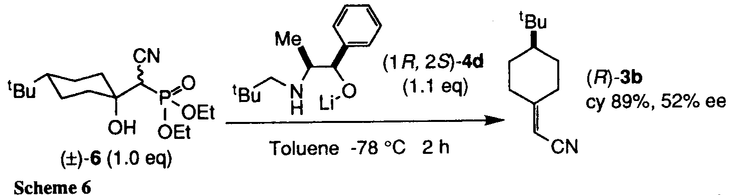 (±)-6の水酸基が脱プロトン化された後,直ちにホスフェートが脱離すれば,ラセミ体の3bが生成するはずである.しかし、実際に得られた3bは光学活性体であった.この理由として,(±)-6からのレトロアルドール反応が考えられる.すなわち,一旦ケトンと,ホスホネートのリチウム塩に戻ったのち,再び反応が進行していると予想される.これは,実際の不斉反応と不斉収率が一致すること,およびbenzaldehyde存在下の脱離反応においてcinnamonitrile(7)が生成することから示唆される(Scheme7). 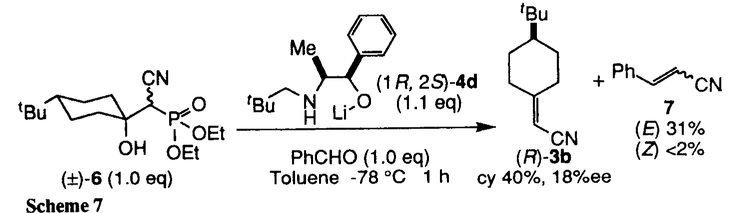 一方,アルドール体のアニオンとキラルアミノアルコールとの錯体はジアステレオトピックな関係にあるためその錯体の安定性,すなわち脱離反応の速度に差が生じることが予想される.不安定な錯体からの脱離反応が進行すると共に,レトロアルドール反応による平衡を介して不安定な錯体が供給された結果,不斉誘起が観察されたと思われる. 本研究により,アキラルホスホネートとプロキラルケトンのエナンチオ選択的不斉Horner-Wadsworth-Emmons反応が可能であることを初めて見いだした.本反応には,分子内配位子を有し,リチウムを含む5員環キレート構造をとりうるキラルリチウム2-アミノアルコキシドが有効である. また,中間体のアルドール体の脱離反応の検討から,レトロアルドール反応による熱力学的コントロールが,本反応の不斉誘起に重要な役割を果たしていることが示唆された. | |
| 審査要旨 | 金属アルコラートは有機合成化学に繁用される塩基である。さきに本論文提出者は、キラルな金属アルコラートを設計し、キラルな塩基として用いる可能性を検討し、5員環キレートを形成し得るキラルなリチウム2-アミノアルコキシドが、エナンチオ選択的な不斉マイケル反応において有効に機能し得ることを実証した。本論文は、このキラルな金属アルコラートを用い、エナンチオ選択的な不斉Horner-Wadsworth-Emmons反応を開拓した経緯を記したものである。 Horner-Wadsworth-Emmons反応は、ホスホネートを塩基によって対応するアニオンとし、これを用いてアルデヒドやケトンのカルボニル基を炭素-炭素二重結合に変換する反応であり、カルボニル化合物によっては、二重結合のまわりの軸不斉に由来するキラルな生成物が得られる。キラルなホスホネートを用いたジアステレオ選択的な不斉合成はすでに報告があるが、アキラルなホスホネートを用いたエナンチオ選択的な不斉合成の例は、これまで知られていなかった。本研究は、上記の不斉マイケル反応の検討で得た考え方を展開したものであり、ホスホネートをキラルな金属アルコキシドで脱プロトン化したとき、得られるホスホネートの金属塩あるいはアルドール付加体の金属塩の金属にキラルアルコールが配位することによって、その反応におけるエナンチオ面の識別を実現しようとするものである。 4-tert-butylcyclohexanone(1)をカルボニル化合物とし、様々なホスホネート、様々なキラル金属アルコラートを用いて反応を検討した結果、ホスホネートとして2、キラル金属アルコラートとして3を用いたとき、軸不斉化合物((R)-4)が92%(52%ee)で得られることを見出した。金属アルコラートとしては、5員環キレート構造を取り得るキラルなリチウム2-アミノアルコキシドが最適であり、キレート環を形成しない単純な単配座型アルコキシド(例えば5)では不斉は誘起されない事が示された。また、3における窒素上の置換基は、メチレンを挟んで大きな基を持つことが必要であり、ここにリチウムに対する配位子となり得る置換基をさらに導入(例えば6)しても良い結果は得られないことも明らかになった。
本不斉反応は、アルドール付加と、それに引き続くのホスフェート脱離の2段階の反応である。本不斉反応条件下でのアルドール付加体の単離には成功しなかったが、MeMgBrを塩基として用いることにより、アルドール付加体の両ジアステレオマー(dl-7およびdl-8)を単離することが出来た。これらを本不斉反応条件に付すと、下記の結果が得られた。
この結果から本不斉反応は、レトロアルドール反応を含むものであり、アルドール付加段階および脱離段階のいずれの段階も不斉収率に影響を与えていると結論された。 以上、本研究は、アキラルホスホネートと4-置換シクロヘキサノンのHorner-Wadsworth-Emmons反応において、キラルリチウム2-アミノアルコキシドを塩基として用いることにより、エナンチオ選択的な不斉反応が実現できることを見出したもので、有機合成化学に寄与するであり、博士(薬学)の学位に値するものであると認める。 | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/54537 |
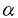 ,
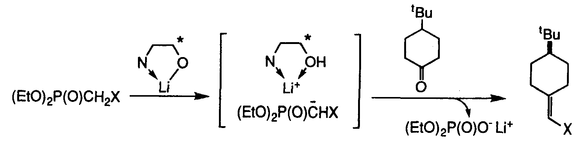
,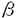 -不飽和化合物であるため,キラルアミンなどがMichael付加-逆Michael反応を起こしてラセミ化する可能性がある.そこで,種々の反応時間で検討した.いずれの反応時間においても不斉収率には大きな変化はなかった.よって,反応が完結するまでの間にはラセミ化は起きていないと思われる(Scheme4,Table4).
-不飽和化合物であるため,キラルアミンなどがMichael付加-逆Michael反応を起こしてラセミ化する可能性がある.そこで,種々の反応時間で検討した.いずれの反応時間においても不斉収率には大きな変化はなかった.よって,反応が完結するまでの間にはラセミ化は起きていないと思われる(Scheme4,Table4).