出芽酵母のSEP1遺伝子産物(Sep1p)は、DNAの組換え、RNA代謝、微小管形成、胞子形成、テロメアの形成・分離、細胞老化など、細胞内の様々な機能に関与していることが知られている。哺乳動物におけるこSep1p様蛋白質の役割を考えたとき、少なくとも配偶子の形成や個体の老化に関与していることが予想されるが、実際に配偶子形成のどの段階で必要とされるのか、個体の老化にどのように影響を与えるのかということを明らかにすることは、まだまだ不明な点が多い哺乳動物の配偶子形成や老化の全体像の解明に新たな手がかりを与えることになると考えられる。また、配偶子形成と老化に限らず、酵母で明らかにされているSEP1関連遺伝子の様々な機能が、哺乳動物でどのように反映されるのかは興味ある問題である。そこで、本研究では、実験材料として、遺伝子操作が一般的に行われるようになってきたマウスを選び、マウスにおけるSEP1関連遺伝子の機能の解明を目指すことにした。マウスのSEP1関連遺伝子に関する変異マウスを作製するのが方法として最も有効であると考え、まず、マウスのSEP1関連遺伝子のcDNAの単離を試みた。 マウスの精母細胞cDNAライブラリーを探索した結果、2つのSEP1関連遺伝子のcDNAのクローニングに成功した。これらを、Dhm1、Dhm2と名付けた。 このうち、Dhm2pは1687アミノ酸からなると予想され、Sep1pとの間で高い相同性を示した(図1A)。 ノザン分析の結果、Dhm2の発現は、精巣特異的に行われていたことから(図2A)、マウスの配偶子形成への関与が強く示唆された。さらに、Dhm2は過剰発現下で、出芽酵母のsep1変異体( sep1)の示す、生育の遅れ、胞子形成不能(spo-)、組換え頻度の低下という3つの欠損を、いずれもSEP1過剰発現下のレベルまで回復させた(表1)。このことは、Dhm2が構造上だけでなく、機能的にもSEP1と相同であることを示している。 sep1)の示す、生育の遅れ、胞子形成不能(spo-)、組換え頻度の低下という3つの欠損を、いずれもSEP1過剰発現下のレベルまで回復させた(表1)。このことは、Dhm2が構造上だけでなく、機能的にもSEP1と相同であることを示している。  表1 マウスDhm2による、sep1変異の相補a,SEP1あるいはマウスDhm2cDNAをpYG30ベクターに連結し(SEP1,Dhm2)、出芽酵母のGAPDプロモーターによってsep1変異体内で過剰発現させた; b,胞子形成を48時間誘導した後の胞子の割合; c,減数分裂誘導後12時間経過したときの、his1-1/his1-7→His+の組換えの頻度; d,液体培地中でのOD600の倍加時間; e,親水性に富んだDhm2pのC末端の119アミノ酸分を欠失させたもので、欠失させない場合に比べて酵母内での安定性が増加していると思われる; f,実験はすべて6回以上行い、平均値と標準誤差を求めた(平均値±標準誤差) 表1 マウスDhm2による、sep1変異の相補a,SEP1あるいはマウスDhm2cDNAをpYG30ベクターに連結し(SEP1,Dhm2)、出芽酵母のGAPDプロモーターによってsep1変異体内で過剰発現させた; b,胞子形成を48時間誘導した後の胞子の割合; c,減数分裂誘導後12時間経過したときの、his1-1/his1-7→His+の組換えの頻度; d,液体培地中でのOD600の倍加時間; e,親水性に富んだDhm2pのC末端の119アミノ酸分を欠失させたもので、欠失させない場合に比べて酵母内での安定性が増加していると思われる; f,実験はすべて6回以上行い、平均値と標準誤差を求めた(平均値±標準誤差)  sep1では、テロメアにおける機能の異常が原因となって、spo-、テロメアの短絡化、細胞の老化といった表現型を示すと考えられている。Dhm2が sep1では、テロメアにおける機能の異常が原因となって、spo-、テロメアの短絡化、細胞の老化といった表現型を示すと考えられている。Dhm2が sep1のspo-を相補するという結果は、Dhm2がテロメアにおいて機能し、配偶子形成のみならずマウスの老化にも関与している可能性を示しており、非常に興味深い。 sep1のspo-を相補するという結果は、Dhm2がテロメアにおいて機能し、配偶子形成のみならずマウスの老化にも関与している可能性を示しており、非常に興味深い。 一方、Dhm1pは947アミノ酸からなることが予想され、Sep1p或いはDhm2pとも相同性を示すが(図1C)、それよりもDhp1pの間で非常に高い相同性が認められた(図1B)。dhp1+は分裂酵母のSEP1ホモログであり、dhp1+とSEP1の遺伝子産物の構造はよく類似しているが、dhp1+が生育に必須な遺伝子であるのに対してSEP1は必須ではない点で両者は大きく異なる。Dhm1をプローブとしたノザン分析の結果、Dhm1の発現は調べた中ではすべての臓器でみられ、Dhm1がマウスにおいても必須遺伝子であることをうかがわせた(図2B)。またその中でも精巣での発現が多く、Dhm2と同様に配偶子形成への関与が示唆された。 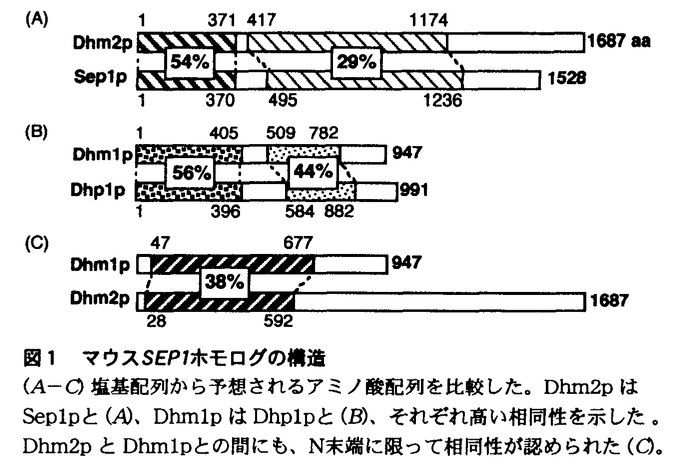 図1 マウスSEP1ホモログの構造(A-C)塩基配列から予想されるアミノ酸配列を比較した。Dhm2pはSep1pと(A)、Dhm1pはDhp1pと(B)、それぞれ高い相同性を示した。Dhm2pとDhm1pとの間にも、N末端に限って相同性が認められた(C)。 図1 マウスSEP1ホモログの構造(A-C)塩基配列から予想されるアミノ酸配列を比較した。Dhm2pはSep1pと(A)、Dhm1pはDhp1pと(B)、それぞれ高い相同性を示した。Dhm2pとDhm1pとの間にも、N末端に限って相同性が認められた(C)。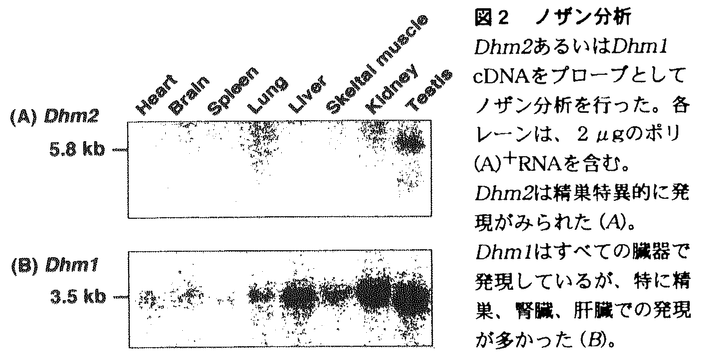 図2 ノザン分析Dhm2あるいはDhm1cDNAをプローブとしてノザン分析を行った。各レーンは、2 図2 ノザン分析Dhm2あるいはDhm1cDNAをプローブとしてノザン分析を行った。各レーンは、2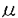 gのポリ(A)+RNAを含む。Dhm2は精巣特異的に発現がみられた(A)。Dhm1はすべての臓器で発現しているが、特に精巣、腎臓、肝臓での発現が多かった(B)。 gのポリ(A)+RNAを含む。Dhm2は精巣特異的に発現がみられた(A)。Dhm1はすべての臓器で発現しているが、特に精巣、腎臓、肝臓での発現が多かった(B)。 dhp1+とDhm1はともに生体内での機能は全く不明であったので、まず取り扱いの容易な分裂酵母を用いて、dhp1+に関する変異体を作製することによってdhp1+の機能を明らかにしようと考えた。dhp1+に関する変異体を用いた解析を行うことによって、マウスにおけるDhm1の機能が推測できるだけでなく、Dhm1に関する変異マウスを作製する際の手がかりが得られると思われた。 dhp1+に関する分裂酵母の高温感受性変異体であるdhp1-1ts株を単離し、その表現型を調べたところ、dhp1-1ts株では、高温でM期の染色体分配の過程が異常になっていることがわかった(図3D,E)。つまりdhp1+は染色体分配の過程に要求されることが初めて明らかになった。 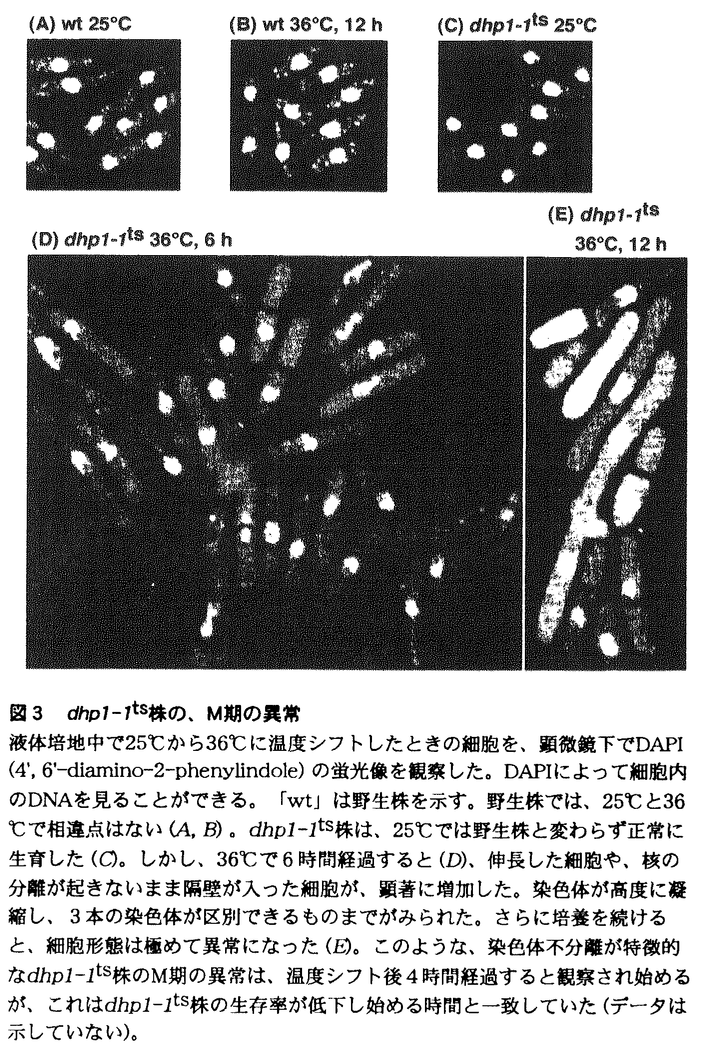 図3 dhp1-1ts株の、M期の異常液体培地中で25℃から36℃に温度シフトしたときの細胞を、顕微鏡下でDAPI(4’,6’-diamino-2-phenylindole)の蛍光像を観察した。DAPIによって細胞内のDNAを見ることができる。「wt」は野生株を示す。野生株では、25℃と36℃で相違点はない(A,B)。dhp1-1ts株は、25℃では野生株と変わらず正常に生育した(C)。しかし、36℃で6時間経過すると(D)、伸長した細胞や、核の分離が起きないまま隔壁が入った細胞が、顕著に増加した。染色体が高度に凝縮し、3本の染色体が区別できるものまでがみられた。さらに培養を続けると、細胞形態は極めて異常になった(E)。このような、染色体不分離が特徴的なdhp1-1ts株のM期の異常は、温度シフト後4時間経過すると観察され始めるが、これはdhp1-1ts株の生存率が低下し始める時間と一致していた(データは示していない)。 図3 dhp1-1ts株の、M期の異常液体培地中で25℃から36℃に温度シフトしたときの細胞を、顕微鏡下でDAPI(4’,6’-diamino-2-phenylindole)の蛍光像を観察した。DAPIによって細胞内のDNAを見ることができる。「wt」は野生株を示す。野生株では、25℃と36℃で相違点はない(A,B)。dhp1-1ts株は、25℃では野生株と変わらず正常に生育した(C)。しかし、36℃で6時間経過すると(D)、伸長した細胞や、核の分離が起きないまま隔壁が入った細胞が、顕著に増加した。染色体が高度に凝縮し、3本の染色体が区別できるものまでがみられた。さらに培養を続けると、細胞形態は極めて異常になった(E)。このような、染色体不分離が特徴的なdhp1-1ts株のM期の異常は、温度シフト後4時間経過すると観察され始めるが、これはdhp1-1ts株の生存率が低下し始める時間と一致していた(データは示していない)。 さらに、マウスのDhm1は、過剰発現下でこのdhp1-1ts変異を相補した(図4)。このことから、Dhm1がdhp1+と構造的にも機能的も相同であることが示され、Dhm1がマウスの細胞の染色体分配に関与していることが示唆された。また、dhp1-1ts変異は野性型Dhp1pのC末端領域を欠失させる変異であり、このような変異蛋白質は、低温でもDhp1pとしての活性が弱まっていることが示唆された(データは示していない)。このことから、Dhm1についても、Dhm1pのC末端が欠失するような変異を導入することで、変異マウスが得られる可能性が示された。 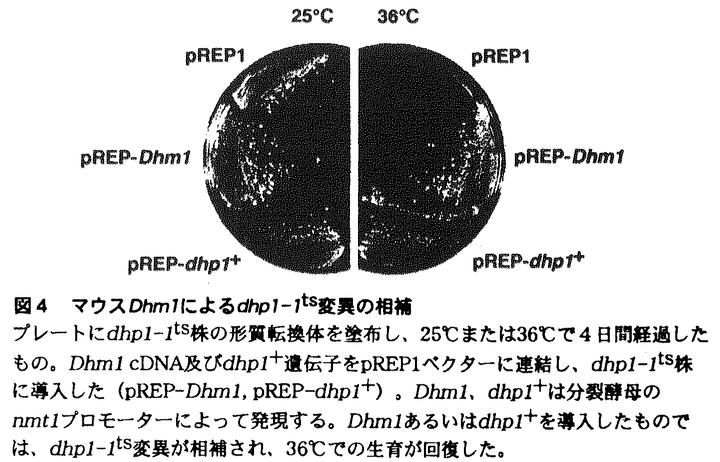 図4 マウスDhm1によるdhp1-1ts変異の相補プレートにdhp1-1ts株の形質転換体を塗布し、25℃または36℃で4日間経過したもの。Dhm1cDNA及びdhp1+遺伝子をpREP1ベクターに連結し、dhp1-1ts株に導入した(pREP-Dhm1,pREP-dhp1+)。Dhm1、dhp1+は分裂酵母のnmt1プロモーターによって発現する。Dhm1あるいはdhp1+を導入したものでは、dhp1-1ts変異が相補され、36℃での生育が回復した。 図4 マウスDhm1によるdhp1-1ts変異の相補プレートにdhp1-1ts株の形質転換体を塗布し、25℃または36℃で4日間経過したもの。Dhm1cDNA及びdhp1+遺伝子をpREP1ベクターに連結し、dhp1-1ts株に導入した(pREP-Dhm1,pREP-dhp1+)。Dhm1、dhp1+は分裂酵母のnmt1プロモーターによって発現する。Dhm1あるいはdhp1+を導入したものでは、dhp1-1ts変異が相補され、36℃での生育が回復した。 |