免疫応答の調節において重要な役割を担っているCD8+T細胞の機能はいまだに充分に解明されていない。本研究ではこのCD8+T細胞の抑制作用の解析、およびその応答性の制御を目的として行われている。特に応答性の制御は基本的な免疫系の作用機序を明らかにするのみならず、アレルギーや自己免疫疾患といった免疫系の異常によって生じる疾患の治療や予防への応用に重要な知見を与えてくれるものである。また本研究は、腸管内のCD8+T細胞に注目して、CD8+T細胞クローンおよび遺伝子欠損マウスを用い、抑制活性を有しているサイトカインのCD8+T細胞クローンからの産生を中心に、その産生パターン、産生機序、産生の制御、さらには生体における役割についての解析を行ない新しい知見を得た。本論文は2章よりなる。 第一章第一節では、免疫系の調節のうち抑制制御に注目し、様々な特異性を有するCD8+T細胞からの抑制活性を有するサイトカイン(IFN- 、IL-10、IL-4)を中心にその産生パターンを検討した。その結果、IFN- 、IL-10、IL-4)を中心にその産生パターンを検討した。その結果、IFN- とIL-10がすべてのCD8+T細胞クローンにおいて産生されることを明らかにした。 とIL-10がすべてのCD8+T細胞クローンにおいて産生されることを明らかにした。 第二節では、第一節で明らかにされたIFN- とIL-10の産生機構の解析を行い、CD8+T細胞クローンからのIFN- とIL-10の産生機構の解析を行い、CD8+T細胞クローンからのIFN- とIL-10の産生誘導のメカニズムは異なっており、cAMPを介したPKA経路を使い分けている可能性を示している。 とIL-10の産生誘導のメカニズムは異なっており、cAMPを介したPKA経路を使い分けている可能性を示している。 第三節では、CD8+T細胞クローンの応答性の抗原特異的な制御を、これらのクローンが認識するT細胞抗原決定基に変異を加えたアナログペプチドを用いて試みている。その結果、IL-10のみの産生を誘導するパーシャルアンタゴニスト、また応答性を阻害するTCRアンタゴニスト、さらにはIFN- 産生の促進を誘導するアナログペプチドの同定に成功し、CD8+T細胞の反応性を制御することに成功している。同時に、クローンレベルだけではなく、ポリクローナルなCD8+T細胞でも、その応答性の制御に成功しており、応用面上意義深い結果が得られている。以上、アナログペプチドを用いたCD8+T細胞応答性の制御で得られた結果は、アレルギーの予防や治療に応用できだけではなく、CD8+T細胞のTCRを介した抗原認識機構の解析という基礎免疫学的な側面においても重要な知見を与えるもである。 産生の促進を誘導するアナログペプチドの同定に成功し、CD8+T細胞の反応性を制御することに成功している。同時に、クローンレベルだけではなく、ポリクローナルなCD8+T細胞でも、その応答性の制御に成功しており、応用面上意義深い結果が得られている。以上、アナログペプチドを用いたCD8+T細胞応答性の制御で得られた結果は、アレルギーの予防や治療に応用できだけではなく、CD8+T細胞のTCRを介した抗原認識機構の解析という基礎免疫学的な側面においても重要な知見を与えるもである。 さらに、本研究の第二章では、CD8+T細胞の構成割合が高いことは周ねく知られているが、未だにその機能および腸管内における役割が全く明らかにされていない小腸上皮内リンパ球(IELs)に注目して研究を行っている。 第二章第一節では、IELsが小腸上皮内に存在していることから、IELsと小腸上皮細胞(IECs)の相互作用について遺伝子欠損マウスを用いて解析し、  IELsおよび IELsおよび 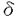 IELsは小腸上皮細胞の分化発達に作用しうること、更にその活性は IELsは小腸上皮細胞の分化発達に作用しうること、更にその活性は  IELsが IELsが 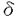 IELsよりも高いことを初めて明らかにしている。 IELsよりも高いことを初めて明らかにしている。 第二節では、  IELsおよび IELsおよび 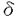 IELsの相互作用ついて解析しており、 IELsの相互作用ついて解析しており、  IELsは IELsは 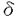 IELsが存在しなくても、サイトカイン産生及び細胞傷害活性を有するが、 IELsが存在しなくても、サイトカイン産生及び細胞傷害活性を有するが、 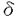 IELsがこれらの機能を獲得するには、 IELsがこれらの機能を獲得するには、  TCRもしくはTCR TCRもしくはTCR 鎖が必要であることを初めて明らかにしている。 鎖が必要であることを初めて明らかにしている。 第三節ではIELsのペプチドの経口投与による活性化を検討している。その結果、IELsはペプチドの経口投与群で高いIFN- の産生が認められ、経口抗原に対してIELsが反応してIFN- の産生が認められ、経口抗原に対してIELsが反応してIFN- を産生することを初めて明らかにしている。 を産生することを初めて明らかにしている。 以上、本研究で得られた知見はCD8+T細胞の抗原に対する応答性、及び抗原認識と活性化についてを解析したもので免疫学において基礎的な研究として重要な意味を持つことはもちろんのこと、応用上貢献するところが少なくない。よって審査委員一同は、本論文が博士(農学)の学位論文として価値あるものと認めた。 |