麻疹は優秀な弱毒生ワクチンが開発され、先進国での大規模な流行はみられなくなってきたが、後進国を中心に毎年全世界で7,000万人が罹患し、150万人の小児が死亡している、人類の課題とも云える疫病である。又先進国においても3種混含ワクチン(MMR)接種における無菌性髄膜炎の発生等なお問題がある。この麻疹はヒトのCD46をレセプターとして利用し、宿主細胞に感染をおこすため、ヒトに感染するといわれている。しかし従来、CD46をもたないマウスの細胞に感染するという報告があり、本当にマウス細胞に麻疹ウイルスが感染しうるかどうかを調べることを目的として研究を始めた。また自然宿主以外の細胞でウイルスを継代することにより、しばしば弱毒株が得られている。そこでEdmonston株をマウスの細胞に継代することにより変異株を分離することから試みた。 角ビンに75%confluent,monolayerのNIH3T3細胞を用意し、m.o.i.lでEdmonston株を接種し、2時間の吸着後、37℃、5%CO2にて培養を続けた。以後3〜4日毎に継代し、8ヵ月間継続した。この細胞はいわゆるcarrier cultureであり、ウイルス中和能のあるSSPE患者血清を感染NIH3T3細胞に加えて培養するとウイルスを出さなくなり、Veroとのco-cultureでもCPEが見られなくなった。即ちMVpは一部のNIH3T3細胞に感染し、感染細胞から非感染細胞へウイルスが感染して感染状態を継続していると考えられる。このようにCD46がないとされるマウス細胞でも麻疹ウイルスは増殖することがわかった。ウイルス感染には他のレセプターを使っていると考えられる。このEdmonston株感染長期培養NIH3T3細胞は親Edmonston株より小さなプラークを作るウイルスを出していた(直径約1/3)。2回のプラーク純化によりウイルスクローンを得、これをMVpと命名した。このプラークサイズの遺伝的安定性を見るため、Vero細胞に接種し、4代まで継代してそのプラークのサイズを比較したが安定して小さいプラークを作った(写真1)。 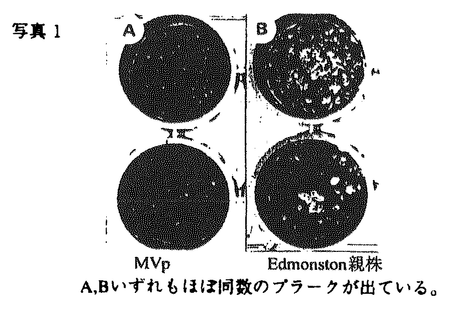 図表 図表 MVpの赤血球凝集能を調べるために、アフリカミドリザルの赤血球をそれぞれのウイルス株が感染したNIH3T3細胞又はVero細胞に加え観察した。MVp感染細胞は親株同様アフリカミドリザル赤血球を吸着し、MVpは親株の血球凝集能を保持していた。 次にVero細胞とNIH3T3細胞におけるMVpと親株の感染性を比較するためにUV-Veroアッセイを行った。UV-Veroアッセイは我々の開発した方法でNIH3T3細胞のように感染してもプラークが出来ない細胞での麻疹ウイルスの感染価を測定する方法である。即ちNIH3T3細胞にウイルス接種した後4日目にUV照射(500ergs/mm2)したあとVero細胞を重層し、1日間培養後ホルマリン固定、クリスタルバイオレット染色してVero細胞が作ったプラークをカウントする。結果親株のNIH3T3細胞での感染価はVero細胞での1%位であったのに、MVpのNIH3T3細胞での感染価はVero細胞での50〜80%であった。 次にMVpが親株と抗原的に異なっているか否かを調べるため、ウサギ抗血清を用いて、中和反応を調べた。MVpも親株と同じ血清濃度で中和されたので抗原性は変わっていないと考えられる。又、マウスにおいて中和抗体を惹起する能力を比較した。MVpで免疫したマウス抗血清は親株を免疫したものより高い力価の中和抗体を誘導する傾向があった。以上より、MVpは親株と抗原性は変わらず、むしろ、より高い免疫原性を持つと考えられた(図1)。  図表 図表 マウスにおける神経病原性を調べた。まずBALB/cマウス新生仔の出生1日目の仔マウスの脳内にMVp及び親株をそれぞれ1×104pfu、5×103pfu接種して10週に亘り、マウスの神経症状の発現、体重変化、死亡率を調べた。MVpを接種したものは経過を通じて全例無症状で体重変化もなく死亡したマウスはみられなかった。これに対して、親株を接種したものは接種後約10日目から神経症状(尾のケイレン、歩行困難、刺激に対する過敏性)を示し始め、体重が減少し、16匹中9匹死亡した。次に宿主であるマウスの種による感受性を調べるため、近交系マウスC3H/He、BALB/c、C57BL/6、ddY、ICRにMVp、親株をそれぞれ1×104pfu、5×103pfu接種した2群を作り、4週間観察した。親株に対する感受性はCH3/Heが最も高く、BALB/c、ddY、C57BL/6、ICRの順に低くなっていた。MVpの接種では死亡したり発症したマウスは皆無であった(表1)。以上、MVpは親株に比較し神経病原性が低いことが分かった。  表1:種々のマウスに対する神経病原性 表1:種々のマウスに対する神経病原性 次に出生1日目の新生仔に一方はMVpを1×104pfu、一方は培養液を10 l脳に接種し、2日目に両者に親株を5×103pfu接種した。1日目に培養液を接種し次の日に親株を接種した新生仔マウスでは70〜100%が死んだが、MVpを接種し次の日に親株を接種したものは0〜30%と死亡数が減った。しかし、1日目に接種するMVpをあらかじめ丁度活性ウイルスがなくなる量のUVを照射したところ(700ergs/mm2)、親株による発症抑制が見られず、発病抑制には生きたウイルスが必要な事が分かった。つまり、単に麻疹ウイルス抗原を脳内に接種したのでは防御効果はない(表2)。 l脳に接種し、2日目に両者に親株を5×103pfu接種した。1日目に培養液を接種し次の日に親株を接種した新生仔マウスでは70〜100%が死んだが、MVpを接種し次の日に親株を接種したものは0〜30%と死亡数が減った。しかし、1日目に接種するMVpをあらかじめ丁度活性ウイルスがなくなる量のUVを照射したところ(700ergs/mm2)、親株による発症抑制が見られず、発病抑制には生きたウイルスが必要な事が分かった。つまり、単に麻疹ウイルス抗原を脳内に接種したのでは防御効果はない(表2)。  表2:変異ウイルスによる親株が惹き起す神経病原性の防御 表2:変異ウイルスによる親株が惹き起す神経病原性の防御 脳内接種後のウイルスの増殖を調べた。新生仔マウスの出生1日目にMVpを1X104pfu接種し次の日に親株を5×103pfu接種した群、出生1日目に1×104pfuMVpのみを接種した群、親株のみを2日目に5×103pfu脳内接種した群につき出生後、日を追ってそれぞれ脳を摘出し、10%の脳ホモジネートを作り、これを1200rpm、5min.遠心して得た上清をVero細胞でウイルス定量した。MVpは接種後一時的に増殖したのみであった。親株は接種後10日にかけウイルス量が上昇した。 一方MVpを接種し、次いで親株を接種した群ではウイルスは6日目までは親株に近い増殖を示したが、その後ウイルス量が下がり、親株のみの接種とは異なった増殖曲線を示した。 一方これ等の標品でインターフェロン活性を調べたが、MVpのみを接種したものではどの時点でも活性が全く認められなかった。一方親株を接種したものはインターフェロン活性が上昇し、7日目でピークを迎えた。1日目にMVp、次の日に親株を接種したものはある程度のインターフェロン活性の上昇を示した。インターフェロン活性は親株ウイルスの増殖が高い場合に高くなる傾向がありインターフェロン活性上昇は親株ウイルスの増殖の結果であると考えられた。即ちインターフェロンはMVpによる親株ウイルスの病原性抑制にはあまり関与していないと思われる。 次に親株のかわりにSSPEの神経病原性をおさえるかどうかを調べた。生後3週のBalb/cマウスの脳内に一方は1日目にMVpを1.2×105pfu/30 l,2日目にSSPE惑染細胞を600pfu/30 l,2日目にSSPE惑染細胞を600pfu/30 l接種し、もう一方は2日目にSSPE感染細胞のみ600pfu/30 l接種し、もう一方は2日目にSSPE感染細胞のみ600pfu/30 l接種した。その結果前者では後者にくらべて死亡するまでに時間がかかり、死亡率も低下した。SSPEの接種量を140pfu/30 l接種した。その結果前者では後者にくらべて死亡するまでに時間がかかり、死亡率も低下した。SSPEの接種量を140pfu/30 lに変えても同様の結果が得られた。 lに変えても同様の結果が得られた。 さらに親株のかわりにEMCVの神経病原性をおさえるかどうかを調べた。Balb/cマウスの脳内に一方には生後1日目にMVpを4×104pfu/10 l接種し、次の日にEMCVを1pfu/10 l接種し、次の日にEMCVを1pfu/10 lまたは0.5pfu/10 lまたは0.5pfu/10 l接種した。もう一方には生後2日目にEMCVのみ1pfu/10 l接種した。もう一方には生後2日目にEMCVのみ1pfu/10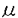 lまたは0.5pfu/10 lまたは0.5pfu/10 l脳内接種した。その結果前者では後者にくらべて死亡するまでに時間がかかり、死亡率も低下した。 l脳内接種した。その結果前者では後者にくらべて死亡するまでに時間がかかり、死亡率も低下した。 以上MVpは(1)プラークサイズが小さいこと、(2)マウス細胞への相対的感染性が上昇していること、(3)新生児マウスへの脳内接種における病原性が低下していること(実際は検出出来ない)(4)親株の抗原性を継続していること、が分かった。又、MVpをあらかじめ脳内接種すると次の日に親株を接種しても親株による神経病原性が抑えられる事が分かった。これ等の事からMVpはマウスでは親株よりもはるかに神経病原性が低いことが分かる。人においても病原性が低ければ、ワクチン候補としてよい株であろう。またMVpを前日脳内接種することにより、EMCVという異種ウイルスの神経病原性をも抑えることから、MVpの脳内接種による、なんらかの非特異的な防御機構が働いていることが考えられる。 |