| [研究の背景と目的] 手術や外傷、熱傷などの外科侵襲後には、腹腔内膿瘍や肺炎などの重症感染症が発生しやすく、これがしばしば多臓器不全の原因となって予後を不良にする。このような外科侵襲後の重症感染症の発生には、侵襲後の生体防御力の低下が密接に関与している。このために、侵襲生体では生体防御力や免疫能を維持、亢進させる対策が必要となる。そのような対策のひとつに栄養管理がある。しかしながら、重症侵襲患者でほぼルーチンに施行されている現行の中心静脈栄養法は、侵襲後の生体防御力増強には不十分であることが明らかにされている。そこで、近年、生体の防御力増強や免疫能賦活をめざす栄養管理の研究がなされている。このような栄養管理法はimmunonutritionとも呼ばれる。その目的で腸管を利用する経腸栄養、さらにグルタミン、アルギニン、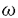 -3脂肪酸などの特殊栄養成分を用いる試みがある。 -3脂肪酸などの特殊栄養成分を用いる試みがある。 とくに侵襲後早期からの経腸栄養に関しては、機械的・免疫学的腸管バリアーの維持、局所および全身の蛋白代謝の改善、侵襲ホルモン分泌の抑制などで、経静脈栄養より優れていることが報告されている。しかし、侵襲生体で経腸栄養が経静脈栄養に比べて生体防御力や免疫能の点で優れている機序については、その詳細はいまだ不明である。とくに、tumor necrosis factor-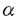 (TNF)やinterleukin-1(IL-1)、IL-8、interferon- (TNF)やinterleukin-1(IL-1)、IL-8、interferon-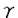 (IFN)など生体防御や免疫で重要な役割を果たすサイトカインの局所や全身における産生・分泌と栄養投与ルートとの関連はほとんど明らかにされていない。さらに外科侵襲が加わる前の栄養投与ルートのこのような生体反応への影響を検討した研究はごくわずかにすぎない。 (IFN)など生体防御や免疫で重要な役割を果たすサイトカインの局所や全身における産生・分泌と栄養投与ルートとの関連はほとんど明らかにされていない。さらに外科侵襲が加わる前の栄養投与ルートのこのような生体反応への影響を検討した研究はごくわずかにすぎない。 一方、臨床においては、腸管を利用した栄養管理の困難な症例に経静脈的高カロリー輸液(TPN)が行われるが、現在市販の静注用アミノ酸製剤には、蛋白代謝改善や免疫賦活で重要な役割をもつグルタミンが含有されていない。グルタミンは、腸吸収細胞に加えてマクロファージやリンパ球など免疫細胞のエネルギー基質であるため、グルタミン添加TPNは侵襲時に優れた免疫能改善効果をもたらすことが期待される。しかし、従来は、グルタミン添加TPNの効果として、外科侵襲時の全身蛋白代謝の維持、あるいは腸や骨格筋などの臓器蛋白代謝の改善に関する研究にもっぱら焦点が当てられ、グルタミン添加TPNの生体防御力や免疫能の改善効果についての詳細な研究はない。 そこで、ラット腹腔内細菌投与モデルを用い、実験1では、侵襲前栄養投与ルートによる腹腔内細菌投与後の局所および全身における炎症細胞やサイトカイン産生・分泌への影響を検討した。ついで、実験2では、侵襲前グルタミン添加TPNの腹腔内細菌投与後の局所および全身への同様の影響をグルタミン非添加TPNと比較した。 [対象と方法] 実験1;ウイスター系雄性ラット(n=68)を経腸栄養群(TEN)、経静脈栄養群(TPN)に分け、TENには胃瘻を、またTPNには頚静脈カテーテルを挿入した。これらを用いて、同一組成、isocaloric(224kcal/kg/日)、isonitrogenous(0.91gN/kg/日)で、完全経静脈栄養または完全経腸栄養を1週間にわたり施行し、その後3×108cfu/mlのE.coli 1mlを腹腔内に投与した。まず細菌投与48時間の生存率を測定した。次にE.coli投与前および投与後2時間、6時間後に犠死せしめ、心腔内採血を施行した後開腹し、腹腔内と気管内を生理食塩水で洗浄、腹腔洗浄液(PLF)中の細菌数(cfu)を測定した。またPLF中、気管内洗浄液(BALF)中、および血中のTNF、IL-1、IFN濃度を測定した。さらに腹腔内滲出細胞(PEC)、気管内洗浄細胞(BALC)をin vitroで培養しTNF、IL-1、IFNの産生を測定した。 実験2;ウイスター系雄性ラット(n=48)を頚静脈カテーテル挿入後に、グルタミンを含有していない標準アミノ酸輸液製剤を用いるSTD-TPN群と、アミノ酸輸液製剤にグルタミンのdipeptideであるアラニルグルタミン(Ala-Gln)を添加したAla-Gln-TPN群の2群に分けた。両輸液剤はisocaloric(199kcal/kg/日)、isonitrogenous(2.2gN/kg/日)とし、経静脈栄養で一週間管理した。Ala-Gln-TPN群はGln1.5%とした。その後、実験1と同様に3×108cfu/mlのE.coliを1ml腹腔内に投与した。投与前および投与2時間、6時間後に犠死させた。PLFおよび肝、脾、血中の細菌数を検討した。PLF中および血中のTNF、IL-8、IFN濃度を測定した。また肝臓組織のTNF濃度、および脾組織のTNF、IFN濃度を測定した。また細菌投与前に脾細胞を採取し、24時間in vitroで培養、培養液中のIFN、TNF濃度を測定した。なお培養液のGln濃度は0、500および1000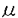 Mとした。 Mとした。 [結果] 実験1;E.coli腹腔内投与48時間後の生存率は、TENラットがTPNラットより有意に良好であった。また、E.coli投与後のPLF中の細菌数は、TPN群がTEN群より有意に多かった。E.coli投与2時間後のTPN群のPEC数は、TEN群に比べ有意に少なかった。TEN群ではPEC数と局所のサイトカイン(TNF、IL-1)濃度に有意な正の相関があったが、TPN群ではこのような有意な相関関係はみられなかった。PLF中のIFN値はTEN群では、細菌投与後0時間から6時間で有意に上昇したが、TPN群では有意な上昇はなかった。E.coli投与前のPECのin vitroでのTNF産生能はTPN群がTEN群より有意に低かった。遠隔臓器である肺での反応では、TEN群のBALC数は、BALF中のTNF値と同様に0時間から2時間にかけて有意に減少した。更にE.coli投与2時間後、TEN群ではPEC数とBALC数、およびPEC数とBALF中TNF濃度の間に負相関があったが、TPN群ではこのような関係はなかった。E.coli腹腔内投与後の全身血中TNF値は、TPN群ではTEN群に比べ高かった。逆に血中IFN値は、TEN群の方がTPN群より有意に高かった。 実験2;PEC数とPLFの細菌数はE.coli投与前、投与後2時間、6時間のいずれにも、両群間に有意差を認めなかった。しかしE.coli投与後6時間でのPLF中のTNF値は、Ala-Gln-TPN群がSTD-TPN群よりも有意に高かった。そしてAla-Gln-TPN群のみでPLF中のTNF値は好中球数と有意に正相関した。またAla-Gln-TPN群での細菌投与2時間後の肝内細菌数は、STD-TPN群より少ない傾向にあった。そして、細菌投与6時間での肝組織TNF濃度、脾IFN濃度はAla-Gln-TPN群がSTD-TPN群よりも有意に高値であった。さらに、細菌投与前のLPS非刺激下でのin vitroにおける脾細胞のIFN産生は、Ala-Gln-TPN群の方がSTD-TPN群に比べて有意に高値であった。Ala-Gln-TPN群の2時間後の末梢血中細菌数は、STD-TPN群に比べて有意に少なく、血中IL-8値も6時間でSTD-TPN群よりも有意に低値であった。また細菌投与後2時間での血中E.coli生菌数は、肝内E.coli数と有意な正の相関があった。 [考察] 実験1では、侵襲前栄養投与ルートによる腹腔内細菌投与後の局所および全身における炎症細胞やサイトカイン産生・分泌への影響を検討した。その結果、TENラットは、TPNラットよりも腹腔内E.coli投与後の生存率が高かった。この理由として、TENラットでは細菌投与初期に腹腔内への滲出PEC数が多くなって、これが腹腔内での細菌のクリアランスを高め、腹腔内細菌数がTPNラットよりも少くなったのが一因と考えられた。一方、TENラットでは気管内洗浄液細胞数が腹腔内細菌投与後初期に有意に減少したのに対し、TPNラットではこの変化が遅延した。これは、TENラットでは遠隔臓器である肺から免疫系細胞が感染局所に迅速に動員される可能性を示唆している。この機序として、TENラットでは腹腔洗浄液中のTNFおよびIL-1濃度が高く、気管内洗浄液中のIFN濃度も高かったことより、腹腔内の高濃度のサイトカインが腹腔内滲出白血球を活性化する一方、肺ではIFNが免疫細胞の肺から腹腔内への動員を促進したと考えられた。さらに、TENラットではLPS刺激による腹腔内滲出細胞のTNF産生が亢進し、さらに全身血中のTNF濃度は低く、逆に血中IFN濃度は高かった。これらの成績から、TENはTPNに比べて腹腔内E.coli投与時の腹腔内での効果的な殺菌を促進し、さらに侵襲時の局所および全身のサイトカイン産生・分泌を適切に制御していることが示唆された。 実験2では、侵襲前グルタミン添加TPNの腹腔内細菌投与後の局所および全身への影響を、実験1と同じモデルを用いてグルタミン非添加TPNと比較した。その結果、侵襲前Ala-Gln添加TPN投与は非添加TPNに比べて、細菌投与後の腹腔洗浄液中のTNF濃度が高かった。つまり、グルタミン添加による局所での好中球などの滲出炎症細胞のTNF産生の促進が示唆される。しかもAla-Gln-TPN群のみでPLF中のTNF値が好中球数と相関しており、グルタミン添加は局所TNF産生による局所への好中球動員を適切に制御していることを推察させる。また、Ala-Gln添加TPN投与によって肝の細菌数は減少し、肝におけるTNF産生が増加した。グルタミンは腹腔マクロファージや肺マクロファージの機能を高めることが報告されているが、これを考慮すると上記の成績はグルタミンが肝のKupffer細胞の貪食能、殺菌能を亢進させ、TNF産生能も促進したためと考えられる。さらにAla-Gln添加TPN投与で脾臓のIFN濃度が上昇し、かつin vitroの実験でグルタミンの脾細胞からのIFN産生促進効果を確認した。さらに、Ala-Gln添加TPN前投与は、STD-TPNに比べ全身血中のE.coli生菌数を少なくした。このグルタミンによる全身血中の細菌数の抑制は、肝と全身血中の生菌数に正の相関がみられたことから、肝における細菌のクリアランスが促進された結果と考えられる。さらにAla-Gln添加TPNは、STD-TPNに比べ血中IL-8濃度が低かった。この全身血中IL-8低値の病態生埋学的意義は明らかではない。いずれにしても、実験2の成績から腹腔内細菌投与モデルでのAla-Gln添加TPN前投与は、STD-TPNよりも効果的に局所、肝、脾、および全身の細菌に対する生体反応やサイトカイン産生をもたらすことが示唆された。 [結語] 腹腔内E.coli投与ラットモデルで、細菌投与前の経腸栄養とグルタミン添加TPNの腹腔局所、肝、脾、肺などの遠隔臓器、全身血における生体防御反応やサイトカイン産生・分泌への影響を、経静脈栄養、グルタミン非添加TPNとそれぞれ比較検討し、 1、侵襲前の栄養投与ルートでは、経腸投与は経静脈投与に比べ、局所、遠隔臓器(肺)そして全身における宿主生体防御力を改善し、かつこれらにおけるサイトカイン産生を適切に制御した。 2、侵襲前のグルタミン添加TPNも、グルタミンを含まないTPNに比べ、局所、遠隔臓器(肝、脾)さらに全身における生体防御力を増強し、さらにこれらの部位でのサイトカイン産生を適切に制御した。 3、これらの成績から、侵襲患者では経腸的な栄養投与が可能な限り、栄養投与ルートとしては経膓投与の方が経静脈投与より望ましい。そして、経腸的栄養投与が不可能な場合には、グルタミン添加TPNの施行が生体防御力の改善に有用である。 |