レチノイドはall-trans-レチノイド酸と9-cis-レチノイン酸に代表され、各々レチノイン酸レセプター(RAR-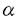 , , , , )および9-cis-レチノイン酸レセプタ-(RXR- )および9-cis-レチノイン酸レセプタ-(RXR-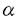 , , , , )を介して特異的な遺伝子の転写を制御する。サブタイプ選択性をもついろいろなRARに対する合成のアゴニストが合成されてきている。梅宮はRARの合成アゴニストAm80から発してRARのアンタゴニストを合成した。その中でもLE540は強いRAR- )を介して特異的な遺伝子の転写を制御する。サブタイプ選択性をもついろいろなRARに対する合成のアゴニストが合成されてきている。梅宮はRARの合成アゴニストAm80から発してRARのアンタゴニストを合成した。その中でもLE540は強いRAR- 選択性をもつアンタゴニストである。 選択性をもつアンタゴニストである。 このアンタゴニスト合成の過程において、梅宮は前骨髄球性白血病細胞株HL60のレチノイドによる顆粒球系細胞への分化を強く増強する化合物HX600を見いだした。この化合物はRAR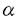 , , , , のタンパクには結合せず、RXR のタンパクには結合せず、RXR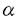 , , , , には弱いながら結合する。しかし、RXR には弱いながら結合する。しかし、RXR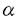 , , , , の細胞内での転写活性化能は十分に強く、HX600はRXR-RARヘテロダイマーのRXRに対するリガンドであると考えられる。 の細胞内での転写活性化能は十分に強く、HX600はRXR-RARヘテロダイマーのRXRに対するリガンドであると考えられる。 梅宮はさらにHX600に関連するRXRアゴニストを多数合成し構造と活性とに関する知見をえた。その過程で、HX600関連誘導体HX531とHX711がRARを活性化しないにも拘ず、HL60の分化を抑制する。これらはリガンド不在下に活性であるRXRミュータントの活性を抑制するのでRXRのアンタゴニストである。 以上梅宮は、十分な強さをもつRARアンタゴニスト、RXR-アゴニストおよびRXR-アンタゴニストを発見した。これらは既にレチノイドの分子生物学研究に十分な寄与をしているが、さらに、RAR依存性疾患やRARやチロキシン、ビタミンDの作用の増強や調節に関与するとみられ、医薬への応用の期待の高いものである。よって、梅宮の研究に医薬化学研究として博士(薬学)の学位にふさわしいと判断する。 |