| 第1章序論 熱ショック蛋白質と呼ばれる、熱等により誘導される一群の蛋白質群は、大腸菌から人に至るまで極めて良く保存されており、ストレスの防御に重要な役割を果たしている可能性がある。その中で、HSC70は正常状態で全細胞内蛋白質の1%をも占め、分子シャペロンとしての蛋白質合成過程への関与が示唆されている。一方、HSP70は、コンセンサスは得られていないが、通常には発現しておらず、各種ストレスによる誘導の可能性が示唆されている。哺乳類中枢神経系のみに限れば、虚血、高体温、中枢興奮薬投与、痙攣、及び組織損傷等の条件下で発現することが報告されている。しかし、誘導イニシエーター、発現意義、ならびに高次細胞機能との関わり等は今もって明らかではない。 脳神経細胞は増殖しない為、ストレスからの防御や損傷からの回復が他の組織よりも必要と思われる。しかもストレス応答は、主に中枢において制御されている。よって中枢におけるHSP70の役割を知ることは非常に意義深いと考えられる。そこで、HSP70のin vivoでの脳内生理的機能を追究することにした。その一環として本論文では、ラットを用いて行なった研究成果について述べる。蛋白質自体の直接適用は不可能な為、まず生理的条件下で中枢神経系に安定してhsp70mRNAを誘導させる系を確立し、その誘導が見られた部位での機能変化を捉えることでHSP70の機能の一端を理解することを試みた。 第2章ラットhsp70mRNAの正常状態並びに高温負荷における発現特性 マウスをはじめ多くの種において、hsp70mRNAはストレス状態下のみで発現するとされる。しかし、HeLa細胞ではその構成的発現も示唆されている。そこでラットの正常状態におけるhsp70mRNAの発現の有無及び高温負荷の影響を、サーカディアンリズムも考慮してin situhybridization(ISH)法を用いて検討した。雄性Wistar系ラット(7週齢)の全脳を明期(14:00)または暗期(2:00)に摘出し、正常脳としてISHに供した。高温負荷は温室(約44℃)に20分間放置して与え、1時間後に全脳を摘出した。正常脳におけるhsp70mRNAの発現が確認された。その発現量は、2:00の方が14:00より若干多く、この差は手綱核、及び松果体で殊に顕著であった。本結果より、以降の動物への処置は明期に限った。高温負荷により、直腸温(TR)は41.3℃〜43.0℃まで上昇し、脳内ではTRR依存的に全脳でhsp70mRNAの発現量増加が認められた。このことから、発現量の多さがストレスの程度を反映する可能性が高い。この誘導は、手綱核、海馬歯状回、視床下部、松果体、脚間核、及び小脳で特に際立っていた。TR=43℃に達した脳においても、神経細胞の脱落は認められなかった。よって、従来考えられた"hsp70mRNAは死に行く細胞で誘導する"という見解は考え難い。しかし、高温負荷は顕著にhsp70mRNAを誘導したものの、血液成分の脳表への浸潤が見られ非生理的であった。よって、本研究の目的にはそわないと判断した。 第3章拘束ストレスによるhsp70mRNAの誘導 高温負荷がhsp70mRNAを顕著に誘導するものの非生理的であった為、他のhsp70mRNA誘導条件を検討することにした。そこで、薬理学的にストレス研究でよく用いられる拘束ストレスを負荷して、そのhsp70mRNA発現への影響を検討した。ラットを24hr絶食させた後、仰臥位に固定した。拘束1時間後に胃および全脳を摘出し、胃は剖検、全脳はISHに供した。胃内容物が皆無の場合、1時間の拘束ストレスにより胃潰瘍が全例で生じた。hsp70mRNA発現量は、個体差が認められたものの、全脳にわたり正常動物より増加していた(図1)。殊に、室傍核、海馬歯状回、手綱核、視索上核、松果体、並びに小脳顆粒細胞層で顕著であった。これらの部位は、生体のストレス反応と密接に結びついている部位でもある。高体温時に観察された脚間核での誘導は弱かった。本研究から、薬理学的にストレス研究で用いられる拘束ストレスでも顕著にhsp70mRNAを誘導することが明らかになった。しかし、その誘導程度が個体間で安定していなかったので、機能追究に使用するには難しいと考えられた。  図1 拘束ストレス(1hr)によるhsp70mRNAの誘導(上段)無処置,(下段)拘束ストレス負荷 図1 拘束ストレス(1hr)によるhsp70mRNAの誘導(上段)無処置,(下段)拘束ストレス負荷 図2 CRF投与によるhsp70mRNAの誘導(i.c.v.1hr後)(上段)vehicle,(下段)CRF10 図2 CRF投与によるhsp70mRNAの誘導(i.c.v.1hr後)(上段)vehicle,(下段)CRF10 g第4章Corticotropin-releasing factor(CRF)によるhsp70mRNAの誘導 g第4章Corticotropin-releasing factor(CRF)によるhsp70mRNAの誘導 拘束ストレスによるhsp70mRNA誘導が不安定であった為、ストレッサーの生体内媒介物質であるCRFを脳室内投与しhsp70mRNA動態を検討した。その際、拘束ストレスによる誘導が神経活動の盛んであると考えられる部位で顕著に見られたので、最初期遺伝子の一つであるzif268mRNAの発現も併せて隣接切片で検討した。CRF(1&10 g)はhsp70mRNAを投与1時間を最大として誘導し、その脳内誘導パターンは、室傍核を除き拘束ストレスと同様であった(図2)。また、この誘導は拘束ストレスよりも安定して検出された。この誘導パターンとzif268mRNAの発現パターンを比較した結果、一致しない部位が存在した。このことは、神経活動のみでそれらの誘導が起こるのではないことを意味する。また、両mRNAの誘導部位の差異の検討より、zif268mRNAの発現が弱い部位であるCRF1受容体存在部位でもhsp70mRNAの誘導が確認され、しかもCRF1受容体が根本的な内分泌系を制御する部位に存在することから、HSP70が生理的ストレスに対する生体防御システムに関与する可能性が強く示唆された。なお、hsp70mRNA誘導が顕著であった部位としては海馬歯状回、視索上核、手綱核、松果体、小脳であった。一方、zif268mRNAは海馬CAl野や室傍核で特に顕著であった。 g)はhsp70mRNAを投与1時間を最大として誘導し、その脳内誘導パターンは、室傍核を除き拘束ストレスと同様であった(図2)。また、この誘導は拘束ストレスよりも安定して検出された。この誘導パターンとzif268mRNAの発現パターンを比較した結果、一致しない部位が存在した。このことは、神経活動のみでそれらの誘導が起こるのではないことを意味する。また、両mRNAの誘導部位の差異の検討より、zif268mRNAの発現が弱い部位であるCRF1受容体存在部位でもhsp70mRNAの誘導が確認され、しかもCRF1受容体が根本的な内分泌系を制御する部位に存在することから、HSP70が生理的ストレスに対する生体防御システムに関与する可能性が強く示唆された。なお、hsp70mRNA誘導が顕著であった部位としては海馬歯状回、視索上核、手綱核、松果体、小脳であった。一方、zif268mRNAは海馬CAl野や室傍核で特に顕著であった。 CRF投与後の自発運動量の変化を検討したところ、溶媒投与群に比して1 gでは増加を、10 gでは増加を、10 gでは減少を認めた(図3)。このことは、運動量亢進に起因する体温上昇でCRFによるhsp70mRNA誘導が起きたのではないことを示唆する。また、CRF投与により、ストレス時の行動と類似した行動を惹起できた。 gでは減少を認めた(図3)。このことは、運動量亢進に起因する体温上昇でCRFによるhsp70mRNA誘導が起きたのではないことを示唆する。また、CRF投与により、ストレス時の行動と類似した行動を惹起できた。 すなわち、CRFという薬理学的ツールを用いたことから安定して拘束ストレスと同様の脳内hsp70mRNA誘導パターンを模倣でき、ストレスとHSP70の関連性が示唆された。しかも、CRF脳室内投与によって非生理的な現象は観察されず、急性ストレス時の行動のみを動物に惹起することが出来た。CRF脳室内投与により、生理的条件下におけるHSP70の機能追究が可能になったといえる。  図3 CRFが累積自発運動量に及ぼす影響 図3 CRFが累積自発運動量に及ぼす影響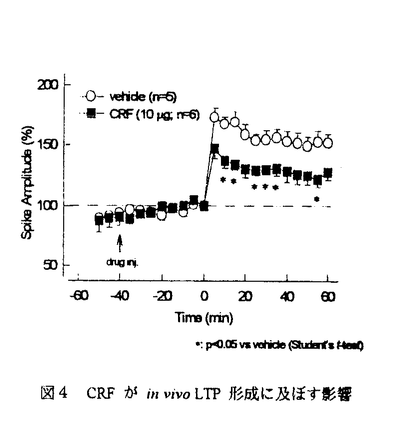 図4 CRFがin vivo LTP形成に及ぼす影響第5章Corticotropin-releasing factorの中枢神経に対する作用-海馬歯状回長期増強現象(LTP)への影響- 図4 CRFがin vivo LTP形成に及ぼす影響第5章Corticotropin-releasing factorの中枢神経に対する作用-海馬歯状回長期増強現象(LTP)への影響- CRFが海馬歯状回でhsp70mRNAを誘導したことから、同部位でのHSP70の機能を探る目的で、CRFが海馬歯状回LTPに及ぼす影響を麻酔下ラットを用いて検討した。嗅内皮質貫通線維テスト刺激に対する海馬歯状回誘発電位はCRF10 gで影響を受けなかった。しかし、投与40分後のテタヌス刺激(60Hz,0.5sec)によるLTP形成は有意に抑制された(図4)。これが、CRFによる急性ストレス再現によるのかは本実験からだけでは解らないが、青斑核等と海馬との関連を考えるとその可能性は高い。本現象とHSP70誘導との関連性の有無は今後の検討課題である。 gで影響を受けなかった。しかし、投与40分後のテタヌス刺激(60Hz,0.5sec)によるLTP形成は有意に抑制された(図4)。これが、CRFによる急性ストレス再現によるのかは本実験からだけでは解らないが、青斑核等と海馬との関連を考えるとその可能性は高い。本現象とHSP70誘導との関連性の有無は今後の検討課題である。 LTP形成促進と記憶・学習改善は関連するとされる。しかし、CRFによる学習改善効果が報告されている一方で、逆に本実験ではLTP形成を抑制した。前章でCRF10 g投与がzif268mRNAを海馬ではCAl野錐体細胞層のみに顕著に誘導した。zif268mRNAはLTP形成で発現すると言われる。このことと、記憶とLTPが関連することを信じるならば、CRFによる空間学習改善は海馬歯状回ではなくCAl野におけるLTP形成による可能性が高い。 g投与がzif268mRNAを海馬ではCAl野錐体細胞層のみに顕著に誘導した。zif268mRNAはLTP形成で発現すると言われる。このことと、記憶とLTPが関連することを信じるならば、CRFによる空間学習改善は海馬歯状回ではなくCAl野におけるLTP形成による可能性が高い。 テタヌス刺激を嗅内皮質に負荷し、1時間後のhsp70mRNA発現量を調べた。歯状回顆粒細胞層における誘発電位の細胞外記録、並びにzif268mRNAの隣接切片での発現によりLTPが形成されたと判断される刺激側海馬歯状回でも、hsp70mRNAは殆ど誘導されなかった。これより、テタヌス刺激、ないしはLTP自身と、hsp70mRNA誘導とはさほど関連が無いといえる。しかし、テタヌス刺激前のCRF投与でLTP形成が抑制されたこと、及びCRFでhsp70mRNAが誘導されたことから、HSP70誘導とLTP形成抑制が関連する可能性が示唆された。 第6章Corticotropin-releasing factorの中枢神経に対する作用-小脳、視床下部培養神経細胞生存への影響 CRFがhsp70mRNAを小脳並びに視床下部で誘導したので、CRFの長期的作用並びにHSP70の細胞保護作用検討の為、両部位の培養神経細胞生存に対するCRFの影響を見た。両細胞群とも、それぞれ1 M及び100nMのCRFにより培養5日後の生存が有意に促進された(図5)。本結果とCRF受容体が両細胞群にあることから、CRFがHSP70の誘導を介して培養神経細胞の生存促進効果を示す可能性が示唆された。 M及び100nMのCRFにより培養5日後の生存が有意に促進された(図5)。本結果とCRF受容体が両細胞群にあることから、CRFがHSP70の誘導を介して培養神経細胞の生存促進効果を示す可能性が示唆された。 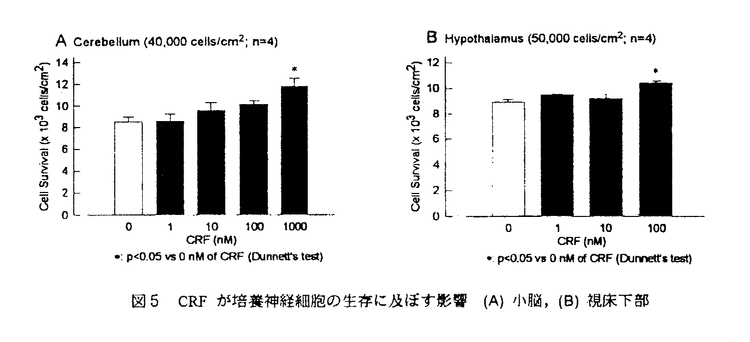 図5 CRFが培養神経細胞の生存に及ぼす影響(A)小脳,(B)視床下部第7章総括 図5 CRFが培養神経細胞の生存に及ぼす影響(A)小脳,(B)視床下部第7章総括 本研究の結果、ラットhsp70mRNAは中枢において構成的に発現していることが判明し、正常状態においてもHSP70は機能していることが推測された。その発現は、熱以外のストレスによっても、ストレスと関係があるとされる特定の脳内部位で誘導されることがわかった。また、CRFの脳室内投与は、拘束ストレスにより誘導されるhsp70mRNA発現パターンを、より安定に再現でき、CRF投与がストレスとHSP70の関係を追究する手段となりうることが理解された。さらにCRFの新しい薬理作用として、海馬歯状回LTPの抑制作用や、培養神経細胞の生存促進作用がわかった。これらの現象を利用したHSP70の機能解明が可能となった。 以上より、生理的条件下におけるHSP70の機能を解明する上で、CRFのラット脳室内投与が非常に有用であることが示唆された。本実験では、最終的な目的であったHSP70の機能を知るには至らなかったが、今後は本実験で関連が示唆された実験系にアンチセンスDNAを用いることにより、その機能が追究できると考えられる。 |