学位論文要旨
| No | 112883 | |
| 著者(漢字) | 野地,匡裕 | |
| 著者(英字) | ||
| 著者(カナ) | ノヂ,マサヒロ | |
| 標題(和) | 酸素を用いた触媒的酸化カップリングによるビナフトール類不斉合成法の開拓 | |
| 標題(洋) | ||
| 報告番号 | 112883 | |
| 報告番号 | 甲12883 | |
| 学位授与日 | 1997.03.28 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(薬学) | |
| 学位記番号 | 博薬第794号 | |
| 研究科 | 薬学系研究科 | |
| 専攻 | ||
| 論文審査委員 | ||
| 内容要旨 | 光学活性ビナフトール系化合物は有効な不斉空間を構築し、不斉合成反応における極めて優れた不斉配位子として広く用いられている。しかし、それらの合成は、化学量論量以上の金属酸化剤を用いた、2-ナフトール類の酸化的カップリングと、それに引き続く光学分割を経て行われてきた。 先に我々は、本カップリング反応における金属酸化剤の使用量を減らすべく、検討を行った。すなわち、我々は、酸素との錯体が数多く知られている銅-アミン錯体に注目し、ナフトールを酸化後、2価から1価に還元された銅を、酸素を用いて2価に再酸化する事が出来れば、触媒的な反応になると予想した。これに従い、各種銅塩、溶媒等を検討の結果、塩化銅(I)と2座配位型アミンのTMEDAから、容易に調製可能な安定な二核錯体、[Cu(OH)TMEDA]2Cl2が、触媒として非常に有効であることを見出した。  更に我々は、配位子であるTMEDAをキラルアミンに置き換えることで不斉カップリングへの展開が可能と考え検討を行った。その結果、スパルテインを配位子として用いると有意な不斉誘起を示すことを見出した。(化学収率18%、不斉収率46%eeにて(S)-2dを与えた)。更に本反応はカップリング時に不斉を誘起していることが判明し、触媒的不斉反応へ展開可能であることが示された。そこで化学収率、不斉収率の改善を目的に本研究を開始した。 化学収率の低さに対しては、生成したビナフトールがスパルテイン-銅錯体と安定な錯体を形成し、触媒の不活性化をしている可能性を考え、検討を行った。 ナフトールのエステル置換基を嵩高くすることで、カップリングにより生成したビナフトールが嵩高くなり、スパルテイン-銅錯体から解離しやすくなると考えた。スパルテインと塩化銅、水から、酸素雰囲気下調製した錯体に、エステル置換基の異なる各種ナフトール誘導体を用い、検討した。 残念ながらエステル置換基の大きさは化学収率に対して影響を与えなかった。また反応時間を延長しても化学収率の向上は見られなかった。しかし、エステル置換基が嵩高くなるに従い、不斉収率の大幅な上昇が見られ、基質として3-ヒドロキシ-2-ナフトエ酸tert-ブチルエステル(1i)を用いると74%eeにて(S)-2iを与えた。  化学収率の向上を目的として、酸素の溶解度の大きい含フッ素溶媒中の反応を検討した。ペルフルオロヘキサン(PFH)のみを溶媒として用いたときは触媒、1iとも溶解せず、反応は進行しなかった。そのため塩化メチレン-ペルフルオロヘキサン=1:3の混合溶媒を用いた(run4)。この場合、両溶媒が混合せず二相系の反応となったが、収率の向上が見られた。このとき触媒と1iはいずれも塩化メチレン層に全て溶解している事が確認され、従って、本反応の化学収率は濃度に大きく依存している事が示唆された。  上に示す様に、本不斉反応の化学収率は基質濃度に高く依存し、640mMの1iの濃度において、不斉収率を低下させることなく、化学収率65%にて2iが得られた(run6)。本反応条件下、72時間反応させると、化学収率78%、75%eeにて(S)-2iが得られる(run8)。これをシクロヘキサンより再結晶する事で99.8%ee以上の(S)-2iを得ることが出来た。1iの濃度が960mM以上の反応においては、化学収率の向上は認められるが、不斉収率の低下が見られた。 市販のスパルテインを触媒の不斉配位子として用いた反応では、上記のようにかなりの不斉誘起を示す。しかしスパルテインの構造変換は困難を伴うので新規なキラル配位子を設計した。本設計においては、銅に対する不斉配位子として縮合した環形を持つ化合物を選択し、銅へ配位したときに配座の固定が起こることを期待した。配座の固定が実現できれば置換基による効果が明確に表れると考えられる。 立体的な要因から銅とアミンは図のように配位すると予想した。 置換イサト酸無水物とプロリン誘導体を1段階で縮合して環状ジアミドとし、これをボランを用いて還元し光学活性ピロロ〔2,1-c〕〔1,4〕ベンゾジアゼピン(PBD)誘導体28を合成した。 このジアミンは、芳香環とプロリン置換基の種類により幅広い構造変換が可能である。特に芳香環側の置換基は立体的な効果のみならず、電子的な効果を期待出来る。窒素の電子密度の制御により、配位している銅の酸化力の制御を試みた。 酸素雰囲気下、それぞれ10mol%のジアミンと塩化銅(I)及び水から錯体を調製し2iのカップリング反応を行った。 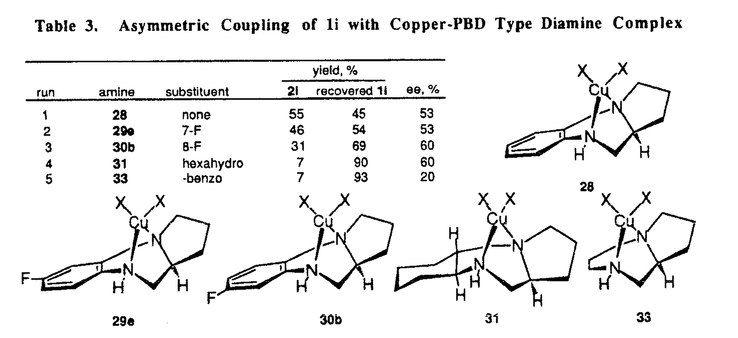 電子求引性置換基の存在は銅の電子密度を下げ銅の酸化力を向上させ、化学収率の向上につながると考えたが、効果は見られなかった(run1-3)。しかしアニリン型の窒素を、より電子供与力の大きいと考えられる脂肪族アミン型の窒素に変えると大幅な化学収率の低下が見られた(run4)。Run5の結果も考慮すると、アニリン型の窒素を1個持つ配位子28の電子供与力は、本反応に対して適切な範囲であり、化学収率に対して有利に働いたと考えられる。 次にプロリン環由来部分を検討した。ヒドロキシプロリンから誘導したアミンや六員環を持つピペコリン酸から誘導したアミンを検討した。これまで同様に酸素雰囲気下、それぞれ10mol%のジアミンと塩化銅(I)及び水から錯体を調製し2iのカップリング反応を行った。2位のpseudoaxial位の水素を除いた形のオキソ体を用いると不斉収率の低下が見られた(run3)。逆にプロリン由来の五員環部分のR1に置換基をつけると大幅な不斉収率の上昇が見られた(run4)。 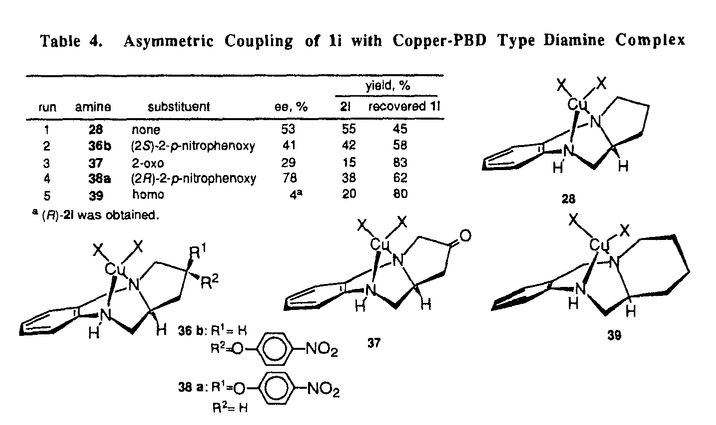 五員環上部の置換基の存在により、不斉収率の大きな変化が見られたことは、推定した配位構造を支持するものと考えられる。不斉誘起には五員環上に大きな立体的障害があれば有利と考えられる。これらの結果から、六員環を持つジアミン39は高い不斉誘起が期待された。しかし全く他のアミンとは違う傾向を示した。これはアミンの平面に対して下側からも銅の配位が可能なためと考えている。 光学活性ジアミンを配位子として用いることにより、触媒的不斉酸化カップリングが可能なことが示された。新規合成ジアミンを用いた不斉酸化カップリングによりスパルテインを超える不斉収率にてビナフトールを得ることが出来た。 不斉収率はナフトールの3位のエステル置換基が大きくなるほど上昇する傾向にある。またアミンの骨格が固定しているほど高い不斉誘起を示す。 ジアミンの構造変換により更に選択性の上昇が可能と思われる。 (1) Noji,M.;Nakajima,M.;Koga,K.1994,35,7983-7984. | |
| 審査要旨 | 光学活性ビナフトール類は、不斉合成反応におけるキラル補助剤の構成要素として広く用いられているが、その合成はラセミ体の光学分割によって行われてきた。本研究は、ナフトール類の触媒的不斉酸化カップリング反応によるこれらの化合物の新規合成法の開拓を行ったものである。 本研究は、下に示すように、極めて効率のよいナフトール類の触媒的酸化カップリング反応を見出したしたことに始まっている。すなわち、塩化銅(I)とTMEDAから容易に調製される安定な二核錯体[Cu(OH)TMEDA]2Cl2(1)を用い、ナフトール類(2)のビナフトール類(3)への酸化カップリング反応を酸素雰囲気下で行うとき、1は触媒量でよいことを見出した。本反応は、2価から1価に還元された銅が、酸素によって2価に再酸化されることにより、1が触媒回転するものである。
この結果は、1に用いている配位子TMEDAをキラルなジアミンに置き換えることによって、本反応を触媒的不斉酸化カップリング反応へと展開できる可能性を示している。事実、TMEDAの代わりに(-)-スパルテインを用いて2(R=CO2Me)の酸化反応を行うと、化学収率は低いものの不斉が誘起され、(S)-3(R=CO2Me)が18%、46%e.e.で得らることを初めて見出した。そこで、本反応を詳細に検討し、反応の化学収率は基質濃度に依存していること、不斉収率は2の置換基(R)により異なることを見出し、2(R=CO2But)を用いて(S)-3(R=CO2But)を78%、75%e.e.で得ることに成功し、再結晶によって99.8%e.e.の純度をもつ(S)-3(R=CO2But)とすることができた。 しかし、(-)-スパルテインを不斉配位子とする上記の反応は、(-)-スパルテインの構造変換には限度があること、対掌体が入手困難であること等の欠点がある。そこで、両対掌体の入手が可能で構造変換もできるジアミン型不斉配位子の検索を行い、ピロロベンゾジアゼピン(4)を基本骨格にもつ定まった構造のジアミン(5)に到達した。5を不斉配位子として2(R=CO2But)の酸化カップリング反応を行うと、(S)-3(R=CO2But)が38%、78%e.e.で得られた。また、この結果に基づいて、立体化学的反応機構の推定をおこなった。
以上本研究は、化学収率(反応速度)および不斉収率に未だ問題を残しているが、触媒的不斉酸化カップリング反応による光学活性ビナフトール類の不斉合成の途を拓いたものとして、有機合成化学に寄与するものであり、博士(薬学)の学位に値するものと認める。 | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/54595 |

