| 内容要旨 | | 硫酸化多糖には血液の凝固作用すなわち抗凝血作用があることがよく知られており、その代表として天然硫酸化糖のヘパリンがある。ヘパリンはヒトを含む動物の体内で抗凝血活性を司る重要な糖鎖ポリマーであり、負電荷を沢山持つ糖シーケンスがタンパク質のアンチトロンビンIIIに結合しそれを活性化することにより、その機能を発揮する。また、カードラン硫酸、リボプラナン硫酸などの硫酸化多糖は新しい生理活性としての抗エイズウイルス活性を示すことが当研究室により報告されている。抗エイズウイルス活性を示す硫酸化多糖の抗エイズウイルス活性発現機構としてはエイズウイルス(HIV)の表層に存在する糖タンパク質であるgp120とカードラン硫酸との静電気的相互作用により、ヒトリンパ球(T-4)への接触阻害であるとが考えられている。このような硫酸化多糖の生体内での生理活性作用は、正電荷を示すリジンあるいはアルギンニンなどの塩基性アミノ酸を持っているタンパク質との相互作用の結果として推定されている。 本論文では、生体内での硫酸化多糖の生理活性作用機構をタンパク質の正電荷部位のモデル化合物としてポリリジン及びリジンコポリマーを用いて、硫酸化多糖の陰イオンとタンパク質の陽イオンとのイオン相互作用という側面でNMR的手法から解明することを目的とした。 本研究では、1)硫酸化多糖の生理活性、2)エイズ治療薬としてのカードラン硫酸、3)抗凝血剤としてのヘパリン、4)細胞外マトリックズ成分としてのコンドロイチン硫酸をそれぞれ硫酸化多糖として用いて、タンパク質とのイオン相互作用について研究した結果を述べる。 1)エイズ治療薬としての硫酸化多糖の作用機構のNMR的研究 HIVのgp120についての詳細な解析によりgp120には6つの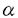 -ヘリックス、 -ヘリックス、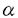 1〜 1〜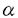 6が存在し、 6が存在し、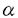 1, 1,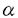 4, 4,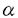 5, 5,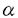 6はC1,C4,C6領域に 6はC1,C4,C6領域に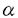 2, 2,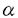 3はV2とプセウドーC2領域に存在していることが報告されている。特に 3はV2とプセウドーC2領域に存在していることが報告されている。特に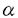 6-ヘリックス部位のアミノ酸配列の506から518番目にかけてNH3+とグアニル基に由来するプラスチャージが連続する部位が存在し、これがポリアニオンである硫酸化糖と相互作用をする位置として推定されている。硫酸化多糖はgp120と結合することで物理的なリンパ球との接触阻害、あるいはgp120のコンホメーションを変化させることにより活性を発現していると考えられている。硫酸化物アニオンを持っているカードラン硫酸(平均分子量79,000,硫酸度1.5)とアンモンニウムカチオンを持っているポリリジン(平均分子量10,700)を種々の割合で混合したところ、そのイオン間の相互作用により高分子コンプレックスを形成することを見出した。高分子コンプレックスは両成分のモル比すなわちイオン比によって水にゲルの状態あるいは可溶性コンプレックスの状態で存在した。Fig.1と2にはカードラン硫酸とポリリジンとのモル比の変化による400MHz 1H-NMRと100MHz 13C-NMRの測定結果を示した。Fig.1の(a)はカードラン硫酸、(b)はポリリジン、(c)〜(f)はカードラン硫酸とポリリジンのモル比が各々0.5、0.8、1.0、2.0で混合した試料の1H-NMRスペクトルである。Fig.2の(a)はポリリジン、(b)〜(e)はカードラン硫酸とポリリジンのモル比が各々0.5、0.8、1.0、2.0で混合した際のそれぞれ試料の13C-NMRスペクトルである。1H及び13C-NMRスペクトルではカードラン硫酸とポリリジン間でのイオン反応の生成物であるゲル状態のコンプレックスの含量に依存し有意に変化した。モル比が0.5の場合は未反応のポリリジンとゲル状態コンプレックスの共存状態、モル比0.8ではイオン比がほぼ1:1.2となり陰イオンと陽イオンとの結合によって生成されたゲル状態のコンプレックスのみが存在していることを示唆している。モル比1.0と2.0の場合は、ゲル状態のコンプレックスとフリー状態のポリリジンあるいは可溶性コンプレックスとの共存状態であることを示唆している。 6-ヘリックス部位のアミノ酸配列の506から518番目にかけてNH3+とグアニル基に由来するプラスチャージが連続する部位が存在し、これがポリアニオンである硫酸化糖と相互作用をする位置として推定されている。硫酸化多糖はgp120と結合することで物理的なリンパ球との接触阻害、あるいはgp120のコンホメーションを変化させることにより活性を発現していると考えられている。硫酸化物アニオンを持っているカードラン硫酸(平均分子量79,000,硫酸度1.5)とアンモンニウムカチオンを持っているポリリジン(平均分子量10,700)を種々の割合で混合したところ、そのイオン間の相互作用により高分子コンプレックスを形成することを見出した。高分子コンプレックスは両成分のモル比すなわちイオン比によって水にゲルの状態あるいは可溶性コンプレックスの状態で存在した。Fig.1と2にはカードラン硫酸とポリリジンとのモル比の変化による400MHz 1H-NMRと100MHz 13C-NMRの測定結果を示した。Fig.1の(a)はカードラン硫酸、(b)はポリリジン、(c)〜(f)はカードラン硫酸とポリリジンのモル比が各々0.5、0.8、1.0、2.0で混合した試料の1H-NMRスペクトルである。Fig.2の(a)はポリリジン、(b)〜(e)はカードラン硫酸とポリリジンのモル比が各々0.5、0.8、1.0、2.0で混合した際のそれぞれ試料の13C-NMRスペクトルである。1H及び13C-NMRスペクトルではカードラン硫酸とポリリジン間でのイオン反応の生成物であるゲル状態のコンプレックスの含量に依存し有意に変化した。モル比が0.5の場合は未反応のポリリジンとゲル状態コンプレックスの共存状態、モル比0.8ではイオン比がほぼ1:1.2となり陰イオンと陽イオンとの結合によって生成されたゲル状態のコンプレックスのみが存在していることを示唆している。モル比1.0と2.0の場合は、ゲル状態のコンプレックスとフリー状態のポリリジンあるいは可溶性コンプレックスとの共存状態であることを示唆している。  Figure 1.400MHz 1H NMR Spectra of curdlan sulfate(CS),poly-L-lysine(PL)and polyion complexes(PIC)between CS and PL at different molar ratios(CS/PL). Figure 1.400MHz 1H NMR Spectra of curdlan sulfate(CS),poly-L-lysine(PL)and polyion complexes(PIC)between CS and PL at different molar ratios(CS/PL). Figure 2.100MHz 13C NMR Spectra of poly-L-lysine(PL)and polyion complexes(PIC)between CS and PL at different molar ratios. Figure 2.100MHz 13C NMR Spectra of poly-L-lysine(PL)and polyion complexes(PIC)between CS and PL at different molar ratios. カードラン硫酸とポリリジンの対イオンであるNa+及びBr-イオンの元素分析結果によるとゲル状態のコンプレックスは透析前にもかかわらずNa+及びBr-イオンは理論値に比べて16%程度しか存在していないことが分かった。更に、透析後にはNa+及びBrイオンが全く検出されなかった。この結果はゲル状態コンレックスがカードラン硫酸のとポリリジンのイオン間の静電気的な相互作用により生成されたことを強く支持している。 高分子コンプレックスの形成は、モル比、濃度、pH、分子量、反応時間、温度等の影響を受けると考えられるのでそれらの条件を様々変化させてNMRを測定し、その結果をFig.3に示した。モル比0.8でゲル状態のコンプレックスの含量は最大になり、低い濃度でもほぼ同量のゲル状態のコンプレックスの形成が認められた。モル比0.67と1.0の場合ではゲル状態のコンプレックスの含量がイオン濃度に依存して増加した。モル比2.0ではゲル状態のコンプレックスは生成されなかった。これはカードラン硫酸の陰イオンの割合が多いために、コンプレックスが破壊されたと考えられる。(Fig.3a)カードラン硫酸の硫酸基は酸性下でも安定なアニオンの状態で存在しFig.3b示したようにモル比1.0の混合溶液でほぼ同量のゲル状態のコンプレックスが酸性から中性範囲で生成した。塩基性のpH範囲ではポリリジンのアンモニウム基の中和によりゲル状態のコンプレックスの生成は減少した。ゲル状態のコンプレックスはテトラマー以上の分子量のリジン化合物とのイオン反応により生成され、分子量が一万程度で最大になった。 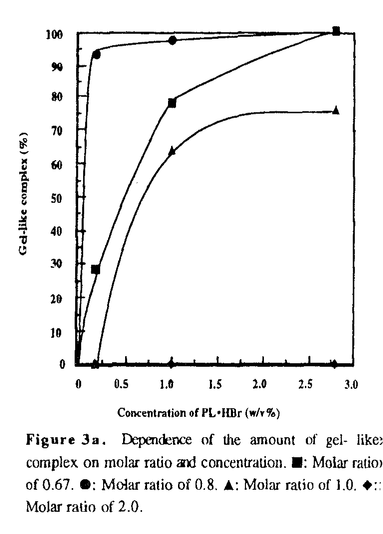 Figure 3a.Dependence of the amount of gel-like complex on molar ratio and concentration.■:Molar ratio of 0.67.●:Molar ratio of 0.8.▲:Molar ratio of 1.0.◆:Molar ratio of 2.0. Figure 3a.Dependence of the amount of gel-like complex on molar ratio and concentration.■:Molar ratio of 0.67.●:Molar ratio of 0.8.▲:Molar ratio of 1.0.◆:Molar ratio of 2.0. Figure 3b.Dependence of the amount of gel-like complex on pH in the molar ratio of 1.02)抗凝血剤としてのヘパリンの作用機構のNMR的研究 Figure 3b.Dependence of the amount of gel-like complex on pH in the molar ratio of 1.02)抗凝血剤としてのヘパリンの作用機構のNMR的研究 ヘパリンはマイクロ濃度で血奨中に存在するアンチトロンビンIII(AT-III)との静電気的な相互作用により,トロンビンを障害することが知られている。AT-III側のヘパリン結合部位はLys-282,Lys-286,Lys-289が考えられている。このようなイオン相互作用のモデル系であるヘパリンとポリリジン混合溶液の場合にもカードラン硫酸系のようにアンモンニウムカチオンを持っているポリリジンとのイオン間の相互作用により、高分子コンプレックスを形成することが分かった。更に1Hと13C-NMRスペクトルでもカードラン硫酸系と同様にイオン反応の生成物であるゲル状態のコンプレックスの含量に依存し大きく変化した。Fig.4には分子量3,000のヘパリンと分子量8,000のポリリジンの混合溶液系で形成されたゲル状態の高分子コンプレックスのモル比、溶液のpHに対する依存性を示した。この溶液系ではモル比0.6でゲル状態の高分子コンプレックスの含量が最大になった。Fig.4に示すように,高分子コンプレックスの含量は反応系のpHに大きく依存した。酸性ではヘパリンのカルボキシル基の酸への変化、塩基性ではポリリジンのアンモンニウムカチオンのアミンへの変化によって高分子コンプレックスの形成が阻害されることが示唆された。ヘパリンとポリリジンの分子量による高分子コンプレックスの含量変化を調べたところ、ゲル状態の高分子コンプレックスは、リジン化合物の分子量が一万程度で最大になった。分子量が各々3,000,6,000と18,000のヘパリンを用いた場合、分子量が低いほど多量のゲル状態のコンプレックスが生成された。分子量6,000と18,000のヘパリンを用いた場合は反応温度及び時間を変化させることによってコンプレックス含量が増加した。(Fig.5)  Figure 4.Dependence of the amount of gel-like complex on pH in the molar ratio of 1.0 Figure 4.Dependence of the amount of gel-like complex on pH in the molar ratio of 1.0 Figure 5.Dependence of the amount of gel-like complex on molecular weight of heparin.Mw of polylysine is 8,000.■:heparin 6,000.口:hcparin 6,000,incubation at 60C for 12hr.●:heparin 18,000.O:heparin 18,000,incubation at 60C for 12hr.3)細胞外マトリックズ成分としてのコンドロイチン硫酸の作用機構の解明 Figure 5.Dependence of the amount of gel-like complex on molecular weight of heparin.Mw of polylysine is 8,000.■:heparin 6,000.口:hcparin 6,000,incubation at 60C for 12hr.●:heparin 18,000.O:heparin 18,000,incubation at 60C for 12hr.3)細胞外マトリックズ成分としてのコンドロイチン硫酸の作用機構の解明 コンドロイチン硫酸は長い鎖中に多数の負電荷イオン基を持ち、その電気的反発力のために延びたコイル状となる。この構造的特性により正に荷電した分子に親和性を示す。このような性質により弾性などの軟骨組織に特有な機能に関与すると同時に塩基性のII型コラーゲンと作用し機械的衝撃に耐える構造体を作ることが知られている。カードラン硫酸やヘパリンに比べて低い陰イオン性で活性を示すコンドロイチン硫酸につき、ポリリジンを用いてイオン間の相互作用を調べた。コンドロイチン硫酸とポリリジンの混合溶液の場合においても、カードラン硫酸系のようにアンモンニウムカチオンを持っているポリリジンとのイオン間の相互作用により高分子コンプレックスを形成することが分かった。コンドロイチン硫酸とポリリジンのモル比に対する高分子コンプレックス生成率をFig.7に示した。イオン比がほぼ1:1になるモル比である0.94〜1の間でゲル状態の高分子コンプレックスの含量が最大になった。カードラン硫酸とヘパリンが各々モル比0.8,0.6で最大の高分子コンプレックスを形成することを考えるとカードラン硫酸などの硫酸化多糖とポリリジンとの相互作用により生成された高分子コンプレックスはイオン比がほぼ1:1になるモル比で最大の疎水性を示していると考えられる。  Figure 6.Dependence of the amount of gel-like complex on molar ratio between chondroitin sulfate(CC) and polylysine(PL).4)まとめ Figure 6.Dependence of the amount of gel-like complex on molar ratio between chondroitin sulfate(CC) and polylysine(PL).4)まとめ 異なる硫酸化度及びカルボキシル化度を有するカードラン硫酸、ヘパリン及びコンドロイチン硫酸とポリリジンの間にイオンコンプレックスが生成することを見出した。イオンコンプレックスの生成は種々の条件によって影響された。中でも、コンプレックスの溶解性は硫酸化多糖の親水性基の含量と密接な関係があった。ゲル状態のコンプレックスの量は陰イオンと陽イオンの比が1に近い場合に低濃度でも一定の量が生成されるが、それの以外の割合ではポリイオンの濃度に大きく依存した。また、ゲル化する割合は反応温度の上昇により増加することが分かった。このような結果から、ゲル状態のコンプレックスは硫酸化多糖とポリリジンの多官能相互作用により生成された架橋コンプレックス或いは一定の親水性/疎水性を示すコンプレックスの集合体であるとして考えられる。 |
| 審査要旨 | | 天然多糖や合成多糖を硫酸化して得られる硫酸化多糖には、種々の生理活性を持つ化合物がある。本論文は、そのような生理活性を持つ硫酸化多糖の活性発現機構を、モデル化合物などを使って分光学的手段で解明しようとするもので、4章から成る。 第1章では、新規な生理活性である抗エイズウイルス活性を持つ硫酸化多糖、古くから知られている生理活性の抗凝血作用を持つ天然硫酸化多糖のヘパリン、および天然のグルコサミノグリカンであるコンドロイチン硫酸などにつき、これまでの研究の概略がまとめられており、本研究の位置付けがされている。 第2章では、エイズ薬として研究開発が進められている硫酸化多糖のカードラン硫酸につき、その抗エイズウイルス活性の発現機構の解明が研究された。カードラン硫酸は溶液中で強く負電荷を帯びており、その負電荷が、エイズウイルスのエンベロープ糖タンパク質の正電荷集中部位とイオン相互作用を行うことにより、抗エイズウイルス活性が発現されると考えられる。タンパク質のモデル化合物としてポリリジンを用いて、カードラン硫酸とエイズウイルスタンパク質の間で想定される相互作用を、高分解能NMR分光学で調べた。ある濃度のポリリジンとカードラン硫酸を混合することにより生成するゲル状物質が、ポリマー間の相互作用に基づく生成物であり、1Hおよび13C NMRで検出可能であることを見出した。1H NMRスペクトルでは、ゲル状物質に含まれるポリリジンの側鎖の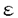 CH2の吸収が、溶液中のフリーのそれより高磁場に現れることを利用して、生成物の定量を行った。カードラン硫酸とポリリジンのそれぞれの構成単位のモル比が0.8の時、ゲル生成割合は100%に達し、それ以上では減少した。ゲルは、中性領域では高い割合で生成するが、pH2以下およびpH10以上では生成量が大幅に減少した。これは測定している現象が、イオン相互作用に基づく高分子相互作用であること、そして本研究で用いたモデル系が、生体内における硫酸化多糖の生理活性の発現機構を調べる適切なモデル系であることを示している。この結果、エイズウイルスの感染阻害剤としてのカードラン硫酸の作用機構が解明された。 CH2の吸収が、溶液中のフリーのそれより高磁場に現れることを利用して、生成物の定量を行った。カードラン硫酸とポリリジンのそれぞれの構成単位のモル比が0.8の時、ゲル生成割合は100%に達し、それ以上では減少した。ゲルは、中性領域では高い割合で生成するが、pH2以下およびpH10以上では生成量が大幅に減少した。これは測定している現象が、イオン相互作用に基づく高分子相互作用であること、そして本研究で用いたモデル系が、生体内における硫酸化多糖の生理活性の発現機構を調べる適切なモデル系であることを示している。この結果、エイズウイルスの感染阻害剤としてのカードラン硫酸の作用機構が解明された。 第3章では、抗凝血活性を有する天然硫酸化多糖のヘパリンの活性発現機構を、第2章で用いたモデルおよび測定系で調べている。ヘパリンは、抗凝血タンパク質のアンチトロンビン-IIIのリジン集中部位へ接着することによって、抗凝血作用を引起すことが知られている。本研究では、タンパク質のモデルとしてポリリジンを使って、ヘパリンとポリリジンの相互作用を1Hおよび13C NMRで検出した。分子量3000のヘパリンと8000のポリリジンのモル比が0.6の時、相互作用によって生じたゲル状物質は最大の割合である93%に達した。高分子間相互作用によるゲル生成は、四量体以上の分子量のポリリジンでなければ起らなかった。また、ヘパリンに含まれるカルボキシル基の低い解離度のため、酸性領域では、ゲル形成すなわち分子間相互作用は大幅に抑えられた。解離度の高い塩の添加によっても相互作用は抑えられた。その結果、通常は検出しにくい多糖とタンパク質の生体系における相互作用が、化学的に解明された。 第4章では、コンドロイチン硫酸などの硫酸化グリコサミノグリカンが持つ生理活性の発現機構を、NMR分光学や円偏向二色性スペクトルによって調べた結果が記述されている。タンパク質のモデル化合物としてポリリジンおよびリジンコポリマーが使われている。コンドロイチン硫酸をポリリジンなどと混合すると、ゲル状コンプレックスが生成し、NMRで検出された。このゲル生成はpH、モル比、ポリリジンの分子量、およびリジンコポリマーの疎水性度によって大きく影響された。解離度の高い硫酸基の他にそれの低いカルボキシル基を含むコンドロイチン硫酸は、ポリカチオンであるポリリジンとの相互作用がやや弱いことが分かった。 以上のように、本研究は、主としてNMR分光学を使って、多糖とタンパク質の間で起る生理活性発現の機構を検出する新しい化学的手段を見出した。更に、硫酸化多糖の発揮する抗エイズウイルス活性、抗凝血活性、および機能性タンパク質との相互作用の発現機構を解明した。本論文の成果は、高分子化学、有機工業化学、および生命化学への貢献が極めて大きい。 よって本論文は博士(工学)の学位請求論文として合格と認められる。 |