学位論文要旨
| No | 113264 | |
| 著者(漢字) | 森,聖治 | |
| 著者(英字) | ||
| 著者(カナ) | モリ,セイジ | |
| 標題(和) | 有機銅-リチウム会合体の反応に関する理論的研究 | |
| 標題(洋) | Theoretical Studies on the Reactions of Organocopper-Lithium Aggregates | |
| 報告番号 | 113264 | |
| 報告番号 | 甲13264 | |
| 学位授与日 | 1998.03.30 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(理学) | |
| 学位記番号 | 博理第3410号 | |
| 研究科 | 理学系研究科 | |
| 専攻 | 化学専攻 | |
| 論文審査委員 | ||
| 内容要旨 | 有機遷移金属化合物の中で有機銅化合物は有機化学的に最も重要な化合物であり,他の有機金属化合物にはない特徴的な反応性を示すことが広く知られている.中でも有機銅アート錯体を用いた炭素-炭素結合生成反応は,触媒反応や化学量論反応として幅広く用いられているが,その反応機構についてはいまだに不明な点が多い.本論文では,有機銅化合物の反応のうちで典型的な反応として知られているアセチレンへの付加反応, 第1章では本研究以前の反応機構の理解の現状および本研究の目的を述べた.R2CuLiの組成を持つGilman試薬は有機リチウム銅(I)アート錯体の典型例であり有機化学上最も重要な有機銅会合体であるが,反応機構の理解は余り進んでいない.有機リチウム銅(I)アート錯体研究の問題点の一つは銅やリチウム金属原子が反応にかかわった複雑な挙動である.その会合状態は溶媒によって大きく異なることが知られている.ジエチルエーテル中では,下図1のAに示すような8員環構造を有した2量体が存在することが知られており,結晶中でもその存在が確認されている.一方,THF中では,分子量測定及び理論計算によりR2CuLi・LiXのハロゲンXで架橋した3核の6員環構造(下図1のB)であると結論付けられている.しかし,これらの錯体がそのままの形で溶液相での反応に関与しているのかどうかは全く不明である. 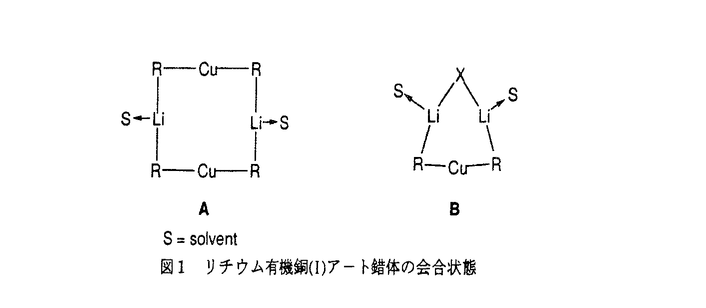 第2章ではアセチレンへの付加反応について述べるとともに,本研究で用いた有機銅反応の理論的解析の信頼性についても述べた.アセチレンへのシス選択的付加反応はビニル銅試薬の合成法として重要かつ基本的な反応であるが,その反応機構についての研究はこれまでほとんど行われていない. (Me2CuLi)2,Me2CuLi・LiClなどいくつかの会合状態をモデルとしてアセチレンとの反応経路をab initio MP2法及びB3LYP密度汎関数法を用いて求めた.その結果,反応が図2に示す反応経路で進行することを明らかにした.すなわち,第一段階では有機銅-リチウム会合体の銅原子がアセチレンと  ここで重要なのは,銅とリチウムの同時相互作用が有機銅アート試薬の示す高い活性に重要な役割を果たしていることである.会合体構造の重要性はモデル計算との比較で明らかにすることができた.すなわちMe2CuLi・LiCl,(Me2CuLi)2の付加の活性化エネルギーはそれぞれ13.6,16.1kcal/molであるのに対し,リチウム原子のもたないMe2Cu-の付加反応の計算では活性化エネルギーが20.3kcal/molとかなり高い.また,このような計算結果と並び,Li+イオンを捕捉するためクラウンエーテルを過剰量加えると反応速度が著しく低下するという実験結果もリチウムカチオンの重要性を支持する. 第2章後半(2-2節)では,有機銅化合物の反応の計算レベル依存性,信頼性について述べた.まず,有機銅反応の検討には,電子相関効果が必須であることを明らかにした.すなわち電子相関を考慮したMP2法とB3LYP法で求まった種々の構造はよい一致を示す.一方,MeCu,Me2Cu-,Me2CuLi・LiClのアセチレンへの付加反応をモデルとして検討した結果,エネルギーの議論にはMP2法に比べてB3LYP法の方が適していることを明らかにした.基底関数の効果および銅原子についての相対論の効果は大きくないこともわかった. 第3章では,有機銅反応の中で有機化学上最も重要であるところの 第3-1節では,錯体(Me2CuLi)2,Me2CuLi単量体などいくつかの会合体のアクロレインに対する共役付加反応についてB3LYP密度汎関数法を用いて検討したことについて述べた.有機銅試薬の銅の3dxz電子がアクロレインに逆電子供与する過程を含む反応のエネルギー状態(図3)を求めた.銅(III)の状態から銅(I)の状態への還元的脱離だけでなく, 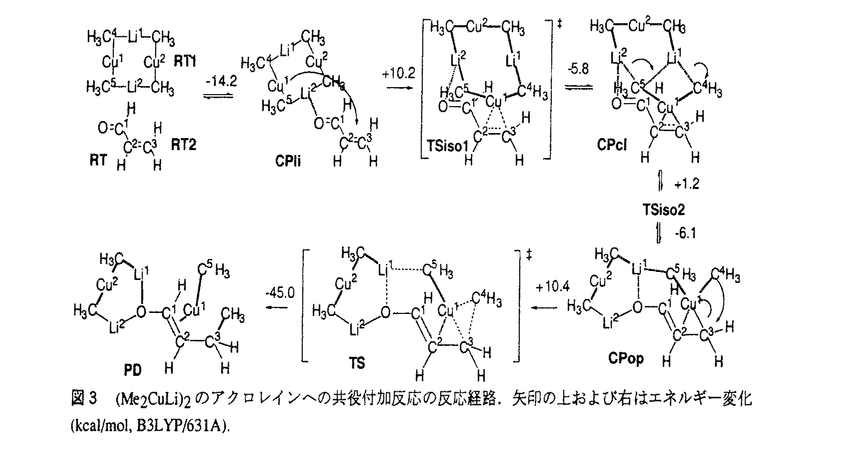 さらに,炭素-炭素結合生成の遷移状態について,2つのリチウム原子がそれぞれ溶媒和された反応系も検討した.その結果,このような溶媒和の効果は反応遷移状態の構造とエネルギーに大きな影響を与えないことがわかった(図4). 3-2節では,2-シクロヘキセノンへの共役付加反応の検討について述べた.反応経路は,アクロレインの場合と同様にまず,Me2CuLi2量体が閉じて配位した中間体と,ついで開環した錯体という2種類のリチウム-酸素/銅-オレフィン錯体を含んでおり,開環した錯体の還元的脱離によって炭素-炭素結合が生成する.エネルギーダイアグラムからこの共役付加反応では,還元的脱離が律速段階であることを明らかにした.この結果は,速度同位体効果の理論計算値と,ごく最近報告された実験値がよく一致することで確認した.さらにシクロヘキセノンとの反応では,シクロヘキサン環の立体配座に関して2種類の反応経路が存在し,いわゆる「アキシアル攻撃」の反応経路(還元的脱離の遷移状態においてシクロヘキサン環がイス型)が有利である理由を初めて明らかにした. 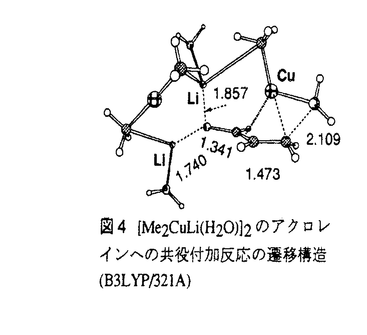 第4章では,ハロゲン化アルキルへの求核置換反応の検討について述べた. 主に存在する炭素求核剤の中で,有機銅アート試薬は,C-X結合への求核置換反応を起こす試薬として最も重要である.臭化アルキルおよびエポキシドとの反応は立体反転をともなって進行することが知られている.求核攻撃の本体は何か,会合体の役割は何かに関する情報はほとんどない.本研究ではMe2CuLi・LiClの臭化メチルへの置換反応を検討し、ともに求核攻撃の本体がCH3-Cuの  第5章では以上検討した有機銅反応を総括し結論を述べた. この章では,分子軌道および溶媒効果の観点から有機銅会合体の反応性の総括を行った.本論文の結論として以下に述べるようなことを導いた.本論文に述べた有機銅会合体のアセチレンへの付加反応, | |
| 審査要旨 | 有機化学的に重要な有機銅アート錯体を用いた炭素-炭素結合生成反応は,触媒反応や化学量論反応として幅広く用いられているが,その反応機構についてはいまだに不明な点が多い.本論文では,有機銅化合物の反応のうちで典型的な反応として知られているアセチレンへの付加反応, 第1章では本研究以前の反応機構の理解の現状および本研究の目的を述べている.R2CuLiの組成を持つGilman試薬は有機リチウム銅(I)アート錯体の典型例であり有機化学上最も重要な有機銅会合体であるが,反応機構の理解は余り進んでいない.有機リチウム銅(I)アート錯体の会合状態は溶媒によって大きく異なることが知られている.しかし,有機銅錯体の反応機構を構造に基づいて議論した例はほとんどない. 第2章ではアセチレンへの付加反応について述べるとともに,本研究で用いた有機銅反応の理論的解析の信頼性についても述べている.アセチレンへのシス選択的付加反応はビニル銅試薬の合成法として重要かつ基本的な反応であるが,その反応機構についての研究はこれまでほとんど行われていない.(Me2CuLi)2,Me2CuLi・LiClなどいくつかの会合状態をモデルとしてアセチレンとの反応経路をab initio MP2法及びB3LYP密度汎関数法を用いて求めた.第一段階では有機銅-リチウム会合体の銅原子がアセチレンと ここで重要なのは,銅とリチウムの同時相互作用が有機銅アート試薬の示す高い活性に重要な役割を果たしていることである.リチウム原子のもたないMe2Cu-の付加反応の計算では活性化エネルギーが20.3kcal/molとかなり高い. 第2章後半(2-2節)では,有機銅化合物の反応の計算レベル依存性,信頼性について述べた.有機銅の反応の検討に電子相関が重要であることがはじめてわかった. 第3章では,有機銅反応の中で有機化学上最も重要であるところの 第3-1節では,錯体(Me2CuLi)2,Me2CuLi単量体などいくつかの会合体のアクロレインに対する共役付加反応,3-2節では2-シクロヘキセノンへの共役付加反応についてB3LYP密度汎関数法を用いて検討したことについて述べている.有機銅試薬の銅の3dxz電子が 第4章では,ハロゲン化アルキルへの求核置換反応の検討について述べている. 主に存在する炭素求核剤の中で,有機銅アート試薬は,C-X結合への求核置換反応を起こす試薬として最も重要である.求核攻撃の本体は何か,会合体の役割は何かに関する情報はほとんどない.本研究ではMe2CuLi・LiClの臭化メチルへの置換反応を検討し,求核攻撃の本体がCH3-Cuの 第5章では以上検討した有機銅反応を総括し結論を述べた. 本論文の結論として以下に述べるようなことを導いた.本論文に述べた有機銅会合体の反応はいずれも,リチウムと銅原子が同時に関与した中間体あるいは遷移状態を経て反応が進行することを明かにした.いずれの反応においても銅の3d軌道が関与し,有機銅会合体のR-Cu-R部分の立体構造によって相互作用の形式が異なる.前二者の付加反応では3dxz軌道が関与するのに対し,後者の置換反応では3dz2軌道が関与することも明らかにした.今回理論的に明らかになった反応経路はこれまでの実験データを合理的に説明するばかりでなく,会合体の役割を初めて明らかにした. 以上の業績は有機化学の分野に貢献すること大である.なお本研究は数名による共同研究であるが論文提出者が主体となって研究開発を行ったものであり,論文提出者の寄与は十分であると判断する.したがって、博士(理学)を授与できると認める. | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/54620 |
 ,
, -不飽和カルボニル化合物への共役付加反応,ハロゲン化アルキルへの求核置換反応の機構について理論的手法を用いた検討を加え,有機銅試薬の会合状態と反応性との関係を明らかにした結果を述べた.五章よりなる本論文の各章の内容を以下に要約する.
-不飽和カルボニル化合物への共役付加反応,ハロゲン化アルキルへの求核置換反応の機構について理論的手法を用いた検討を加え,有機銅試薬の会合状態と反応性との関係を明らかにした結果を述べた.五章よりなる本論文の各章の内容を以下に要約する. 錯体CPを形成し,銅の3dxz電子がアセチレンの空の
錯体CPを形成し,銅の3dxz電子がアセチレンの空の 結合電子(CH3のspn軌道とCuの4s/3dz2軌道からなる)であり,求核攻撃の段階が律速段階であることを明らかにした.この反応においても,Me2CuLi・LiClの6員環が開環した遷移状態TSが重要であることを示した.銅への溶媒和の効果は律速段階の求核反応の遷移状態に至るまでは小さい.溶媒和の効果はCH3-Cu結合の置換の遷移状態TS・SCuのあとで大きく現れ,Cu(III)中間体INT・SCu還元的脱離の遷移状態TS2・SCuを経て反応が進行することが明らかとなった(図5).
結合電子(CH3のspn軌道とCuの4s/3dz2軌道からなる)であり,求核攻撃の段階が律速段階であることを明らかにした.この反応においても,Me2CuLi・LiClの6員環が開環した遷移状態TSが重要であることを示した.銅への溶媒和の効果は律速段階の求核反応の遷移状態に至るまでは小さい.溶媒和の効果はCH3-Cu結合の置換の遷移状態TS・SCuのあとで大きく現れ,Cu(III)中間体INT・SCu還元的脱離の遷移状態TS2・SCuを経て反応が進行することが明らかとなった(図5).