| 内容要旨 | | 1.緒言 低原子価化合物の最大の特徴は,還元力を有することであり,活性な結合あるいは不飽和結合と反応し,合成上有用な反応活性種を生成しうる点にある。多数の低原子価化合物が有機合成反応に用いられてきたが,従来有機合成反応に利用されることのなかった低原子価化合物も存在し,その反応性に興味が持たれている。また,既存の低原子価化合物であっても,反応条件により,劇的に反応性が変化する場合もありうる。そこで,本研究では有機合成化学の立場から低原子価化合物が有する還元力を有効に活用して反応活性種を発生させることを基本的な考え方とし,これらの反応活性種を用いた有機合成反応の開発を目的とした。その結果,いくつかの低原子価化合物が,興味深い反応性を示すことを明らかにした。 2.ヨウ化ゲルマニウム(II)を用いるカルボニル化合物のBarbier型アリル化反応 ケイ素及びスズ化合物は幅広く有機合成反応に用いられているが,同族のゲルマニウム化合物を用いた報告例は少数である。また,そこで用いられているゲルマニウム化合物は大部分が4価の化合物である。一方,低原子価種としてゲルマニウム(II)化合物が知られており,その反応性に興味が持たれているが,これらを用いる有機合成反応,特に炭素-炭素結合生成反応はほとんど報告されていない。そこで,ゲルマニウム(II)化合物が有する還元力を利用した有機合成反応の開発を行なった。 カルボニル化合物のアリル化反応は,重要な炭素-炭素結合生成反応の一つである。そこで,カルボニル化合物存在下,ヨウ化ゲルマニウム(II)とハロゲン化アリルからアリルゲルマニウム(IV)を調製し,カルボニル化合物のBarbier型アリル化反応を検討した。 まず,ベンズアルデヒドとヨウ化アリルの混合物に,ヨウ化ゲルマニウム(II)を作用させたところ,対応するホモアリルアルコールが86%の収率で得られた。一方,同一の条件下で臭化アリルを用いた場合には,反応が極めて遅く,低収率でしか付加体を得ることができなかった(29%)。そこで,臭化アリルをヨウ化アリルに変換することを考え,種々の金属ヨウ化物塩の添加を検討したところ,ヨウ化亜鉛を添加した場合に反応が速やかに進行することがわかった(式1)。そこで,ヨウ化亜鉛添加の条件下,種々のカルボニル化合物のアリル化反応を行なったところ,いずれの場合も良好な収率で対応する付加体を得ることができた(式2)。  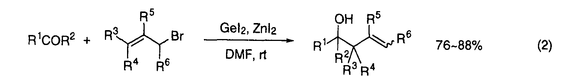 次に,位置及び立体選択性が問題となるクロチル化反応を行なった。その結果,臭化クロチルのE/Z比と付加体のアンチ/シン比に高い相関が認められた(式3)。従って,本クロチル化反応は,ハロゲン化クロチルの二重結合の立体化学の情報を大部分保持したままクロチルゲルマニウム(IV)が生成した後,これがベンズアルデヒドと6員環椅子型の遷移状態を形成して,進行しているものと考えられる。  また臭化プロパルギルを用いた場合には,ホモプロパルギルアルコールが高選択的に生成することがわかった(式4)。同様の反応を低原子価スズ化合物で行った場合にはこのような高選択性は発現しないこととは対照的である。  3.活性化金属ゲルマニウムを用いる不斉Reformatsky反応 ヨウ化ゲルマニウム(II)を用いるアリル化反応におけるハロゲン化アリルを -ハロカルボニル化合物に代えれば,Reformatsky反応となる。そこで,臭化アリルの代りに2-ブロモプロピオフェノンを用い, -ハロカルボニル化合物に代えれば,Reformatsky反応となる。そこで,臭化アリルの代りに2-ブロモプロピオフェノンを用い,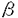 -ヒドロキシケトンの合成を試みた。しかしながら, -ヒドロキシケトンの合成を試みた。しかしながら,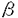 -ヒドロキシケトンは低収率でしか得られなかった(式5)。 -ヒドロキシケトンは低収率でしか得られなかった(式5)。  一方,ゲルマニウム(II)化合物と同様,金属ゲルマニウムも還元力を有する。そこで,無機ゲルマニウム塩を還元して得た活性化金属ゲルマニウムを,本反応に適用することを考えた。ヨウ化ゲルマニウム(II)を金属カリウムで還元して得た活性化金属ゲルマニウムに2-ブロモプロピオフェノンとベンズアルデヒドを作用させたところ,反応はシン選択的に進行し,高収率で付加体が得られた(式5)。さらに, -ブロモイミドを用いた場合にも高収率で付加体が得られた(式6)。 -ブロモイミドを用いた場合にも高収率で付加体が得られた(式6)。  このように,オキサゾリジノン誘導体が良好なReformatsky供与体となることが明らかになったことから,次に,キラルオキサゾリジノンを用いる不斉Reformatsky反応の開発を行った。まず,4種のキラルオキサゾリジノンを合成し,不斉誘起能を検討したところ,いずれの場合でも付加体が高収率かつ高選択性で得れることがわかった(式7,表1,entries 1-4)。その中では,(1S,2R)-2-アミノ-1,2-ジフェニルエタノールから誘導したオキサゾリジノンが有効であったことから(entry 4),次に,このオキサゾリジノンと種々のアルデヒドとの反応を行った(entries 4-7)。その結果,芳香族及び脂肪族アルデヒドとの反応が円滑に進行し,高立体選択性で対応する付加体を得ることができた。すなわち,金属亜鉛を用いた従来の不斉Reformatsky反応と比較し,格段に選択性を向上させることに成功した。   Table14.トリフェニルホスフィン/塩化ゲルマニウム(IV)系を用いる Table14.トリフェニルホスフィン/塩化ゲルマニウム(IV)系を用いる -ブロモカルボン酸誘導体の還元反応 -ブロモカルボン酸誘導体の還元反応 トリフェニルホスフィンが -ハロケトンの還元に有効であることは知られているが,その還元力はそれほど強くないことから, -ハロケトンの還元に有効であることは知られているが,その還元力はそれほど強くないことから, -ハロカルボン酸誘導体の還元反応に適用する際には,厳しい条件下で反応を行わせる必要があった。そこで,トリフェニルホスフィンの弱い還元能を補うために,ルイス酸により -ハロカルボン酸誘導体の還元反応に適用する際には,厳しい条件下で反応を行わせる必要があった。そこで,トリフェニルホスフィンの弱い還元能を補うために,ルイス酸により -ハロカルボン酸誘導体の炭素-ハロゲン結合を活性化すれば,還元反応が速やかに進行するものと考えた。 -ハロカルボン酸誘導体の炭素-ハロゲン結合を活性化すれば,還元反応が速やかに進行するものと考えた。  -ブロモアミドの還元反応においてルイス酸を検討したところ,塩化ゲルマニウム(IV)を用いた場合に好結果が得られ,さらに,塩化ゲルマニウム(IV)を触媒量とした場合でも反応が円滑に進行することがわかった(式8)。 -ブロモアミドの還元反応においてルイス酸を検討したところ,塩化ゲルマニウム(IV)を用いた場合に好結果が得られ,さらに,塩化ゲルマニウム(IV)を触媒量とした場合でも反応が円滑に進行することがわかった(式8)。  次にこの反応条件下,種々の -ブロモカルボン酸誘導体の還元反応を試みた。その結果,トリフェニルホスフィン/塩化ゲルマニウム(IV)系が広範な -ブロモカルボン酸誘導体の還元反応を試みた。その結果,トリフェニルホスフィン/塩化ゲルマニウム(IV)系が広範な -ブロモカルボン酸誘導体の還元反応に有効であることがわかった(式9)。また,本系を -ブロモカルボン酸誘導体の還元反応に有効であることがわかった(式9)。また,本系を , , -ジブロモ- -ジブロモ-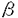 -ラクタムの還元反応に適用したところ,半還元反応が進行し,高ジアステレオ選択的にcis- -ラクタムの還元反応に適用したところ,半還元反応が進行し,高ジアステレオ選択的にcis- -ブロモ- -ブロモ-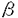 -ラクタムを得ることができた(式10)。 -ラクタムを得ることができた(式10)。  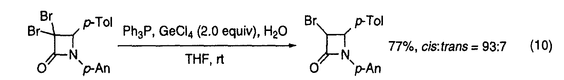 本還元反応の特徴は,厳密な無水条件を必要とせず,温和な条件で反応が進行し,さらに,広範な -ブロモカルボン酸誘導体に対し有効な点にある。 -ブロモカルボン酸誘導体に対し有効な点にある。 5.1,7-エンインの環化異性化反応による8員環化合物の合成 アルケン,アルキン等の不飽和結合の関与する反応は,遷移金属錯体の得意とするものである。これらの反応では,低原子価状態にある中心金属の還元力により金属に配位した不飽和分子が還元され,金属-炭素結合を持つ中間体が生成する場合が多い。また,適切な反応条件の下では,遷移金属錯体を用いた反応を触媒的に行わせることが可能である等の特徴を持つ。そこで,低原子価遷移金属化合物に注目し,これらの還元力を利用した反応の開発を行った。 Pauson-Khand反応はアルキンージコバルトヘキサカルボニル錯体とアルケンからシクロペンテノン誘導体を合成する反応であり,熱的に,あるいは第3級アミンオキシドの作用により進行することが知られている。3位にケイ素を含む1,7-エンインとジコバルトオクタカルボニルから調製したアルキン-コバルトカルボニル錯体にN-メチルモルホリン N-オキシドを作用させたところ,シクロペンテノン誘導体は生成せず,8員環ジエニルシラン誘導体が得られた(スキーム1)。すなわち,1位の炭素-水素結合に対するアルキンの位置選択的挿入が起こり,環化異性化反応が進行することがわかった。一般に,1,7-エンインの環化異性化反応では2位と7位で結合が生成するのに対し,本反応では1位と8位で結合が生成していることから極めて興味深い環化モードであると考えられる。  Scheme1 Scheme1 本反応は,次のように進行しているものと考えている(スキーム2)。まず,エンインとCo2(CO)8が反応し,アルキン-コバルト錯体が生成する。続いてCo-C(8)結合に対するアルケンの挿入が,コバルトがケイ素の 位を占めるように起こり,メタラサイクルが生成する(path a)。挿入過程における位置選択性は,ケイ素による 位を占めるように起こり,メタラサイクルが生成する(path a)。挿入過程における位置選択性は,ケイ素による 位カルボアニオンの安定化により決定されているものと考えられる。引き続き,このメタラサイクルから 位カルボアニオンの安定化により決定されているものと考えられる。引き続き,このメタラサイクルから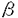 -水素脱離,還元的脱離,コバルト部分の脱離が起こり8員環ジエニルシランが生成する。もう一方の挿入過程(path b)では,このようなケイ素の効果が期待できないため,メタラサイクルの生成は不利となる。 -水素脱離,還元的脱離,コバルト部分の脱離が起こり8員環ジエニルシランが生成する。もう一方の挿入過程(path b)では,このようなケイ素の効果が期待できないため,メタラサイクルの生成は不利となる。  Scheme2 Scheme2 |
| 審査要旨 | | 本論文は,低原子価化合物の還元力を利用した有機合成反応に関する研究の成果について述べたものであり,6章より構成されている。 第1章は序論であり,有機合成化学における金属試薬の重要性,有機金属試薬の発生法について述べるとともに,低原子価化合物の還元力を利用して反応活性種を発生させる手法の重要性を論じ,本研究の目的と意義を述べている。 第2章では,ヨウ化ゲルマニウム(II)を用いたカルボニル化合物のBarbier型アリル化反応について述べている。すなわち,ヨウ化ゲルマニウム(II)とヨウ化アリルから調製したアリルゲルマニウム(IV)が,カルボニル化合物のアリル化反応に有効であることを明らかにしている。また,ヨウ化アリルの代わりにより入手容易な臭化アリルを用いた場合には,ヨウ化亜鉛を添加することでアリル化反応が速やかに進行することを見出している。さらに,臭化クロチルを基質として用いた場合には反応が立体及び位置特異的に進行すること,臭化プロパルギルを基質として用いた場合には高選択的にホモプロパルギルアルコールが得られることなどを明らかにし,本反応の有用性を示している。 第3章では,活性化金属ゲルマニウムを用いてReformatsky反応を行った結果について述べている。まず,活性化金属ゲルマニウムの調製法について検討し,ヨウ化ゲルマニウム(II)と金属カリウムから調製する手法を確立している。次に,この活性化金属ゲルマニウムを用いてReformatsky反応を行ない,最適条件下では -ブロモケトン及び -ブロモケトン及び -ブロモイミドが良好なReformatsky供与体となることを明らかにし,高いシン選択性で対応する -ブロモイミドが良好なReformatsky供与体となることを明らかにし,高いシン選択性で対応する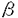 -ヒドロキシカルボニル化合物が得られることを見出している。 -ヒドロキシカルボニル化合物が得られることを見出している。 さらに,本反応をキラルオキサゾリジノンを不斉助剤として用いた不斉Reformatsky反応に拡張している。すなわち, -ブロモプロピオン酸にエリトロ-2-アミノ-1,2-ジフェニルエタノールから誘導したキラルオキサゾリジノンを導入し,これと活性化金属ゲルマニウムとの反応によって調製したエノラートに種々のアルデヒドを反応させ,いずれの場合にも対応する生成物を極めて高ジアステレオ選択的に得ることに成功している。さらに,脱不斉助剤も容易であることを明らかにし,本反応によって高光学純度の -ブロモプロピオン酸にエリトロ-2-アミノ-1,2-ジフェニルエタノールから誘導したキラルオキサゾリジノンを導入し,これと活性化金属ゲルマニウムとの反応によって調製したエノラートに種々のアルデヒドを反応させ,いずれの場合にも対応する生成物を極めて高ジアステレオ選択的に得ることに成功している。さらに,脱不斉助剤も容易であることを明らかにし,本反応によって高光学純度の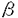 -ヒドロキシカルボン酸誘導体を容易に入手することができることを示している。本成果は,従来困難であったReformatsky反応の不斉化が,活性化金属ゲルマニウムを用いることにより達成できることを示した点で,意義深い。 -ヒドロキシカルボン酸誘導体を容易に入手することができることを示している。本成果は,従来困難であったReformatsky反応の不斉化が,活性化金属ゲルマニウムを用いることにより達成できることを示した点で,意義深い。 第4章では,トリフェニルホスフィン/塩化ゲルマニウム(IV)を用いた -ブロモカルボン酸誘導体の還元反応について述べている。本反応は,ルイス酸の活性化能によって弱い還元能を補うという全く新しい系であり,厳密な無水条件を必要とせずに温和な条件で進行し,広範な -ブロモカルボン酸誘導体の還元反応について述べている。本反応は,ルイス酸の活性化能によって弱い還元能を補うという全く新しい系であり,厳密な無水条件を必要とせずに温和な条件で進行し,広範な -ブロモカルボン酸誘導体に適用可能である点に特徴がある。次いで, -ブロモカルボン酸誘導体に適用可能である点に特徴がある。次いで, , , -ジブロモ- -ジブロモ-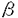 -ラクタムにトリフェニルホスフィン/塩化ゲルマニウム(IV)を適用し,選択的な半還元を実現することに成功し,高ジアステレオ選択的にシス- -ラクタムにトリフェニルホスフィン/塩化ゲルマニウム(IV)を適用し,選択的な半還元を実現することに成功し,高ジアステレオ選択的にシス- -ブロモ- -ブロモ-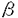 -ラクタムを得ている。さらに,トリフェニルホスフィン/ルイス酸が -ラクタムを得ている。さらに,トリフェニルホスフィン/ルイス酸が -ブロモカルボン酸誘導体のジアステレオ選択的Reformatsky反応に有効であることを明らかにし,炭素-炭素結合生成反応への展開の可能性を示している。 -ブロモカルボン酸誘導体のジアステレオ選択的Reformatsky反応に有効であることを明らかにし,炭素-炭素結合生成反応への展開の可能性を示している。 第5章では,ジコバルトオクタカルボニルを用いた3-シラ-1,7-エンインの新規環化異性化反応による8員環化合物の合成について述べている。3-シラ-1,7-エンインとジコバルトオクタカルボニルから調製したアルキンーコバルト錯体にN-メチルモルホリンN-オキシドを作用させると環化異性化反応が円滑に進行し,8員環ジエニルシラン誘導体が得られることを見出している。一般に,1,7-エンインの環化異性化反応では2位と7位で結合が生成するのに対し,本反応では1位と8位で結合が生成する点が特徴であり,従来全く報告例のない環化モードであることから極めて興味深い反応である。この異常な環化モードはケイ素官能基の導入に起因することを明らかにしており,今後,分子内ヘテロ元素による環化モード制御が可能になるものと期待される。 第6章では,本論文を総括するとともに,将来展望を述べている。 以上のように,低原子価化合物の還元力を利用した有機合成反応を開発している。その成果は,有機合成化学及び有機工業化学の進展に寄与するところ大である。 よって本論文は,博士(工学)の学位請求論文として合格と認められる。 |