近年、真核細胞表層に存在する糖脂質、糖タンパク質に含まれるオリゴ糖鎖の生物学的機能の解明が進むにつれ、これら糖鎖を構築あるいは分解する種々の酵素に対する阻害剤を、医薬、農薬などに利用しようとする試みが活発に行われるようになった。特に最近、新たに糖質加水分解酵素(グリコシダーゼ)阻害剤が癌の転移を抑制することや、抗HIV活性を有することなど、様々な生理活性発現に関与していることが報告され、きわめて注目されている。一方、末だ機能のよくわかっていない糖鎖の研究に、阻害剤を試験薬として積極的に利用しようという試みも行われている。活発なスクリーニングの結果、現在までに多数のグリコシダーゼ阻害剤が報告されている。それらの阻害剤の特徴は、基質と阻害剤それぞれの水酸基の立体配置や三次元構造が類似していることと、加水分解されるグリコシド結合周辺に対応する構造部位に窒素原子を有していることである。そこで、より多くの研究に利用可能であるような試料の多量供給と様々な類縁体の合成による構造活性相関に基づく新しいグリコシダーゼ阻害剤の開発を目的として、有機化学者による化学合成が活発に行われている。 本論文は実用性の開拓と高い酵素特異性を持つ阻害剤の開発を目的とした含窒素糖の合成研究に関するものである。 1.強力な -グルコシダーゼ阻害作用を持つ新規疑似糖類、DAB-1とLAB-1の合成 -グルコシダーゼ阻害作用を持つ新規疑似糖類、DAB-1とLAB-1の合成 近年、ピロリジン骨格を持つ糖の類縁体がグリコシド結合の酵素的な加水分解を阻害することが報告されている。1985年NashらによってAngylocalyx boutiqueanusとArachniodes standishiiから単離されたDAB-1(1)とその鏡像体であるLAB-1(2)は特に強力な -グルコシダーゼ阻害剤として知られている。私はその生物活性に興味を持ち合成に着手した。 -グルコシダーゼ阻害剤として知られている。私はその生物活性に興味を持ち合成に着手した。 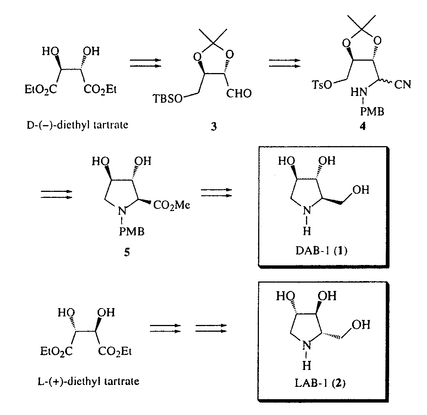 光学活性体であるD-(-)-酒石酸ジエチルを出発物質にして、LiAlH4還元やSwern酸化など4工程、68%の収率でアルデヒド3を得た。次にStrecker反応を用いてアミノ基とニトリル基を同時に付加させ、その後、TBS保護基をTBAFで外して生じたアルコールに対し、トシル化を行って環化前駆体である4を得た。4を酸性条件下でアセタールを除去しながら環化させた後、ニトリル基を塩基性条件下で加メタノール分解したところ、ジアステレオマー比約1:1でメチルエステルが得られた。ここで望まない立体配置を持つジアステレオマーは異性化させる事によって選択的に望む立体配置を持つ5のエステルを得ることが出来た。続いてエステル部分をNaBH4で還元し、最終段階としてPd(OH)2触媒を用いて加水素分解反応で脱保護した後、濃塩酸処理する事によって目的化合物であるDAB-1(1)の塩酸塩を11工程(25-30%収率)で合成することが出来た。同様にL-体の酒石酸ジエチルを出発物質として用いてLAB-1(2)の塩酸塩も合成することが出来た。 2.Nectrisine、4-epi-Nectrisine及びその類縁体の合成 1988年ShibataらによってNectria lucidaから単離されたNectrisine(6)はピペリジン骨格の疑似糖として有名なNojirimycinに比べ,in vitroだけではなくin vivoでも強力な -グルコシダーゼ阻害活性を示し,また高い -グルコシダーゼ阻害活性を示し,また高い -マンノシダーゼ阻害活性もあわせ持っている。またNectrisineの異性体である4-epi-Nectrisine(7)はまだその活性が知られてなかったので、実用的合成ルートの開拓と -マンノシダーゼ阻害活性もあわせ持っている。またNectrisineの異性体である4-epi-Nectrisine(7)はまだその活性が知られてなかったので、実用的合成ルートの開拓と -グルコシダーゼ阻害及び -グルコシダーゼ阻害及び -マンノシダーゼ阻害という二つの活性分離を目的として、この6と7そして一連の類縁体の合成に着手した。まず、D-(-)-酒石酸ジエチルから5段階で収率よくアミノニトリル10をジアステレオマー混合物として得る事が出来た。続いてTBS保護基をはずし、1級アルコール部分をTPAP,NMO条件下で酸化的環化反応を行い、ピロリジン化合物11を得た。そしてニトリル基を加メタノール分解してメチルエステルとし、さらにエステルをLiBH4で還元後、二つのジアステレオマーを分離し、12と13を56:44の割合で得た。得られた13の1級アルコールをTBDPS保護し、窒素保護基をBoc保護基にかえた。ラクタムをLiEt3BHで還元した後、最終段階としてすべての保護基をはずして目的化合物であるNectrisine(6)を15工程(10-12%収率)で合成することができた。 -マンノシダーゼ阻害という二つの活性分離を目的として、この6と7そして一連の類縁体の合成に着手した。まず、D-(-)-酒石酸ジエチルから5段階で収率よくアミノニトリル10をジアステレオマー混合物として得る事が出来た。続いてTBS保護基をはずし、1級アルコール部分をTPAP,NMO条件下で酸化的環化反応を行い、ピロリジン化合物11を得た。そしてニトリル基を加メタノール分解してメチルエステルとし、さらにエステルをLiBH4で還元後、二つのジアステレオマーを分離し、12と13を56:44の割合で得た。得られた13の1級アルコールをTBDPS保護し、窒素保護基をBoc保護基にかえた。ラクタムをLiEt3BHで還元した後、最終段階としてすべての保護基をはずして目的化合物であるNectrisine(6)を15工程(10-12%収率)で合成することができた。  次に先ほど得られた12からNectrisine合成と同様に1級アルコールの保護、アミンのBoc保護基への変換、続くLiEt3BHによるラクタムの還元、そして酸加水分解による脱保護によって4-epi-Nectrisine(7)を15工程(8-10%収率)で合成した。またNectrisineの類縁体である5-Deoxynectrisine(8)の合成においては13からアルコールのトシル化,ヨウ素化を経て、続く加水素分解反応を行い5-Deoxy中間体を得た後、Nectrisine合成に用いられた手法に従って合成に成功した。ピロリドン9は13から2段階の脱保護により調製した。現在13からの選択的な脱保護によって可能になった2-Deoxynectrisine及びその異性体の合成ルートを検討中である。また、今回得られた目的化合物及びその重要中間体は生物活性試験により、それらの阻害活性が明らかになった。 3.Broussonetine Cに関する合成研究。 1997年Kusanoらによって落葉樹であるBroussontia kazinokiの枝から単離されたBroussonetine C(14)はピロリジン骨格と共に長い側鎖を持つ新しいタイプの構造を有している。また高い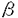 -ガラクトシダーゼ及び -ガラクトシダーゼ及び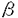 -マンノシダーゼ阻害活性をあわせ持っている。 -マンノシダーゼ阻害活性をあわせ持っている。  合成計画としては18の様なハロゲン化アルキルから調製した有機金属を用いてNectrisineの合成中間体から容易に得られるラクタムあるいはそのO-メチル,アセチル誘導体19に置換させると20の様な中間体が得られると考えた。1,10-デカンジオール15の一方の水酸基のTBDPS保護した後、もう一方の水酸基をSwern酸化しアルデヒドを得た。1,3-プロパンジチオールを用いてこのアルデヒドをジチオアセタール16へと変換、続いてt-ブチルリチウムでアニオンを発生させ、臭化物17とカップリングした後、シリル基を外してアルコールを得た。アルコールのヨウ素化あるいはブロム化により18を合成した。現在20を得るための有機金属を用いた立体選択的なアルキル化を検討している。  以上、私は本研究を通じて多数のグリコシダーゼ阻害剤の合成法について述べた。現在、様々なグリコシダーゼに対する強力かつ特異的な阻害剤の必要性が高まっているので、本研究によりさらなる構造活性相関の研究に貢献したいと思っている。 |