真核生物にはアクチン系と微小管系の2つに大別される運動系が備わっており、それらは基本的に2種類の蛋白質集合体の間の滑り運動である。 骨格筋に特有な収縮構造である筋原線維は、ミオシンとアクチンの二収縮蛋白質が全体の65%を占めており、骨格筋の運動はこれらの間の相対的な滑りによって説明される。また、非筋肉細胞にもアクチン系が存在しており、例えば、植物細胞に一般に見られる現象である原形質流動はアクチン系による運動である。 一方、真核細胞に広く存在する微小管は細胞の運動や細胞の形態形成およびその保持に関係している。微小管上で動力を発生する因子は微小管モーター蛋白質と呼ばれるが、その一種であるダイニンは繊毛や鞭毛の周縁に結合してATPを分解しつつ、向かい合う微小管をずらして運動を起こすと考えられている。また、染色体の移動にも関与し、微小管上をマイナス端方向へ運動する。これとは逆にプラス端方向へ運動するモーター蛋白質としてキネシンが存在する。これは最初、イカの神経細胞において軸索輸送を行う蛋白質として発見されたが、その後、他の細胞にも広く存在が確認され、重要かつ多様な生理的機能を担うと考えられている。例えば、カビや分裂酵母の紡錘体の形成、ショウジョウバエの染色体の分離、線虫のシナプス小胞の軸索輸送などにおいて、キネシン・スーパーファミリーの関与が示唆されている。キネシンは分子量約115,000の重鎖と65,000の軽鎖各2本からなり、電子顕微鏡で見た全体像はミオシンに似ている。また、ショウジョウバエの重鎖cDNAから全一次構造が決定され、N末付近にATP結合部位を含む分子量約50,000の球状ドメインが存在すると予測されている。 当研究室ではすでに、シロイヌナズナのゲノム上から、高等植物で初めて複数のキネシン関連遺伝子と考えられる配列を見出し、それらの配列に対応するcDNAをクローン化し塩基配列を決定した。その結果、キネシン重鎖ではモータードメインがN末端側に位置するのに対し、これらはいずれもC末端側領域にキネシン重鎖のモータードメインと相同と考えられるアミノ酸配列を有し、一部については微小管結合能やATPase活性をもつことも示された。また、アミノ酸配列の二次構造予測によりキネシンに特徴的なcoiled coil構造をとることも分かった。 本研究は、高等植物における新たなキネシン関連遺伝子の単離と、その機能のより明解な研究のための新しいモデル系を構築することを目的としたものである。 1.タバコ培養細胞BY-2キネシン重鎖関連遺伝子の単離 種々のキネシン重鎖のモータードメイン内の、特に保存性の高い領域のアミノ酸配列に基づいてオリゴヌクレオチドプライマーを合成し、BY-2のRNAを用いた RT-PCRを行ったところ、約500塩基対の増幅産物が得られた。この産物の塩基配列はキネシン重鎖のそれと高い相同性を示したので、BY-2からpoly(A)+RNAを調製し、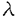 gt10をベクターとして作成したcDNAライブラリーを、これをプローブとしてスクリーニングした。その結果得られた遺伝子の塩基配列を決定したところ、微小管結合部位、およびATP結合部位を含むモータードメインをもつ、キネシン様の配列であることが分かった。また、シロイヌナズナのキネシン関連遺伝子と特に相同性が高く、シロイヌナズナ同様C末端側領域にモータードメインを持っていた。 gt10をベクターとして作成したcDNAライブラリーを、これをプローブとしてスクリーニングした。その結果得られた遺伝子の塩基配列を決定したところ、微小管結合部位、およびATP結合部位を含むモータードメインをもつ、キネシン様の配列であることが分かった。また、シロイヌナズナのキネシン関連遺伝子と特に相同性が高く、シロイヌナズナ同様C末端側領域にモータードメインを持っていた。 2.ウシ脳チューブリンによる検定 微小管は主要構成成分であるチューブリンが重合して管状構造を取ったものであり、微小管壁にはMAPs(微小管結合蛋白質、microtubule-associated proteins)と呼ばれる多種類の非チューブリン蛋白質が結合している。MAPsはチューブリンの重合を促進し、再構成された微小管に結合して微小管を安定化させる活性をもつ。チューブリンとMAPsを総称して微小管蛋白質と呼ぶ。微小管蛋白質は37℃で重合して微小管となり、遠心により沈殿として回収される。一方、微小管は0℃で脱重合して、微小管蛋白質は遠心上清に回収される。この性質を利用してウシ脳より調製した微小管蛋白質をセルロースカラムを用いて微小管蛋白質画分からMAPsを除き、チューブリンを得た。また、BY-2より得られたキネシン重鎖関連遺伝子のモータードメインを、PCR産物を発現ベクターに組み込むことで大腸菌内で過剰発現させて約40,000の大きさの蛋白質を得た。これを、ウシ脳より精製したチューブリンをタキソールによって安定化させた微小管を用いてキネシン活性の検定を行った。その結果、この蛋白質は、微小管との結合能、および微小管上を運動する能力を持つことが分かった。この運動はプラス端方向でありキネシン重鎖とは一致するが、塩基配列が類似しており、さらに、同じC末端側にモータードメインを持つ酵母(Saccharomyces cerevisiae)のKAR3遺伝子の運動方向とは逆であった。また、ATPase活性があり、その活性は微小管の存在下で上昇することが示された。 3.シロイヌナズナチューブリンによる検定 今回単離したキネシン重鎖関連遺伝子は高等植物であるタバコより得られたものであるが、この遺伝子のより厳密な検定には、動物であるウシ脳のチューブリンによる検定の他に、さらに植物のチューブリンによる検定が必要であると思われる。従って、まず、タバコより微小管蛋白質の精製を試みたが、実験に供するだけの十分な量の微小管蛋白質が得られなかった。次に、既に塩基配列が明らかになっているシロイヌナズナのチューブリンの塩基配列に基づいてオリゴヌクレオチドプライマーを合成し、大腸菌内で 、 、 チューブリンを過剰発現させた。これらは温度および発現誘導物質であるIPTGの濃度等の条件を変えても大部分が不溶性画分に封入体として発現する。よって、再活性化の条件検討を行った。その結果、 チューブリンを過剰発現させた。これらは温度および発現誘導物質であるIPTGの濃度等の条件を変えても大部分が不溶性画分に封入体として発現する。よって、再活性化の条件検討を行った。その結果、 、 、 チューブリンの活性が再生し、両者の重合が見られた。これを用いて検定を行ったところ、 チューブリンの活性が再生し、両者の重合が見られた。これを用いて検定を行ったところ、 チューブリン、 チューブリン、 チューブリンそれぞれとの結合能があることが示された。また チューブリンそれぞれとの結合能があることが示された。また 、 、 チューブリンの重合体である微小管とも結合した。 チューブリンの重合体である微小管とも結合した。 4.タバコBY-2チューブリンによる検定 検定をより生体内での状況に近づけるために、BY-2よりチューブリン遺伝子の単離を試みた。まず、シロイヌナズナのチューブリンの発現に用いたオリゴヌクレオチドプライマーを利用し、BY-2のRNAを用い、RT-PCRを行ったところ、 チューブリンのプライマーに対しては約1300塩基対の増幅産物が見られたが、 チューブリンのプライマーに対しては約1300塩基対の増幅産物が見られたが、 チューブリンのプライマーに対しては増幅は見られなかった。これは、種々の チューブリンのプライマーに対しては増幅は見られなかった。これは、種々の チューブリンのC末端の配列が多岐にわたっていることによると思われたので、 チューブリンのC末端の配列が多岐にわたっていることによると思われたので、 チューブリンに関してはC末端よりも少し上流の相同性の高い領域に基づいてプライマーを合成し、再度RT-PCRを試みたところ増幅が見られた。これらのPCR産物の塩基配列を決定し、また、RACE法によって両末端の配列も調べ新たにオリゴヌクレオチドプライマーを合成し、それらを用いたPCRによって増幅した産物を発現ベクターに組み込むことによって大腸菌内で発現させた。この結果得られた蛋白質もシロイヌナズナの時と同様、封入体で発現したので、活性の再生を行い、検定に用いた。結果はシロイヌナズナの時と同様、 チューブリンに関してはC末端よりも少し上流の相同性の高い領域に基づいてプライマーを合成し、再度RT-PCRを試みたところ増幅が見られた。これらのPCR産物の塩基配列を決定し、また、RACE法によって両末端の配列も調べ新たにオリゴヌクレオチドプライマーを合成し、それらを用いたPCRによって増幅した産物を発現ベクターに組み込むことによって大腸菌内で発現させた。この結果得られた蛋白質もシロイヌナズナの時と同様、封入体で発現したので、活性の再生を行い、検定に用いた。結果はシロイヌナズナの時と同様、 チューブリン、 チューブリン、 チューブリン、微小管それぞれとの結合が観察された。 チューブリン、微小管それぞれとの結合が観察された。 5.キネシン軽鎖関連遺伝子単離の試み キネシンは2本の重鎖と2本の軽鎖から成る四量体であることが知られているが、BY-2にも軽鎖に相当する遺伝子が存在するかどうか検討してみた。まず、重鎖が得られたときと同様の手法で、軽鎖の塩基配列のうち特に保存性の高い配列に基づくオリゴヌクレオチドプライマーによる、BY-2およびシロイヌナズナのRNAを用いたRT-PCRでは、種々のプライマーに対して、増幅産物が全く得られないか、あるいは増幅が認められてもその配列は既知の軽鎖の配列とは大きく異なるものであった。また、Two-hybridによってライブラリーをスクリーニングすることでキネシン重鎖に結合するキネシン軽鎖関連遺伝子を探索する方法も試みたが、同様に満足な結果は得られなかった。従って、高等植物にはキネシン軽鎖関連遺伝子が存在しないか、あるいは、キネシン軽鎖様の活性を持つ遺伝子が存在はするが、その塩基配列が既知のキネシン軽鎖とは大きく異なる等の可能性が考えられる。 まとめ 高等植物であるタバコ培養細胞BY-2よりキネシン活性をもつ遺伝子の単離に成功し、また、 、 、 チューブリンを大腸菌内で過剰発現させて得られた蛋白質を用いることで、従来の単離精製した微小管を用いる手法における、微小管に付随する他の蛋白質の関与という問題点を考慮することなくキネシン重鎖の微小管およびチューブリンとの相互作用を直接に検定できる新たなモデル系を構築することが出来た。これによって得られた、キネシンとチューブリンが直接的に相互作用するという結果および、今回キネシン軽鎖がBY-2に見いだせなかったと言うことを考え合わせると、キネシンが細胞内微小管系運動を行ううえで、重鎖が大部分の重要な役割を果たしていることが示唆される。 チューブリンを大腸菌内で過剰発現させて得られた蛋白質を用いることで、従来の単離精製した微小管を用いる手法における、微小管に付随する他の蛋白質の関与という問題点を考慮することなくキネシン重鎖の微小管およびチューブリンとの相互作用を直接に検定できる新たなモデル系を構築することが出来た。これによって得られた、キネシンとチューブリンが直接的に相互作用するという結果および、今回キネシン軽鎖がBY-2に見いだせなかったと言うことを考え合わせると、キネシンが細胞内微小管系運動を行ううえで、重鎖が大部分の重要な役割を果たしていることが示唆される。 |