トランスポゾンはゲノム上のある部位から他の部位に転移可能な遺伝因子で、生物に普遍的に存在する。トランスポゾンは、その転移によって挿入だけでなく、欠失や逆位、重複、融合等の非相同的組換えによる変異を引き起こすことが知られている。これらトランスポゾンの特性は生物のゲノムの可塑性を高める大きな要因となっており、生物の進化にも大きな役割を果たしてきたと想像される。 Tn3(4957bp)は細菌に存在する代表的なトランスポゾンで、アンピシリン耐性遺伝子blaを運ぶ。腸内細菌のみならず海洋・土壌細菌からもbla以外の様々な薬剤耐性遺伝子や重金属耐性遺伝子などを運ぶTn3様のトランスポゾンが多数発見されているが、その転移機構に関する研究はほとんど進展していなかった。これは主に転移を司る酵素であるトランスポゼースの生化学的な解析が困難であったことに起因していると考えられる。Tn3及び、その類縁のトランスポゾン 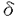 のトランスポゼース(M.W.=約110,000)の精製は早くから試みられ、それがTn3の末端の38bpの繰り返し配列(inverted repeat;IR)に特異的に結合する活性とともに強い非特異的DNA結合活性を持つことが示されていた。トランスポゼースはDNA結合活性のほかにも、Tn3の末端を切断する活性や、切断されたTn3末端を標的DNAにトランスファーする活性を持つことが予想されるが、精製したトランスポゼースの酵素活性についてはこれまで報告がなかった。 のトランスポゼース(M.W.=約110,000)の精製は早くから試みられ、それがTn3の末端の38bpの繰り返し配列(inverted repeat;IR)に特異的に結合する活性とともに強い非特異的DNA結合活性を持つことが示されていた。トランスポゼースはDNA結合活性のほかにも、Tn3の末端を切断する活性や、切断されたTn3末端を標的DNAにトランスファーする活性を持つことが予想されるが、精製したトランスポゼースの酵素活性についてはこれまで報告がなかった。 本研究は、転移反応を司る酵素であるトランスポゼースを酵素活性のある状態で精製することを最初の目標とし、酵素活性をin vitroで詳細に解析することでTn3の転移機構を明らかにすることを最終目標に行ったものであり、得られた結果は以下のように要約される。 1.Tn3のcell-free転移系における転移の解析 当研究室の市川らは、Tn3のトランスポゼースを発現させた大腸菌の粗精製タンパク質画分を用い、プラスミドDNA上のmini-Tn3を DNAに転移させるcell-free系を構築した。本研究において、プラスミドDNAを転移の標的として用いたTn3のcell-free転移系を構築したところ、転移が供与体DNA103分子あたり約1個という効率のよい頻度で起こっていることが分かった。この系における転移にはトランスポゼース、ATP、Mg2+、dNTPs、ポリビニールアルコール(PVA)が必須であった。転移産物を解析した結果、供与体DNAと標的DNAがmini-Tn3を介して融合したコインテグレートと標的DNAにmini-Tn3が挿入された単純挿入体があることが分かった。挿入部位をDNAシークエンシングによって決定したところ、挿入は標的プラスミドの様々な部位で起きており、挿入部位はATに富む配列で標的配列の重複は5bpであることがわかった。これらの結果は、in vivoにおけるTn3の転移と同様の転移反応がこの系において再現できることを示したものである。 DNAに転移させるcell-free系を構築した。本研究において、プラスミドDNAを転移の標的として用いたTn3のcell-free転移系を構築したところ、転移が供与体DNA103分子あたり約1個という効率のよい頻度で起こっていることが分かった。この系における転移にはトランスポゼース、ATP、Mg2+、dNTPs、ポリビニールアルコール(PVA)が必須であった。転移産物を解析した結果、供与体DNAと標的DNAがmini-Tn3を介して融合したコインテグレートと標的DNAにmini-Tn3が挿入された単純挿入体があることが分かった。挿入部位をDNAシークエンシングによって決定したところ、挿入は標的プラスミドの様々な部位で起きており、挿入部位はATに富む配列で標的配列の重複は5bpであることがわかった。これらの結果は、in vivoにおけるTn3の転移と同様の転移反応がこの系において再現できることを示したものである。 この系において、Tn3IRをもたせたプラスミドを標的DNAに用いるとIRをもたないプラスミドに比べ転移頻度が約1/3に低下することがわかった。これはin vivoで観察されていた転移免疫現象をこの系において再現できたものである。この標的DNAにIRをもたせると転移頻度が低下するという効果は、標的DNAを反応溶液とあらかじめインキュベーションしておくことにより強められ、このときの転移頻度は約1/8に低下した。標的DNAにIRの変異体をもたせた実験から、転移免疫にはIR全体が必要なのではなく、トランスポゼース結合部位があれば十分であることを示した。この結果はトランスポゼースが標的DNAのIRに結合することが転移免疫を現すのに重要であることを示している。 2.ニッキング活性を指標としたトランスポゼースの精製と、ニッキング促進因子(NSF:Nicking Stimulation Factor)の精製 cell-free転移系において、IRの3’末端特異的にニックが生じていた。このニックはトランスポゼースとMg2+に依存しており、T4DNAリガーゼにより修復可能なものであった。ニッキング活性を指標にトランスポゼースを比活性で約1300倍に精製した。また、ゲルろ過カラムクロマトグラフィーにおける溶出ピークからトランスポゼースの分子量を算出した結果、トランスポゼースが2量体化していることが示唆された 精製したトランスポゼースのニッキング活性は弱いものであったが、トランスポゼースを発現していない大腸菌の破砕液を加えることによりニッキング活性は促進された。このことは、宿主由来の因子にトランスポゼースのニッキング活性を促進する因子(NSF:Nicking Stimulation Factor)が存在することを示す。NSFを大腸菌の破砕液からトランスポゼースのニッキング活性を促進する活性を指標に数種のカラムクロマトグラフィーを行って精製しようと試みた。最後のステップにグリセロール密度勾配遠心法を用いた結果、沈降係数からNSFは11Kd程度のかなり小さな分子であることが分かったが、活性と一致して溶出されるタンパク質は認められなかった。DNAの組み換えや複製を促進する因子としては様々な実験系において数種類のヒストン様タンパク質が同定されている。しかし、これらのヒストン様タンパク質の欠損株から調整した菌体破砕液もニッキング促進活性を有していた。NSFの熱安定性を調べたところ、95℃で5分間熱処理を行ってもほとんど活性が低下しないことがわかった。そこで精製の最初のステップとして熱処理を行った結果、NSFをSDS-PAGEにおいて単一のバンドになるまで精製することができた。このタンパク質のアミノ酸配列を決定したところ、大腸菌のACP(Acyl Carrier Protein)と一致した。さらに、NSFのニッキング促進活性は抗ACP抗体によって阻害されること、またNSFの大きさや熱安定性もACPの特性と一致することから、NSFはACPであると結論した。 ACPは酸性アミノ酸残基に富む小さなタンパク質で、脂肪酸生合成においてアシル基を供与する因子として同定された。アシル基を供与できないapo-ACPも同程度のニッキング促進活性を有していたことから、ニッキング促進活性にはACPの補欠分子団は関与していないことが分かった。また、塩基性アミノ酸残基を多く含むトランスポゼースとACPが非特異的に静電的相互作用をしてニッキング促進効果がみられる可能性を考え、様々なポリアニオンでニッキング促進効果がみられるか検討したが、試験した全てのポリアニオンはニッキング促進効果をもたなかった。このことはトランスポゼースとACPの間に特異的な相互作用が存在することを示唆する。 3.DNA-タンパク質複合体の解析 mini-Tn3を運ぶプラスミドpSIR24にトランスポゼースを混合し更にACPを加えた反応物をゲル電気泳動で分析するとトランスポゼースとACPに依存してDNAのバンドがラダー状に遅れて泳動された。反応物をプロテアーゼや制限酵素で処理した結果から、ラダー状に遅れたDNAのバンドはタンパク質がDNAに結合したDNA-タンパク質複合体で、DNAのトポロジーの変化ではないことが分かった。また、DNA-タンパク質複合体がラダー状になるということはDNA上に結合しているタンパク質の数を反映しているものであることが示唆された。抗ACP抗体と抗トランスポゼース抗体を用いてDNA-タンパク質複合体中のタンパク質をウェスタンブロッティング法で解析したところ、ラダー状のDNA-タンパク質複合体にはACPとトランスポゼースの両方のタンパク質が含まれることが分かった。このことはニッキング反応の促進がトランスポゼースとACPの直接的な相互作用により引き起こされることを示唆するものである。 ニッキング反応において、ACPの量を増やしていくとそれにともないDNA-タンパク質複合体が生じ、ニッキングが促進された。また、ニッキング反応において、反応時間とともにDNA-タンパク質複合体が生じ、ニッキングが促進された。これらの観察はDNA-タンパク質複合体の形成がニッキングの促進と強く相関していることを示すものである。 DNAとトランスポゼースとACPを混合する順番の影響を調べた。その結果、ACPはDNAに結合したトランスポゼースに作用することでのニッキング促進効果を示すことが示唆された。このときDNA-タンパク質複合体がどのように変化するかを低イオン強度下でのアガロースゲル電気泳動で分析した。DNAとトランスポゼースを混合し30分間インキュベートすると、ゲルトップおよびDNAより少しシフトした位置にDNA-タンパク質複合体が生じていることが観察された。ここにACPを加え更に15分間インキュベートするとゲルトップに生じていたDNA-タンパク質複合体は消失し、新たにラダー状のDNA-タンパク質複合体が生じた。このことはACPがDNA-トランスポゼースのネットワーク状のDNA-タンパク質複合体を解離させる"シャペロン"として機能していることを示唆している。 以上の結果から、ACPによるトランスポゼースのニッキング活性促進の機構について次のようなモデルを考えている。トランスポゼースはIR特異的DNA結合ドメインの他に複数の非特異的DNA結合ドメインを持つことがすでに明らかにされているが、このためIRに結合しニッキング反応を行うような「正しい」コンフォメーションをとる前にネットワーク状のアグリゲートを生じ、トランスポゼースの自由な動きが妨げられる。そこにACPを加えるとACPがアグリゲートを生じているDNAと置換されトランスポゼースが自由に動けるようになりラダー状の複合体を生じる。そのうちのIRを探し当てたトランスポゼースがニッキング反応を行う、というものである。 ACPは脂肪酸生合成においてアシル基を供与する因子として同定されたが、現在では様々な代謝系で機能していることがわかっている。また、ACPは大腸菌の染色体分配に関わるDNA結合タンパク質MukBやトランスポゾンTn7の転移標的DNA捕捉タンパク質TnsDとも相互作用していることがわかっている。これらのことと本研究の結果は、ACPが新たな生理活性、すなわちDNA結合たんぱく質のDNA結合能を調節するような活性をもっているのではないかということを示唆するものである。 |