| 内容要旨 | | 【序論】 生体内カテコールアミン分析は、交感神経系に関与する機能をはじめ、様々な生体内機能を把握するために非常に重要であり、簡便かつ迅速な分析法が求められている。生体内カテコールアミン分析法には、(1)前処理が簡便であること、(2)他の物質による妨害が少なく高選択的であること、(3)少量のサンプルで測定できるように高感度であることなどが要求されるが、これらの条件をすべて満たす優れた分析法として、高速液体クロマトグラフィー(HPLC)-過シュウ酸エステル化学発光検出法を軸とした全自動血中カテコールアミン分析計が開発された1)。しかし、この分析計の問題点として、分析時間が長いこと、多種類の試薬溶液を用いるため溶媒消費量が多くなることなどが挙げられた。そこで、最近開発されたHPLC用ファストカラム(粒子径2 m)やセミミクロカラム(内径2.0mm)を分離カラムとして適用することにより、全自動カテコールアミン分析計の高性能化を試みた。具体的には、分析時間の短縮のためにファストカラムを、省溶媒化のためにセミミクロカラムを用いることにし、各々のカラムを導入するために必要な諸条件(各試薬溶液の反応条件など)について検討を行った。 m)やセミミクロカラム(内径2.0mm)を分離カラムとして適用することにより、全自動カテコールアミン分析計の高性能化を試みた。具体的には、分析時間の短縮のためにファストカラムを、省溶媒化のためにセミミクロカラムを用いることにし、各々のカラムを導入するために必要な諸条件(各試薬溶液の反応条件など)について検討を行った。 また、現在、その作用等について非常に注目されている新規内因性生理活性物質として一酸化窒素(NO)が挙げられるが、NOによってニトロ化されたと考えられる6-nitrono-repinephrineが、ブタやラットの脳内に存在することが報告された2)。そこで、上記で検討・開発した分析計を用いて、カテコールアミンと6-ニトロカテコールアミンの一斉分析を検討した。また、検討した分析計を用いて、ラット血中及び組織(全脳・副腎)中のカテコールアミンと6-ニトロカテコールアミンの一斉分析を行った。 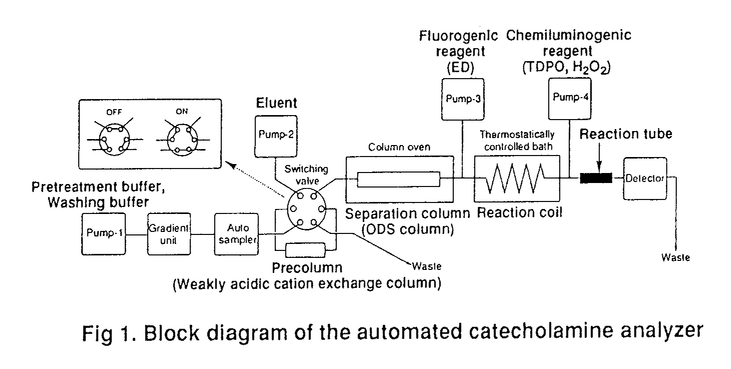 Fig1. Block diagram of the automated catecholamine analyzer【実験方法・結果・考察】1.本研究の検討対象である全自動カテコールアミン分析計について Fig1. Block diagram of the automated catecholamine analyzer【実験方法・結果・考察】1.本研究の検討対象である全自動カテコールアミン分析計について 本研究の検討対象である全自動カテコールアミン分析計は、まず弱酸性陽イオン交換カラムとカラムスイッチング法との組み合わせにより、生体試料中のカテコールアミン(norepinephrine(NE)、epinephrine(E)、dopamine(DA))を抽出した後、オクタデシルシリカ(ODS)カラムで分離し、エチレンジアミン(ED)による蛍光誘導体化反応を行った後、bis[2-(3,6,9-trioxadecanyloxycarbonyl)-4-nitrophenyl]oxalate(TDPO)とH2O2を用いた過シュウ酸エステル化学発光検出法により高感度検出を行う仕組みになっている(Fig.1)。なお、HPLC用送液ポンプには、PU-980(JASCO)やNANOSPACE SI-1/2001(SHISEIDO)を、化学発光検出器にはFP-920(CL option)(JASCO)等を用いた。また、分離カラムには、従来のシステムで用いられていたCrestpak-C18S(4.6mm i.d.×150mm;5 m;JASCO)、ファストカラムとしてTSKgel Super-ODS(4.6mm i.d.×100mm;2 m;JASCO)、ファストカラムとしてTSKgel Super-ODS(4.6mm i.d.×100mm;2 m;TOSOH)、セミミクロカラムとしてTSKgel ODS-80Ts(2.0mm i.d.×150mm;5 m;TOSOH)、セミミクロカラムとしてTSKgel ODS-80Ts(2.0mm i.d.×150mm;5 m;TOSOH)等を用い、前処理用の弱酸性陽イオン交換カラムには、Cpak-P(4.0mmi.d.×10mm;JASCO)を用いた。 m;TOSOH)等を用い、前処理用の弱酸性陽イオン交換カラムには、Cpak-P(4.0mmi.d.×10mm;JASCO)を用いた。 2.ファストカラムを用いた全自動カテコールアミン分析計の高速化3)、4) 微小粒子(粒子径2 m)を充填したカラムであるファストカラムをHPLCに適用する利点として、移動相の流速を増加させても理論段数が大きく変化しないため、高分離能を維持したまま分析の高速化が容易に達成できる点が挙げられる。そこで、全自動カテコールアミン分析計の高速化を達成するために、移動相・蛍光試薬・化学発光試薬について、各試薬の組成や流速を再検討した。その結果、移動相の組成を調整し、かつ各試薬の流速を従来の分析計の2倍に設定することにより、各カテコールアミン間の分離を維持したまま、分析時間を従来(Fig.2、左図)の約半分(Fig.2、中図)に短縮することに成功した。また、検出感度や定量範囲は、従来の分析計とほぼ同様の値(検出限界(S/N2)が数fmol/injection、定量範囲が25fmol〜1000fmol/injection)が得られた。 m)を充填したカラムであるファストカラムをHPLCに適用する利点として、移動相の流速を増加させても理論段数が大きく変化しないため、高分離能を維持したまま分析の高速化が容易に達成できる点が挙げられる。そこで、全自動カテコールアミン分析計の高速化を達成するために、移動相・蛍光試薬・化学発光試薬について、各試薬の組成や流速を再検討した。その結果、移動相の組成を調整し、かつ各試薬の流速を従来の分析計の2倍に設定することにより、各カテコールアミン間の分離を維持したまま、分析時間を従来(Fig.2、左図)の約半分(Fig.2、中図)に短縮することに成功した。また、検出感度や定量範囲は、従来の分析計とほぼ同様の値(検出限界(S/N2)が数fmol/injection、定量範囲が25fmol〜1000fmol/injection)が得られた。  Fig.2 Chromatograms of catecholamines3.セミミクロカラムを用いた全自動カテコールアミン分析計の溶媒消費量の削減3)、5) Fig.2 Chromatograms of catecholamines3.セミミクロカラムを用いた全自動カテコールアミン分析計の溶媒消費量の削減3)、5) セミミクロカラム(内径2.0mm)をHPLCに適用する利点として、移動相の流速が低下しても従来と同じ分離能が得られるので、分析の省溶媒化が可能な点が挙げられる。そこで、まず最初に、移動相・蛍光試薬・化学発光試薬の流速について検討したところ、3種類の試薬溶液の最適流速比が従来の分析計とは異なることが分かり、各試薬の組成についても再検討が必要であることが示唆された。そのため、各試薬の組成等について再検討を行い、その結果、全自動カテコールアミン分析計の溶媒消費量を、従来の約半分に節減することに成功した(Fig.2、右図)。この時、各カテコールアミン間の分離は十分維持されており、検出限界や定量範囲は従来とほぼ同様の値(検出限界(S/N2)が数fmol/injection、定量範囲が25fmol〜1000fmol/injection)が得られた。 また、この分析計で用いられているEDによる蛍光誘導体化反応では、途中でカテコール環がキノン体に酸化される過程を得るため、酸化剤を添加することにより、反応がより促進され、検出感度が向上する可能性が予想された。そこで、酸化剤(K3[Fe(CN)6],NalO4,Phl(OAc)2)の適用に関する検討も行ったが、酸化剤を添加するとベースラインが不安定になる等の不都合が生じたので、今回確立した分析計には酸化剤を適用しないことにした。 4.全自動カテコールアミン分析計を用いたカテコールアミンと6-ニトロカテコールアミンの一斉分析法の確立とその応用 まず最初に、上記で述べた3種類のカテコールアミンに対応する6-ニトロカテコールアミンを合成し、カテコールアミンと6-ニトロカテコールアミンが一斉分析できる分析条件を、3.で検討したセミミクロカラムを適用した分析計を用いて検討した。その結果、カテコールアミンと6-ニトロカテコールアミンの一斉分析が可能になったが(Fig.3、左図)、6-ニトロカテコールアミンの検出感度は、カテコールアミンの検出感度より大幅に低下した。これは、EDとの蛍光誘導体化反応生成物の構造の違いや、この反応における最適反応条件の違いなどが、その原因として推定される。次に、この分析計を用いて、ラット血中及び組織(全脳・副腎)中のカテコールアミンと6-ニトロカテコールアミンの一斉分析を行ったところ、ラット血中や脳中には6-ニトロカテコールアミンは検出されなかった。しかし、ラット副腎において、6-nitronorepinephrineに該当するピークが検出され、その存在の可能性が示唆された(Fig.3、右図)。  Fig.3 Chromatograms of catecholamines and 6-nitrocatecholamines【総括】 Fig.3 Chromatograms of catecholamines and 6-nitrocatecholamines【総括】 まず最初に、ファストカラムやセミミクロカラムを用いることにより、従来より短時間あるいは少量の溶媒量で生体内カテコールアミン分析を行うことが可能な全自動カテコールアミン分析計の構築に成功した。この結果は、従来の全自動血中カテコールアミン分析計が有していた簡便性・高選択性・高感度という利点に、高速と省溶媒化(つまり低コスト)という実用的な利点を加えたことになり、現状では一、二を争う高性能な全自動カテコールアミン分析計の構築に成功した。次に、今回確立した全自動カテコールアミン分析計を用いて、カテコールアミンと6-ニトロカテコールアミンの一斉分析を行うことが可能になった。また、この分析計を用いることにより、ラット副腎中に6-nitronorepinephrineが存在する可能性が示唆された。これらの結果は、交感神経系とNOの関係など現在まだ十分に解明されていない分野を研究するための重要なツールとして、今回開発した分析計が使用できることを示唆している。 【参考文献】1)P.Prados,S.Higashidate and K.Imai,Biomed.Chromatogr.,8,1-8(1994).2)F.Shintani,T.Kinoshita,S.Kanba,T.Ishikawa,E.Suzuki,N.Sasakawa,R.Kato,M.Asai and T.Nakaki,J.Biol.Chem.,271,13561-13565(1996).3)村山一久,P.Prados,三田智文,福島 健,本間 浩,今井一洋,第12回生体成分の分析化学シンポジウム講演要旨集,282(1997).4)村山一久,三田智文,本間浩,今井一洋,日本分析化学会第44年会講演要旨集,617(1995).5)村山一久,三田智文,福島健,本間浩,今井一洋,日本薬学会第117年会講演要旨集(4),90(1997). |