| 内容要旨 | | Introduction 生物は、環境の変化に適切に対応することによって、自己の恒常性を維持しているが、生物が、どのようにして環境の変化を認識しているのか、そして、どのようにして環境の変化に適応しているのかについては、よく理解されていない。 大腸菌からヒトに至る、あらゆる生物の細胞内のDNAは、負にスーパーコイルしているが、最近、大腸菌細胞内のプラスミドDNAが、熱刺激後に急速に弛緩し、その後、熱刺激が続いても、再び元の状態にまでスーパーコイルすること1,3)、大腸菌に冷刺激を与えた場合には、熱刺激を与えた場合とは逆に、細胞内のDNAが急速かつ一過的に負にスーパーコイルすること6)が見いだされた。細胞内におけるDNAのスーパーコイリングは、温度のみならず、酸素分圧や栄養などの環境の変化に応じて変化すること、及びDNAの複製や転写、組み換えなど、細胞の基本的な機能に影響を与えることが知られているので、環境の変化による細胞内のDNAのスーパーコイリングの変化は、細胞が環境の変化を認識し、これに適応する上で重要な役割を担っていることが考えられる。すでに、熱刺激を含む環境のストレスによるDNAの弛緩が、熱ショック蛋白の誘導と密接な関係にあることが見いだされており、DNAの弛緩が熱ショック応答の引き金としての役割を果たしているとする仮説が提唱されている1)。 本研究において、私は、大腸菌における熱刺激によって誘導される急速かつ一過的なDNAの弛緩の分子機構を解明することを目的として、この反応に関与する因子を遺伝学的手法を用いて同定し、さらに、これらの因子の作用機序を生化学的手法を用いて明らかにした。 Results(1)熱刺激によって誘導されるDNAの弛緩を触媒するDNAトポアイソメレースの同定 熱刺激によるDNAの弛緩を触媒するDNAトポアイソメレースの同定を試みたところ、この反応が、負にスーパーコイルしたDNAを弛緩させる酵素であるDNAトポアイソメレースIのみならず3)、これまで弛緩したDNAに負のスーパーコイルを導入する酵素として考えられてきた、DNAジャイレース(大腸菌DNAトポアイソメレースII)によっても触媒されることが分かった3,4)。すなわち、(i)DNAトポアイソメレースIをコードするtopA遺伝子の欠失変異株においても、熱刺激後にプラスミドDNA(pUC118)が弛緩すること(Fig.1)、(ii)topA欠失変異株における熱刺激後のDNAの弛緩が、DNAジャイレースの阻害剤であるナリジキシン酸やオキソリン酸によって阻害されること(Fig.1)、(iii)DNAジャイレースのAサブユニットをコードするgyrA遺伝子のナリジキシン酸耐性変異(nalA26変異)をtopA欠失変異株に導入すると、この株における熱刺激後のDNAの弛緩が、ナリジキシン酸に耐性になることが示された。  Fig.1.Influence of DNA gyrase inhibitor on heat shock-induced DNA relaxation in a topA deletion mutant and its isogenic wild-type strain. Fig.1.Influence of DNA gyrase inhibitor on heat shock-induced DNA relaxation in a topA deletion mutant and its isogenic wild-type strain. さらに、熱刺激によるDNAの弛緩のふたつの経路のうち、DNAジャイレース依存の経路が、これまで知られていなかった、ATP存在下におけるDNAジャイレースによるDNAの弛緩反応の性質によって説明可能であることが見いだされた4)。すなわち、(i)精製したDNAジャイレースが、すでに報告されているATP非存在下のみならず、生理的濃度のATP存在下においても、負にスーパーコイルしたDNAを弛緩させること、(ii)ATP存在下において高温で反応させたDNAジャイレースの産物の飽和レベルが、低温で反応させた場合に比べ、より弛緩していること、(iii)ATP存在下における温度上昇に伴うDNAジャイレースによるDNAの弛緩反応がナリジキシン酸やオキソリン酸によって阻害されることが示された。 (2)熱刺激によって弛緩したDNAの再スーパーコイリングにおける熱ショック蛋白DnaKの関与 熱刺激によって弛緩したDNAの再スーパーコイリングは、クロラムフェニコールによって阻害されることから、この反応に新たな蛋白合成が必要であることが示唆された5)。実際、熱刺激によって弛緩したDNAの再スーパーコイリングに、熱刺激によって誘導される熱ショック蛋白のひとつであるDnaK蛋白が必要であることが分かった5)。すなわち、(i)大腸菌におけるhsp70ホモログであるDnaK蛋白をコードするdnaK遺伝子の温度感受性変異株(dnaK756変異株)や欠失変異株(△dnaK52変異株)では、熱刺激によって弛緩したDNAの再スーパーコイリングが起こらず、逆にDNAが過剰に弛緩すること(Fig.2)、(ii)△dnaK52変異株における熱刺激後のDNAの過剰な弛緩が、低コピー・ベクターであるミニRプラスミド(pKP1673)にクローンした野生型dnaK遺伝子によって抑制されることが示された。 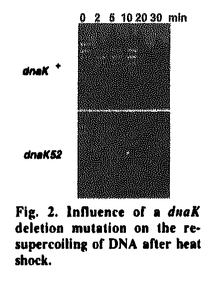 Fig.2.Influence of a dnaK deletion mutation on the resupercoiling of DNA after heat shock. Fig.2.Influence of a dnaK deletion mutation on the resupercoiling of DNA after heat shock. また、DnaK蛋白と並んで細胞内に最も多く含まれる熱ショック蛋白であるGroEL蛋白、及びGroES蛋白をコードするgroEL、及びgroES遺伝子の温度感受性変異株(groEL44変異株、及びgroES72変異株)では、熱刺激後にDNAの過剰な弛緩が起こらないことから5、熱刺激によって弛緩したDNAの再スーパーコイリングにおける熱ショック蛋白の関与は、DnaK蛋白に特異的であることが示唆された。 さらに、この反応におけるDnaK蛋白の機能を明らかにするために、生化学的な解析を試みたところ、(i)△dnaK52変異株から調製した細胞粗抽出液(フラクションII)で反応させたプラスミドDNAが、同じ遺伝学的背景を持つ野生株から調製した細胞粗抽出液で反応させた場合に比べ、より弛緩していること(Fig.3)、(ii)精製したDnaK蛋白が、△dnaK52変異株から調製した細胞粗抽出液中のDNAを負にスーパーコイルさせること(Fig.3)、(iii)精製したDnaK蛋白が、精製したDNAジャイレースによるDNAスーパーコイリング反応を促進させることが分かった5)。DNAジャイレースは、熱刺激によって弛緩したDNAの再スーパーコイリングを触媒する酵素であることから1)、DnaK蛋白は、in vivoにおいて、DNAジャイレースに直接作用することによって、この反応を引き起こしていることが考えられる。このように、熱ショック蛋白がいわゆる"DNA chaperone"としてDNAの超らせん構造の構築に寄与することが、本研究において初めて示された。 (3)熱刺激によって弛緩したDNAの再スーパーコイリングにおけるヒストン様蛋白HUの関与 また、熱刺激によって弛緩したDNAの再スーパーコイリングに、大腸菌染色体の主要な構成成分であるヒストン様蛋白HUが必要であることが見いだされた7)。すなわち、大腸菌におけるヒストン様蛋白であるHU蛋白をコードするhupA、及びhupB遺伝子の二重欠失変異株(hupA16 hupB11変異株)では、danK変異株同様5)、熱刺激後にDNAが過剰に弛緩することが示された。 他のヒストン様蛋白であるIHF蛋白をコードするhimA、及びhimD遺伝子の二重欠失変異株(himA himD変異株)や、H-NS蛋白をコードするhns遺伝子の欠失変異株(hns-2変異株)では、熱刺激後にDNAの過剰な弛緩が起こらないことから、熱刺激によって弛緩したDNAの再スーパーコイリングにおけるヒストン様蛋白の関与は、HU蛋白に特異的であることが示唆された。 精製したHU蛋白は、精製したDNAジャイレースの反応産物を、より負にスーパーコイルさせることが報告されているので、HU蛋白は、in vivoにおいて、DNAジャイレースによるDNAスーパーコイリング反応を促進させることによって、熱刺激によって弛緩したDNAの再スーパーコイリングを引き起こしていることが考えられる。また、hupA16 hupB11変異株において、熱刺激後にDNAが過剰に弛緩するとき、その生菌数が低下することから、熱刺激後のDNAの過剰な弛緩と細胞死との間に相関関係があることが見いだされた7)。  Fig.3.Co-migration of DnaK protein and stimulation of DNA supercoiling reaction in a crude cell extract,fraction II,prepared from the Fig.3.Co-migration of DnaK protein and stimulation of DNA supercoiling reaction in a crude cell extract,fraction II,prepared from the  dnaK52 mutant on Mono Q column chromatography.Discussion dnaK52 mutant on Mono Q column chromatography.Discussion 熱刺激によって弛緩したDNAの再スーパーコイリングの生物学的意義として、(i)熱ショック応答の負の制御5)、及び(ii)熱ストレス存在下における染色体複製開始反応の促進が考えられる5,7)。 dnaK変異株では、熱ショック応答が一過性を失い、熱刺激後に熱ショック蛋白が過剰に誘導されることから、私は、これまで説明が困難であった熱ショック応答の一過性を説明する分子機構として、熱刺激によるDNAの弛緩を引き金として誘導された熱ショック蛋白のうち、DnaK蛋白が、弛緩したDNAを再スーパーコイルさせることによって、自分自身を含む熱ショック蛋白の誘導を停止させるとする、新しいモデルを提唱した(Fig.4)。  Fig.4.A putative model of heat shock response. Fig.4.A putative model of heat shock response. さらに、DnaK蛋白やHU蛋白が、熱刺激後によって弛緩したDNAの再スーパーコイリングを引き起こし、熱ストレス存在下において細胞内のDNAの負のスーパーコイリングを維持していることを考慮すると、dnaK変異株の増殖が高温感受性であること、熱刺激後にhupA16 hupB11変異株の生菌数が低下することの原因は、熱ストレス存在下において細胞内のDNAの負のスーパーコイリングを維持することが出来ないためであることが考えられる5,7)。特に、大腸菌染色体の複製開始起点oriCからのDNA複製開始反応には、鋳型DNAの負のスーパーコイリングが必要であること、熱刺激後にDNAの過剰な弛緩が起こるdnaK変異株では、熱刺激後にDNA合成が阻害されることが報告されているので、DnaK蛋白は、熱ストレス存在下において、細胞内のDNAの負のスーパーコイリングを維持することによって、大腸菌染色体の複製開始反応を促進させ、熱ストレス存在下での細胞増殖を可能にしていることが考えられる5)。これらの知見より、私は、生物が環境の変化に適応し、自己の恒常性を維持することが出来るのは、環境の変化に対し、細胞内のDNAの負のスーパーコイリングを維持することが出来るからであるとする、「"supercoiling homeostasis"による"intracellular homeostasis"の維持」という、これまでにない概念を提唱した5,7)。 References1.Mizushima,T.,Natori,S.and Sekimizu,K.(1993)Relaxation of supercoiled DNA associated with induction of heat shock proteins in Escherichia coli.Mol.Gen.Genet.,238,1-5.2.Ogata,Y.,Miki.T.and Sekimizu,K.(1993)A role of heat shock proteins for homologous recombination in Escherichia coli.Biochem.Biophys.Res.Commun.,197,34-39.3.Ogata,Y.,Mizushima,T.,Kataoka,K.,Miki,T.and Sekimizu,K.(1994)Identification of DNA topoisomerases involved in immediate and transient DNA relaxation induced by heat shock in Escherichia coli.Mol.Gen.Genet.,243,451-455.4.Kataoka,K.,Mizushima,T.,Ogata,Y.,Miki,T.and Sekimizu,K.(1996)Heat shock-induced DNA relaxation in vitro by DNA gyrase of Esherichia coli in the presence of ATP.J.Biol.Chem.271,24806-24810.5.Ogata,Y.,Mizushima,T.,Kataoka,K.,Kita,K.,Miki,T.and Sekimizu,K.(1996)DnaK heat shock protein of Escherichia coli maintains the negative supercoiling of DNA against thermal stress.J.Biol.Chem.,271,29407-29414.6.Mizushima,T.,Kataoka,K.,Ogata,Y.,Inoue,R.and Sekimizu,K.(1997)Increase in negative supercoiling of plasmid DNA in Esherichia coli exposed to cold shock.Mol.Microbiol.23,381-386.7.Ogata,Y.,Inoue,R.,Mizushima,T.,Kano,Y.,Miki.T.and Sekimizu,K.(1997)Heat shock-induced excessive relaxation of DNA in Escherichia coli mutants lacking the histone-like protein HU.Biochim.Biophys.Acta 1353,298-306. |
| 審査要旨 | | 地球上に生物が誕生して以来、あらゆる生物は環境の変化に対応して自己の恒常性を維持する機構を獲得し、発達させてきた。この様な適応現象の分子機構については種々の側面からの研究が進められている。中でも熱ショック応答はその代表的なものであり、多くの生物種に共通なストレス応答の機構が明らかにされつつある。この様な研究の進展を背景として学位申請者は環境適応における細胞内のDNAのスーパーコイリングの役割に注目し研究を開始した。すなわち大腸菌における熱刺激によるDNAの弛緩とそれに引き続く再スーパーコイリングの分子機構の解析を試み、プラスミドDNAを用いた実験系から以下の結果を得た。 まず第一に熱刺激によるプラスミドDNAの弛緩が負にスーパーコイルしたDNAを弛緩させるDNAトポアイソメレース1のみならずDNAジャイレースによっても触媒される事を見い出した。つまりDNAトポアイソメレース1の欠失変異株でも熱刺激によるプラスミドDNAの弛緩が起こり、またこの現象はナリジキシン酸などのDNAジャイレースの阻害剤で見られなくなったのである。これまでDNAジャイレースは弛緩したDNAに負のスーパーコイルを導入する酵素として知られていたが、この様にDNAを弛緩させる活性を持つ事も明らかになったのである。この事実はDNAトポアイソメレース1の欠失変異株にDNAジャイレースのナリジキシン酸耐性変異を導入すると熱刺激によるプラスミドDNAの弛緩がナリジキシン酸に耐性になる事からも明確である。 さて熱刺激によって弛緩したDNAは再び負のスーパーコイルへとその構造を回復するが、その再スーパーコイリングには幾つかのタンパク質が関与している。申請者は大腸菌におけるhsp70ホモログであるDnaKタンパク質の変異株では熱刺激による弛緩後の再スーパーコイリングが起こらず、逆にDNAが過剰に弛緩する事を見い出した。これはDnaKタンパク質以外の主要熱ショックタンパク質であるGroELタンパク質やGroESタンパク質の変異株では見られず、DnaKタンパク質に特異的な生物機能である事が判った。また精製したDnaKタンパク質とDNAジャイレースからDNAスーパーコイリングの反応系を確立し、両者が直接に相互作用して機能している事を明らかにした。さらにこの弛緩後の再スーパーコイリングにヒストン様タンパク質であるHUが関与している事を欠失変異株の解析から見い出した。つまり大腸菌のヒストン様タンパク質HUをコードするhupAおよびhupBの二重欠失変異株ではDnaKタンパク質の変異株同様、DNAが過剰に弛緩する事が観察されたのである。 これらの研究結果から申請者は熱刺激によって弛緩したDNAの再スーパーコイリングの生物学的な意義について考察を行い、熱ショック応答の負の制御と熱ストレス存在下における染色体複製開始反応の促進を提案している。そして生物の環境に対する恒常性の維持に細胞内のDNAの負のスーパーコイリングが重要であるとする「supercoiling homeostasisによるintracellular homeostasisの維持」と言う新しい概念を提唱するに至っている。 以上、本研究では大腸菌における熱刺激によって誘導される急速かつ一過的なDNAの弛緩とその再スーパーコイリングの分子機構を遺伝生化学的な手法で解析し、この反応に関与する因子を明確に示すことができた。これらの研究結果は生物の環境への適応機構を理解する上で極めて重要な成果であり、細胞における恒常性の維持とストレス応答の研究に大きく貢献すると評価される。よって博士(薬学)の学位に値すると判定した。 |