[はじめに] レチノイン酸(all-trans-Retinoic Acid  )は細胞の分化・増殖を促す生命維持に必須の化学物質であり、特異的な核内レセプターRAR(Retinoic Acid Receptor)に結合することで遺伝子の発現を調節している。またレチノイン酸は癌(白血病・皮膚癌)、増殖性皮膚疾患等の治療に有効であり、レチノイドと総称される多くの同効化合物が合成されてきた。しかし、その広範囲にわたる生理活性故に高ビタミンA症や催奇形性等の副作用があり、レチノイドの本質的な作用としてある程度は不可避なものと考えられていた。
)は細胞の分化・増殖を促す生命維持に必須の化学物質であり、特異的な核内レセプターRAR(Retinoic Acid Receptor)に結合することで遺伝子の発現を調節している。またレチノイン酸は癌(白血病・皮膚癌)、増殖性皮膚疾患等の治療に有効であり、レチノイドと総称される多くの同効化合物が合成されてきた。しかし、その広範囲にわたる生理活性故に高ビタミンA症や催奇形性等の副作用があり、レチノイドの本質的な作用としてある程度は不可避なものと考えられていた。
近年、RARには

 のサブタイプが存在すること、またレチノイン酸には結合しないが9-cis-レチノイン酸
のサブタイプが存在すること、またレチノイン酸には結合しないが9-cis-レチノイン酸 に結合するレセプターRXR(Retinoid X Receptor)が発見されこれらにも
に結合するレセプターRXR(Retinoid X Receptor)が発見されこれらにも

 のサブタイプが存在することが判った。レチノイドの広範な作用の選択性を高めるためにはサブタイプ特異的なリガンドの開発が必要であり、これにはリガンド-レセプター蛋白複合体を形成するDriving forceやMechanismなどの基本原理を精密に理解する必要がある。
のサブタイプが存在することが判った。レチノイドの広範な作用の選択性を高めるためにはサブタイプ特異的なリガンドの開発が必要であり、これにはリガンド-レセプター蛋白複合体を形成するDriving forceやMechanismなどの基本原理を精密に理解する必要がある。
薬化学教室ではレチノ安息香酸と称される安息香酸誘導体に強いレチノイド活性を見いだしてきた、特に芳香族アミドAm80はRAR には結合せず、生理作用の分離が可能なレチノイドである。一方Am80のアミド窒素をメチル化したAm90では活性が消失する。これは芳香族アミドが二級のAm80では自由度の大きなトランス型構造で存在するのに対してN-メチル化体Am90は立体障害の大きなシス型構造に変換する事によると考えられる。
には結合せず、生理作用の分離が可能なレチノイドである。一方Am80のアミド窒素をメチル化したAm90では活性が消失する。これは芳香族アミドが二級のAm80では自由度の大きなトランス型構造で存在するのに対してN-メチル化体Am90は立体障害の大きなシス型構造に変換する事によると考えられる。

[ジエナミド化合物の合成とアミドの立体化学] そこで私はユニークな特性をもたらしたアミド結合の立体特性を生かし、アミド結合をレチノイン酸のポリエン鎖に導入した化合物ジエナミドをデザイン・合成しその活性を評価した。即ちall-trans-レチノイン酸の9位10位の二重結合をアミド結合に置き換えた ,
, がall-trans-レチノイン酸アナログとなり、N-メチル化によってシス型アミド
がall-trans-レチノイン酸アナログとなり、N-メチル化によってシス型アミド ,
, となれば9-cis-レチノイン酸アナログとなると考えた。
となれば9-cis-レチノイン酸アナログとなると考えた。

ジエナミド合成では -Iononeを出発原料として転移反応により安定な中間生成物carbamateを導き、ヨウ化リチウムと加熱してcarbamateを気化脱離させる高収率のルートを開発した(Scheme1)。さらにアミド結合の両側の構造を二重結合から芳香族系に置換した化合物を種々合成した。これらの化合物は二級アミドではtrans構造であるがN-メチル化するとジエナミド誘導体ではcis,trans構造が混在し、他方芳香族アミドでは100%cis体に変換した。この事実は構造変換には
-Iononeを出発原料として転移反応により安定な中間生成物carbamateを導き、ヨウ化リチウムと加熱してcarbamateを気化脱離させる高収率のルートを開発した(Scheme1)。さらにアミド結合の両側の構造を二重結合から芳香族系に置換した化合物を種々合成した。これらの化合物は二級アミドではtrans構造であるがN-メチル化するとジエナミド誘導体ではcis,trans構造が混在し、他方芳香族アミドでは100%cis体に変換した。この事実は構造変換には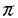 電子が関与している可能性が強く、また
電子が関与している可能性が強く、また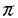 電子でも二重結合より芳香族の方がより強く作用する事を示唆している。
電子でも二重結合より芳香族の方がより強く作用する事を示唆している。
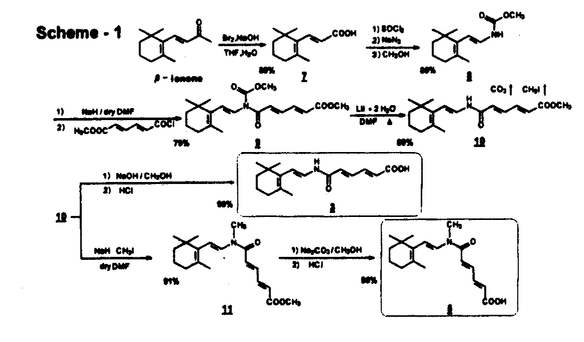 Scheme-1
Scheme-1 Conformational Analysis[Dipoles packing system]
Conformational Analysis[Dipoles packing system] 一方私は以前より別種蛋白質のMolten globule(蛋白質の立体構造形成反応中間体)からNativeになる段階の動的観察にヒントを得てCH結合軌道+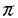 電子原子団+誘電体分子の三者が一組となった空間を介する相互作用力系を発見しDipoles packing systemと名付けた。これを用いて芳香族アミド7をN-メチル化した8ではconformationがtransからcisへの構造変換を以下のように説明することが出来た。
電子原子団+誘電体分子の三者が一組となった空間を介する相互作用力系を発見しDipoles packing systemと名付けた。これを用いて芳香族アミド7をN-メチル化した8ではconformationがtransからcisへの構造変換を以下のように説明することが出来た。
【第一段階】アミド窒素上のメチル基のCH結合軌道とベンゼン環Aの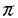 電子軌道とはSoft acidとSoft baseとの関係にあり両者は電荷移動力(charge transfer force)で水素結合を形成する。
電子軌道とはSoft acidとSoft baseとの関係にあり両者は電荷移動力(charge transfer force)で水素結合を形成する。
【第二段階】水素結合プロトンにベンゼン環Aの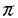 電子が吸引されるので水素結合した側の
電子が吸引されるので水素結合した側の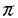 電子平面には電子がより多く集まる事になる、その結果ベンゼン環Aの表裏には電位差が生じてベンゼン環Aは電気双極子に変わる。
電子平面には電子がより多く集まる事になる、その結果ベンゼン環Aの表裏には電位差が生じてベンゼン環Aは電気双極子に変わる。
【第三段階】この電気双極子が作りだす電場Eaは芳香環の表裏二面間で出来ているので指向性を持ち距離による減衰は少ない。このEaの中にベンゼン環Bが入るとBは誘電体であるから分極されて誘導双極子に変わりベンゼン環Aとベンゼン環Bは双極子-誘導双極子相互作用(dipole-induceddipole interaction)で互いに引かれることになる。
このとき第一段階の水素結合によりA環が電気双極子にされる現象は系に電場が生じるので不利な現象であるが、続く第三段階でB環に誘導双極子が発生する現象がA環に生じた電場を緩和することになるので結果的に第一段階の水素結合を有利に進めるように作用する。この因果の応答は相互に有利に作用するので一連の相互作用はサイクルを繰り返して次第に強固になり平衡に達することになる。
芳香族アミドのN-メチル化体がcis100%に変換するのに対してジエナミドN-メチル化体ではcis,trans構造が混在するのは、水素結合によってジエンに誘起される電場は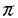 電子数や指向性(電界のまとまり)の点でベンゼン環に誘起される電場よりも相対的に弱く、全ての分子をcisにするだけの力は無いためと説明できる。
電子数や指向性(電界のまとまり)の点でベンゼン環に誘起される電場よりも相対的に弱く、全ての分子をcisにするだけの力は無いためと説明できる。
 Dipoles packing system
Dipoles packing system X線結晶解析、NMRより得られたデータはこの相互作用系の存在を支持するものであった。またこのDipoles packing systemはアミド結合自体には無関係であり、CH結合軌道+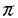 電子原子団+誘電体分子の三つの要素が適切な配置に並ぶ限り普遍的に起きることを他の小化合物で例証した。
電子原子団+誘電体分子の三つの要素が適切な配置に並ぶ限り普遍的に起きることを他の小化合物で例証した。
小さな化合物で実証されたこの相互作用機構は蛋白質のように込み入った構造体では働く機会が増大すると考えられる。そこでレチノイン酸が結合していない不定形のRARを構造の柔軟なMolten globule(立体構造形成反応中間体)ととらえ、レチノイン酸と協同して剛性のある複合体三次構造を構築していく課程をDipoles packing systemを用いて初めて解明した。
RARリガンド結合領域は12個の ヘリックスと
ヘリックスと ターンから構成されており、CH結合軌道(H5鎖のアルキル基アミノ酸残基L268,L271,I275)と誘電体原子団(芳香族残基F288,F230)が一定以上の距離を保った空隙を持っている。この空隙に
ターンから構成されており、CH結合軌道(H5鎖のアルキル基アミノ酸残基L268,L271,I275)と誘電体原子団(芳香族残基F288,F230)が一定以上の距離を保った空隙を持っている。この空隙に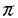 電子原子団であるレチノイン酸が挿入されると直ちにCH結合軌道とレチノイン酸
電子原子団であるレチノイン酸が挿入されると直ちにCH結合軌道とレチノイン酸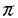 電子との間で水素結合が形成され、次いで双極子となったレチノイン酸とF288の間で双極子-誘導双極子相互作用が生じる。これがリガンド-受容体蛋白質複合体の安定化におけるkey stepであると考えられる。
電子との間で水素結合が形成され、次いで双極子となったレチノイン酸とF288の間で双極子-誘導双極子相互作用が生じる。これがリガンド-受容体蛋白質複合体の安定化におけるkey stepであると考えられる。
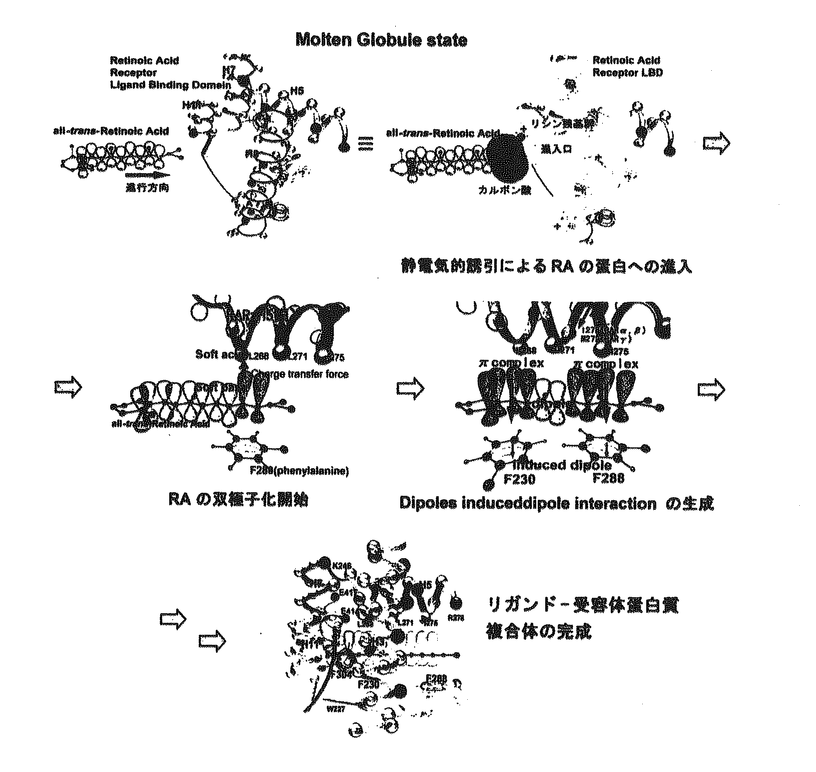 Molten Globule state
Molten Globule state 注目すべき点はDipoles packing systemでは水素結合によってエネルギーを連続的に補充するので複合体自身を自動的に構築することが可能であること、またリガンドに対する特異性・非特異性が生じる原因は複合体構築課程でのMechanismやその許容度に由来していることである。この構造構築を段階別に詳細に示し、最終構造ではX線結晶解析による結合距離・幾何配置を確かめてこの構築原理を検証した。さらにRXRでもRARと同様にDipoles packing systemによって9-cis-レチノイン酸と協働してリガンド-受容体蛋白複合体を自動構築出来ることを示した。
このRAR立体構造モデルによりAm80のサブタイプ選択性も説明できる、RAR 、
、 では272番アミノ酸がイソロイシンであるものがRAR
では272番アミノ酸がイソロイシンであるものがRAR ではメチオニンでおるため硫黄原子がAm80のアミド窒素と引き合うので結合位置にズレが生じて複合体形成に必要なdipoleの相互作用系が成立しない、このためAm80はRAR
ではメチオニンでおるため硫黄原子がAm80のアミド窒素と引き合うので結合位置にズレが生じて複合体形成に必要なdipoleの相互作用系が成立しない、このためAm80はRAR に結合しないと考えられる。
に結合しないと考えられる。