| 内容要旨 | | 1.はじめに 被子植物の精細胞は,花粉または花粉管の中にそれぞれ二個ずつ形成される.一方が卵と,もう一方が中心細胞と融合し,重複受精が行われる(図1A).多くの植物でこの精細胞のペアは非常によく似ていてほとんど区別がつかない.しかし,イソマツ科のインドマツリ(Piumbagozeylanica)のように,中に含まれるオルガネラの違いによって明瞭に区別のつく精細胞をつくる植物も存在する.この植物を用いて花粉管内で後ろ側に位置する精細胞(Sua)が卵と,前側に位置する精細胞(Svn)が中心細胞と選択的に融合することが示され(図1B.Russell1980,1985),二個の精細胞の融合する相手は予め決定していることが提唱された.しかし,このことはP.zeylanica以外の植物では厳密に確認されたことがなく,被子植物に広く一般的であるかどうかは明らかでない.精細胞は5〜20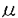 mと小さく細胞質に乏しいので,その差異を見るには電子顕微鏡観察に依存せざるを得ない.それゆえ多くの植物を用いて探索・検証ができなかったことが原因と考えられる. mと小さく細胞質に乏しいので,その差異を見るには電子顕微鏡観察に依存せざるを得ない.それゆえ多くの植物を用いて探索・検証ができなかったことが原因と考えられる. 本研究では,精細胞のペアおよび雄原細胞の両極での細胞質の差異を検出するために,オルガネラDNAを可視化する簡便な方法を開発し,100種以上の植物を対象に探索を試みた.その結果見出された植物について,雄性配偶子形成過程を詳細に追跡し,複数の植物において二個の精細胞間の細胞分化あるいはその前兆となりうる雄原細胞内の極性を見出した. 2.結果と考察(1)成熟花粉内の精細胞間あるいは雄原細胞の両極においてオルガネラの分布に偏りがある植物の探索1)固定法の検討 まず,精細胞及び雄原細胞(以下生殖系列の細胞)内のオルガネラDNAを蛍光顕微鏡により可視化する方法について検討した.これまで,細胞質遺伝様式を調べるために行われた押しつぶし法による観察では,カルノア固定(Corriview and Coleman1988)あるいはグルタールアルデヒド固定(Miyamura et al.1987,Nagata et al.1997)が主に用いられてきた.両者を比較したところ,オルガネラDNAの輝点が明るく形態も保持したまま可視化できる点で後者が優れていた(図2).更に条件を検討した結果,グリセロール,褪色防止剤入りのバッファー内で0.7%グルタールアルデヒドによる固定が,生殖系列の細胞の損傷も少なくオルガネラの染色性も良いので以後これを用いることにした. 2)探索結果 56科102属114種の植物について,上記の方法で観察を行い,精細胞間で,あるいは雄原細胞の両極で,オルガネラDNAが不均等に分布する(以下オルガネラDNAの偏在)ものを探索した(表1).その結果,三細胞性花粉の精細胞間でオルガネラDNAの偏在があるものが4種(新規には2種),二細胞性花粉の雄原細胞内にオルガネラDNAの偏在が生じているものが4種見出された(表2,図3,4). (2)オルガネラDNAの偏在に関する偏りの強さの評価 生殖系列の細胞でオルガネラDNAの偏在が見られたもの中には,花粉を同一の植物体の同一の花からサンプリングした場合でも,その偏在にばらつきがあるものがあった.そこで,その偏りの強さを数量的に評価した. 1)押しつぶし法によるオルガネラDNAの偏在の評価 二細胞性花粉の雄原細胞内でオルガネラDNAの偏在が見られるもののうち,ノウゼンカズラ(Campsis grandiflora),アメリカデイゴ(Erythrina crista-galli)を用い,オルガネラDNAの輝点の多い方を横軸,少ない方を縦軸にとってブロットし,偏在のないツツジ(Rhododendron maximum)と比較した(図5).三細胞性花粉では,栄養核とSvnの連結が既に確立しているスターチス(Limonium sinuatum),ルリマツリ(Plumbago auriculata)を用い,Suaでの輝点の個数を横軸,Svnでの輝点の個数を縦軸にとって,偏在のないゼラニウム(Pelargonium zonale)と比較した(図6).その結果,オルガネラDNAの偏在様式には,二細胞性,三細胞性花粉のいずれでも,花粉によってオルガネラDNAの偏りがあるものとないものが混在するパターン(以下"弱い偏在")と,全ての花粉で片方に極端に偏るパターン(以下"強い偏在")があることがわかった. 2)共焦点レーザー顕微鏡観察によるオルガネラDNAの偏在の評価 "弱い偏在"を示す植物(ノウゼンカズラ,スターチス)は,いずれもミトコンドリアと色素体のDNAを識別できないまま計数したので両方を独立に評価できない.そこで,テクノビット7100切片の同視野を蛍光顕微鏡と電子顕微鏡で観察して各オルガネラを輝点の形態によって区別し,大型の輝点が色素体のものであることを両方の植物で確かめた(図7).そして,5〜12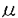 mのテクノビット7100切片を共焦点レーザー顕微鏡で光学切片化し両オルガネラを区別しながら観察し(図8),各オルガネラDNAの分布を独立にブロットした(図9).その結果,ノウゼンカズラ,スターチスは,ツツジやゼラニウムと比べ,生殖系列の細胞内で両オルガネラDNAとも,偏りにばらつきが大きいことがわかった. mのテクノビット7100切片を共焦点レーザー顕微鏡で光学切片化し両オルガネラを区別しながら観察し(図8),各オルガネラDNAの分布を独立にブロットした(図9).その結果,ノウゼンカズラ,スターチスは,ツツジやゼラニウムと比べ,生殖系列の細胞内で両オルガネラDNAとも,偏りにばらつきが大きいことがわかった. 3)オルガネラDNAの"弱い偏在"の生物学的意義 オルガネラDNAの偏在がある植物は,生殖系列の細胞にオルガネラDNAが残る植物と同様,系統関係の中で散発的に現れ,同じ科・属内でも異なる場合があることから,科の分岐以降に現れたものと考えられる.また,同一種の同じ個体由来の細胞で偏りの程度にばらつきがあることからも,進化の中間段階と位置づけられることが示唆される.生殖系列の細胞にオルガネラDNAが残るように進化した植物のうち,融合する相手にオルガネラDNAが伝達されることが有利または不利に働く選択圧によって,オルガネラDNAを不均等に分配するような分化が起こったものと考えられる.その中で,特にそのことが有利に働く植物では,全ての花粉でオルガネラDNAが極端に偏った雄原細胞や精細胞のペアを形成すると考察される. (3)雄原細胞内の極性の形成過程1)雄原細胞内での極性の形成時期と偏在の強さ オルガネラDNAの偏在があるものについて,その形成過程を追跡し,偏在の開始時期をテクノビット7100切片観察により調べた."弱い偏在"を示すもの(ノウゼンカズラ,スターチス)では雄原細胞が栄養細胞内に遊離し,紡錘形になる頃になって偏在が生じた(図10,11)."強い偏在"を示すもの(アメリカデイゴ,ルリマツリ)では,雄原細胞が栄養細胞内に遊離する時点では既に偏在が起こっていた(図12,13).以上の結果から,雄原細胞が形成されてから早い段階でオルガネラの偏在が起こるものは"強い偏在"を示し,遅い段階になって偏在が起こるものに関しては"弱い偏在"しか示さないことがわかった(図17). 2)色素体の挙動を支配する分子機構 オルガネラの偏在がどのような分子機構と関連しているのかを調べるため,生殖系列の細胞でのオルガネラの挙動が最も顕著なルリマツリを用いて細胞生理学的実験を行った.まず,テクノビット7100の連続切片から得られたプロファイルを立体構築することで,各オルガネラの挙動を三次元的に詳細に記述した(図14).識別の容易さから色素体に注目したところ,色素体が顕著な局在様式を示すのは,小胞子の前期,雄原細胞の中期,雄原細胞の後期の3つのステージであることがわかった.その挙動を支配している分子機構の手がかりを得るために,花粉を阻害剤で処理することにより色素体の挙動に対する効果を検討した.微小管破壊剤のアミプロホスメチル処理(1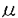 g/ml,1hr)が,前期の小胞子における色素体の挙動を撹乱することがわかった(図15).ところが,同様の処理条件でも雄原細胞の中期や後期では色素体の挙動に顕著な変化は見られず,濃度を1000倍にしても効果がなかった(図16).これらのことから,雄性配偶子形成過程におけるオルガネラの挙動は,小胞子の前期では微小管に依存的であるが,花粉第一分裂以降では別の分子機構に転換する可能性が示唆された. g/ml,1hr)が,前期の小胞子における色素体の挙動を撹乱することがわかった(図15).ところが,同様の処理条件でも雄原細胞の中期や後期では色素体の挙動に顕著な変化は見られず,濃度を1000倍にしても効果がなかった(図16).これらのことから,雄性配偶子形成過程におけるオルガネラの挙動は,小胞子の前期では微小管に依存的であるが,花粉第一分裂以降では別の分子機構に転換する可能性が示唆された. 3.まとめ (1)生殖系列の細胞への損傷を最小限に抑えつつ内部のオルガネラDNAを可視化する方法を開発し,計114種の植物を用いて観察した結果,精細胞間あるいは雄原細胞の両極で,DNAを含むオルガネラが偏在する植物を見出した.そのような植物は,系統関係の中で散発的に現れ,ノウゼンカズラ属,マメ科,イソマツ科の分岐の後に生じたものと予想された. (2)オルガネラDNAの偏りの強さを評価したところ,同一個体から得られた花粉でも極端に偏在するものと均等に存在するものが混じる"弱い偏在"を示す植物と,全て極端に偏在する"強い偏在"を示す植物があることがわかった.偏在の仕方にばらつきの大きい"弱い偏在"という中間的段階もあることからも,進化の途中の段階と位置づけられる.また,従来同形だと結論されていた植物でも,多くの精細胞のペアを観察すれば,その間の差異を見出せる可能性があることが示唆された. (3)オルガネラDNAの偏在の形成機構を調べたところ,雄原細胞形成後の早い段階でオルガネラDNAの偏在が起こるものほど"強い偏在"を示すことがわかった.色素体の挙動は小胞子の前期では微小管に依存的であることがわかった.  図1 被子植物の重複受精二つの精細胞は花粉管によって運搬されて胚のうに至り,片方が卵と、もう一方が中心細胞と融合する.多くの植物では二つの精細胞のペアの区別がつかないため,融合する相手が決まっているのかどうか検証できない.イソマツ科のインドマツリ(Plumbago zeylanica)においてのみ,Suaが卵とSvnが中心細胞と選択的に融合することが確かめられている. 図1 被子植物の重複受精二つの精細胞は花粉管によって運搬されて胚のうに至り,片方が卵と、もう一方が中心細胞と融合する.多くの植物では二つの精細胞のペアの区別がつかないため,融合する相手が決まっているのかどうか検証できない.イソマツ科のインドマツリ(Plumbago zeylanica)においてのみ,Suaが卵とSvnが中心細胞と選択的に融合することが確かめられている. 図2 雄原細胞/精細胞(生殖系列の細胞)内のオルガネラDNAの観察法の改良カルノア固定法後70%EtOHで浸漬する固定(A)と,0.7%グルタールアルデヒドによる固定(B)で,DAM染色して蛍光顕微鏡観察をしたゼラニウム(Pelargonium zonale)の精細胞. 図2 雄原細胞/精細胞(生殖系列の細胞)内のオルガネラDNAの観察法の改良カルノア固定法後70%EtOHで浸漬する固定(A)と,0.7%グルタールアルデヒドによる固定(B)で,DAM染色して蛍光顕微鏡観察をしたゼラニウム(Pelargonium zonale)の精細胞. 図3 2細胞性花粉の雄原細胞におけるオルガネラDNAの偏在DAPl染色して蛍光顕微鏡観察した. ノウゼンカズラ(Campsis grandiflora, A,B). ヒメノウゼンカズラ(Campsis xp, C,D). デイゴ(Erythrina variegata, E,F). アメリカデイゴ(Erythrina crista-galli, G,H)の雄原細胞. 図3 2細胞性花粉の雄原細胞におけるオルガネラDNAの偏在DAPl染色して蛍光顕微鏡観察した. ノウゼンカズラ(Campsis grandiflora, A,B). ヒメノウゼンカズラ(Campsis xp, C,D). デイゴ(Erythrina variegata, E,F). アメリカデイゴ(Erythrina crista-galli, G,H)の雄原細胞. 図4 三細胞性花粉の精細胞のペアにおけるオルガネラDNAの偏在DAPl染色して蛍光顕微鏡観察した,ハナゾノツクバネウツギ(Abeha spatulata, A,B). 図4 三細胞性花粉の精細胞のペアにおけるオルガネラDNAの偏在DAPl染色して蛍光顕微鏡観察した,ハナゾノツクバネウツギ(Abeha spatulata, A,B). 表1 生殖系列の細胞においてオルガネラDNAが偏在する植物の探索結果56科102属114種の植物の,開花時の花粉をDAPl染色して押しつぶし法で,蛍光顕微鏡観察し,雄原細の両極,あるいは二〓の〓細〓のペアの間で,オルガネラDNAの偏在が見られるものを探索した. 表1 生殖系列の細胞においてオルガネラDNAが偏在する植物の探索結果56科102属114種の植物の,開花時の花粉をDAPl染色して押しつぶし法で,蛍光顕微鏡観察し,雄原細の両極,あるいは二〓の〓細〓のペアの間で,オルガネラDNAの偏在が見られるものを探索した. 表2 探索結果のまとめ 表2 探索結果のまとめ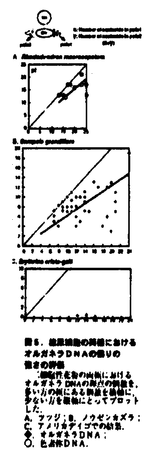 図5 雄原細胞の両極におけるオルガネラDNAの偏りの強さの評価二細胞性花粉の両極におけるオルガネラDNAの輝点の個数を,多いほうの極にある個数を横軸に,少ないほうを縦軸にとってプロットした. 図5 雄原細胞の両極におけるオルガネラDNAの偏りの強さの評価二細胞性花粉の両極におけるオルガネラDNAの輝点の個数を,多いほうの極にある個数を横軸に,少ないほうを縦軸にとってプロットした. 図6 精細胞のペアにおけるオルガネラDNAの偏りの強さの評価三細胞性花粉の精細胞のペアにおけるオルガネラDNAの原点の個数を,Suaでの値を横軸に,Svnでの値を縦軸にとってプロットした. 図6 精細胞のペアにおけるオルガネラDNAの偏りの強さの評価三細胞性花粉の精細胞のペアにおけるオルガネラDNAの原点の個数を,Suaでの値を横軸に,Svnでの値を縦軸にとってプロットした. 図7 オルガネラDNAの輝点の識別テクノビット7100樹脂包埋した花粉を,厚さ〓00nmに薄切し,その同視野を蛍光顕微鏡と電子顕微鏡の両方で観察した. 図7 オルガネラDNAの輝点の識別テクノビット7100樹脂包埋した花粉を,厚さ〓00nmに薄切し,その同視野を蛍光顕微鏡と電子顕微鏡の両方で観察した. 図8 共焦点レーザー顕微鏡による光学切片観察生殖系列の細胞内でのオルガネラDNAの偏在を,両オルガネラを識別しながら観察するために,厚さ5-12 図8 共焦点レーザー顕微鏡による光学切片観察生殖系列の細胞内でのオルガネラDNAの偏在を,両オルガネラを識別しながら観察するために,厚さ5-12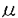 mのテクノビット7100樹脂切片をDNA特異的色素SYTOX Greenにより染色し,0.3 mのテクノビット7100樹脂切片をDNA特異的色素SYTOX Greenにより染色し,0.3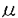 mの光学切片にして観察した. mの光学切片にして観察した. 図9 共焦点レーザー顕微鏡観察によるオルガネラDNA偏りの強さの評価ノウゼンカズラの雄原細胞(A)と,スターチスの精細胞のペア(B)において,色素体とミトコンドリアを区別して計数し,偏りの強さを評価した.ノウゼンカズラでは,色素体DNAの多い方の極の値を横軸に,色素体DNAの少ないほうの極の値を縦軸にとってプロットした.スターチスでは,Suaでの値を横軸に,Svnでの値を縦軸にとってプロットした. 図9 共焦点レーザー顕微鏡観察によるオルガネラDNA偏りの強さの評価ノウゼンカズラの雄原細胞(A)と,スターチスの精細胞のペア(B)において,色素体とミトコンドリアを区別して計数し,偏りの強さを評価した.ノウゼンカズラでは,色素体DNAの多い方の極の値を横軸に,色素体DNAの少ないほうの極の値を縦軸にとってプロットした.スターチスでは,Suaでの値を横軸に,Svnでの値を縦軸にとってプロットした. 図10.ノウゼンカズラの花粉形成過程におけるオルガネラDNAの偏在の開始時期花粉をテクノビット7100樹脂包埋し,0.6 図10.ノウゼンカズラの花粉形成過程におけるオルガネラDNAの偏在の開始時期花粉をテクノビット7100樹脂包埋し,0.6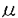 mの切片をDAPlとDiOC6で二重染色して蛍光顕微鏡観察した(図11-13:同様) mの切片をDAPlとDiOC6で二重染色して蛍光顕微鏡観察した(図11-13:同様) 図11.スターチスの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図11.スターチスの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図12.アメリカデイゴの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図12.アメリカデイゴの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図13.ルリマツリの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図13.ルリマツリの花粉形成過程におけるオルガネラDNAの偏在の開始時期 図14.ルリマツリの精細胞形成過程における各オルガネラの挙動の立体的記述40個以上のさまざまな長さのルリマツリの蕾から切り出した〓をテクノビット7100樹脂に包埋して,切片を観察し,そのうちオルガネラの局在パターンが顕著なステージについて0.7 図14.ルリマツリの精細胞形成過程における各オルガネラの挙動の立体的記述40個以上のさまざまな長さのルリマツリの蕾から切り出した〓をテクノビット7100樹脂に包埋して,切片を観察し,そのうちオルガネラの局在パターンが顕著なステージについて0.7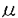 mの連続切片を作製した.それらをDAPlとDiCO6で二重染色した蛍光顕微鏡像から,細胞核,色素体,ミトコンドリア,液胞,細胞の境界のプロファイルをとり,ニコンCOSMO ZONE2S’を用いて立体構築した.色素体が顕著な局在様式を示す3つのステージ(A,C,D)と,花粉第一分裂直後(B),花粉第二分裂直後(C)の結果. mの連続切片を作製した.それらをDAPlとDiCO6で二重染色した蛍光顕微鏡像から,細胞核,色素体,ミトコンドリア,液胞,細胞の境界のプロファイルをとり,ニコンCOSMO ZONE2S’を用いて立体構築した.色素体が顕著な局在様式を示す3つのステージ(A,C,D)と,花粉第一分裂直後(B),花粉第二分裂直後(C)の結果. 図15.ルリマツリの小胞子の前期における色素体の挙動と微小管の関係前期の小胞子に対し,チューブリンの間接蛍光抗体染色を行ったときの,DAPl像(A,C,E)と,FITCで検出したシグナル(B,D,F).AとB,CとD,EとFはそれぞれ同視野.A,Bはホールマウント,C-Fはテクノビット7100切片(0.6 図15.ルリマツリの小胞子の前期における色素体の挙動と微小管の関係前期の小胞子に対し,チューブリンの間接蛍光抗体染色を行ったときの,DAPl像(A,C,E)と,FITCで検出したシグナル(B,D,F).AとB,CとD,EとFはそれぞれ同視野.A,Bはホールマウント,C-Fはテクノビット7100切片(0.6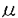 m)上での観察結果. m)上での観察結果. 図16.ルリマツリの雄原細胞の中期・後期での色素体の挙動に微小管破壊剤処理は効果がない中期,後期の雄原細胞に対し,アミプロホスメチル処理を行ったときの色素体の挙動を,DAPl染色したテクノビット7100切片(0.6 図16.ルリマツリの雄原細胞の中期・後期での色素体の挙動に微小管破壊剤処理は効果がない中期,後期の雄原細胞に対し,アミプロホスメチル処理を行ったときの色素体の挙動を,DAPl染色したテクノビット7100切片(0.6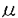 m)上で観察した. m)上で観察した. 図17.雄原細胞内での極性の形成時期とオルガネラDNAの偏在の強さ成熟花粉内の生殖系列の細胞にオルガネラDNAの偏在が生じている植物を見出し,二細胞性花粉,三細胞性花粉を生じるものの両方において,"弱い偏在"を示すもの(ノウゼンカズラ,スターチス)と"強い偏在"を示すもの(アメリカデイゴ,ルリマツリ)が存在することがわかった.その形成過程を追跡したところ,偏在の程度が強いものほど,精細胞形成過程の早い段階で,オルガネラの偏りが生じていることがわかった. 図17.雄原細胞内での極性の形成時期とオルガネラDNAの偏在の強さ成熟花粉内の生殖系列の細胞にオルガネラDNAの偏在が生じている植物を見出し,二細胞性花粉,三細胞性花粉を生じるものの両方において,"弱い偏在"を示すもの(ノウゼンカズラ,スターチス)と"強い偏在"を示すもの(アメリカデイゴ,ルリマツリ)が存在することがわかった.その形成過程を追跡したところ,偏在の程度が強いものほど,精細胞形成過程の早い段階で,オルガネラの偏りが生じていることがわかった. |
| 審査要旨 | | 本論文は4章からなり,第1章は,被子植物の精細胞間または雄原細胞の両極でオルガネラの分布に偏りがある植物の探索について,第2章は,オルガネラの偏在の強さの評価と種間比較について,第3章は,オルガネラの偏在の形成時期と偏在の強さに関する形態学的考察について,第4章は,ルリマツリ(Plumbago auriculata)の花粉形成過程で色素体の挙動を支配する分子機構の細胞生理学的考察について述べられている. 被子植物では,精細胞は花粉または花粉管のなかにそれぞれ二個ずつ形成され,一方は卵と融合して次世代の植物体を形成し,もう一方は中心細胞と融合して胚乳を形成する.大多数の植物で,この二個の精細胞のペアは非常によく似ていて,電子顕微鏡を用いても区別することが困難であった.しかし,イソマツ科のインドマツリ(Plumbago zeylanica)では,形態的に明瞭に区別のつく二個の精細胞が形成される.さらに,それぞれの精細胞の融合する相手が決定されていることが,唯一確かめられている.ところがこの植物は,受精の際重要な働きを担うと考えられる助細胞を欠く.そのため,この選択的な重複受精というのがルリマツリだけで起こる特殊な現象である可能性も否定できない.論文提出者はこうした背景から,簡便な方法で多くの植物の精細胞あるいはその前駆細胞である雄原細胞を観察し,精細胞の二型性やひいては選択的重複受精が,被子植物で広く一般的に起こる現象なのかを明らかにし,またその二型性の形成過程を詳細に観察し,その機構を明らかにするために研究を行った. 第1章では,精細胞及び雄原細胞(以下生殖系列の細胞)内のオルガネラDNAを蛍光顕微鏡により可視化する方法の改良を行った.その方法を用いて,56科102属114種の植物について観察を行い,精細胞間で,あるいは雄原細胞の両極で,オルガネラが不均等に分布(以下オルガネラの偏在)するものを探索した.その結果,生殖系列の細胞にオルガネラDNAが残存する31種のうち,三細胞性花粉の精細胞間でオルガネラの偏在があるものが4種(新規には2種),二細胞性花粉の雄原細胞内に偏在があるものが4種見出された. オルガネラの偏在がある植物の中には,同一の植物体の同一の花から採取した場合でも,偏在の度合いにばらつきがあるものがあった.そこで,第2章では,その偏りの強さを数量的に評価し種間で比較した.その結果,オルガネラの偏在が全ての花粉で起こっている,"強い偏在"を示すものと,オルガネラの偏在が花粉によってばらつきがある,"弱い偏在"を示すものがあることがわかった.これらは,二細胞性花粉,三細胞性花粉の両方で見出され,合計4種のカテゴリーに分けられることがわかった. 第3章ではDNAを含むオルガネラの偏在の開始時期を,テクノビット7100樹脂包埋法で観察し種間で比較した.その結果,雄原細胞が形成されてから早い段階でオルガネラの偏在が起こるものは,"強い偏在"を示し,遅い段階になってから偏在が起こるものは,"弱い偏在"を示すことがわかった. 第4章では,オルガネラの偏在がどのような分子機構と関連しているのかを調べるため,生殖系列の細胞でのオルガネラの挙動が最も顕著なルリマツリ(Plumbago auriculata)を用いて,細胞生理学的実験を行った.まずそれぞれのオルガネラを識別しながらその挙動を立体的に詳細に記述した.色素体に注目したところ,顕著な局在様式を示すのは,小胞子の前期,雄原細胞の中期,雄原細胞の後期の3つであることがわかった.阻害剤処理により,これらのステージの色素体の挙動に対する効果を調べた.その結果,小胞子の前期では,色素体の挙動は微小管に依存的であるが,花粉第一分裂以降では別の分子機構の関与が示唆された. 論文提出者は,改良した高感度の方法で検出することによって,被子植物において二型性を示す精細胞は,従来の認識よりも多くの植物で見られることを示し,また,同一の花で形成された花粉でも,その中の一部では明瞭な差が生じている集団が含まれていることを,初めて明らかにした.さらに,そのようなオルガネラを目印にして,精細胞の二型性が生じる機構を詳細な観察と細胞生理学的手法で考察した. なお,本論文第一章と第二章は,藤江誠,酒井敦,永田典子,松永幸大,森君江,黒岩晴子,黒岩常祥と,第三章は,永田典子,酒井敦,森君江,黒岩晴子,黒岩常祥と,第4章は永田典子,酒井敦,黒岩晴子,黒岩常祥との共同研究であるが,論文提出者が主体となって分析と検証を行ったもので,論文提出者の寄与が十分であると判断する.したがって,博士(理学)の学位を授与できると認める. |