本研究は自己免疫病の代表的な動物モデルである実験的自己免疫性脳脊髄炎(EAE)において、NK細胞が、EAEを抑制的に調節することを証明するため、雌C57BL/6J(B6)マウスおよびB6バックグランドのNK-T細胞欠損マウスにミエリン・オリゴデンドロサイト・グリコプロテイン(MOG)の35-55残基に相当する合成ペプチドを用いて、EAEの誘導を試みた。EAEの免疫調節におけるNK細胞の役割の解析を試みたものであり、下記の結果を得ている。 1.対照のB6マウスではactive EAEの臨床症状は単相性で、きわめてmildであった。一方NK1.1抗体であらかじめNK1.1陽性細胞を除いたマウスでは、約1週間続く1st episodeから約1週間の間隔をおいてより重篤な2nd episodeがみられた。 2.NK-T細胞を欠損する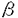 2-microglobulinノックアウトマウス(B6 background)を用いてEAEの誘導実験を行った。対照ではきわめてmildな単相性のEAEが観察されたが、NK-Tノックアウトマウスではwild type B6マウスと同様の発症がみられた。一方抗NK1.1抗体投与を受けたマウスは致死性EAEを発現した。この結果は、NK細胞がNK-T細胞やCD8T細胞に依存することなく、調節機能を発揮することを意味している。 2-microglobulinノックアウトマウス(B6 background)を用いてEAEの誘導実験を行った。対照ではきわめてmildな単相性のEAEが観察されたが、NK-Tノックアウトマウスではwild type B6マウスと同様の発症がみられた。一方抗NK1.1抗体投与を受けたマウスは致死性EAEを発現した。この結果は、NK細胞がNK-T細胞やCD8T細胞に依存することなく、調節機能を発揮することを意味している。 3.passive EAEにおいても、抗NK1.1抗体投与により臨床症状の顕在化がみられた。対照抗体、または抗NK1.1抗体を静脈内投与したB6マウスにMOG35-55特異的T細胞株を3x106個尾静脈より移入した。実験では対照群にはEAEは誘導されなかったが、抗NK1.1抗体を注射した群では明らかなEAEの発症を認めた。さらにT細胞、B細胞、NK-T細胞を欠損するRAG-2ノックアウト・マウスを使って同じ実験を行った。対照群に比べてNK1.1抗体を投与したマウスでは、EAE症状の発現が強く、マウスはすべて死亡した。この結果は、passive EAEにおいてNK細胞はT細胞、B細胞やNK-T細胞に依存せず独立した調節細胞として機能することを意味している。つぎにNK細胞の免疫調節作用をより直接的に証明するために、NK細胞の移入による治療効果を検討した。抗NK1.1抗体を注射したRAG-2ノックアウト・マウスに無処置RAG-2ノックアウト・マウスの脾臓細胞を移入してから、MOG35-55特異的T cell lineを移入する実験を行った。NK細胞をreconstituteされた群では、EAEは完全に抑制された。このことは、NK細胞の移入によりEAEが抑制されることを意味している。 以上、本論文はNK1.1抗原を発現する細胞が自己免疫病の調節性細胞として働くことを示している。さらにCD1分子を欠損し、CD1依存性のNK-T細胞を欠損する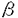 2-microglobulin欠損マウスにおいても抗NK1.1抗体の効果がみられたことから、NK細胞単独でも充分な免疫調節機能のあることを証明した。本研究はこれまで自己免疫病において、ほとんど焦点の当てられていなかったNK細胞が、多発性硬化症などの自己免疫疾病で、想像以上に大きい役割を果している可能性を示したものである。自己免疫病の病因解明に重要な貢献をなすと考えられ、学位の授与に値するものと考えられる。 2-microglobulin欠損マウスにおいても抗NK1.1抗体の効果がみられたことから、NK細胞単独でも充分な免疫調節機能のあることを証明した。本研究はこれまで自己免疫病において、ほとんど焦点の当てられていなかったNK細胞が、多発性硬化症などの自己免疫疾病で、想像以上に大きい役割を果している可能性を示したものである。自己免疫病の病因解明に重要な貢献をなすと考えられ、学位の授与に値するものと考えられる。 |