| 内容要旨 | | 腎臓の急性尿細管壊死は尿細管の閉塞,放射線,薬剤処理以外に虚血再灌流,低酸素,腎動脈の狭窄により引き起こされる。その中でも虚血再灌流は移植腎における,急性の腎機能低下の主要な機序と考えられ,その病態の解明は重要な課題となっている。この尿細管細胞の障害が進行する過程で尿細管細胞にアポトーシスが起こっていることが指摘されている。Nogaeらは虚血再灌流マウス腎臓での遠位尿細管にFasが発現し,このFasの発現が尿細管のアポトーシスの誘導に深い関連があることを示した。今回の研究の目的は,1.形態学的な観察やDNAのラダーパターンの確認によって虚血再灌流腎で尿細管にアポトーシスが起こっていることを証明し,アポトーシス細胞の局在をTUNEL法を用いることにより検討する。2.様々な再灌流時間で検体を採取し,免疫染色,western blot分析,Northern blot分析などの手法を用いてFas及びFasLの関与を時間的,局在的に検討する。3.in situ hybridizationの手法を用いて,Fas,FasLがmRNAレベルで発現している細胞を検討する。4.マウス虚血再灌流モデルにおいてFas系列をブロックすることにより腎尿細管細胞へのアポトーシスの誘導を抑制出来るかを検討することである。今回の研究は虚血再灌流時のアポトーシスにFas-FasL系が関与していることを示すだけではなく,Fas-FasLのブロック実験により,虚血再灌流時の腎組織障害を軽減するための新しいアプローチを切り開く可能性を示唆するものと思われる。 研究方法1.動物モデルの作成 7週令のオスのICRマウスの左腎動静脈に1時間の虚血を行った後,再灌流を施行し,定期的な時間間隔をおいて(0,6,12,24,36,48時間),腎臓を摘出し検討を行った。 Fasの中和抗体によるブロック実験 左腎動静脈を前記と同様にクランプした後,抗Fas血清を100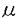 lを再灌流6時間の時点でマウスの腹腔内に注入した。同量の正常ウサギ血清をコントロールのマウスに注入した。それぞれの群のマウスから再灌流24時間で腎臓を摘出しアポトーシスの評価を行った。 lを再灌流6時間の時点でマウスの腹腔内に注入した。同量の正常ウサギ血清をコントロールのマウスに注入した。それぞれの群のマウスから再灌流24時間で腎臓を摘出しアポトーシスの評価を行った。 2.アポトーシスの同定と評価法 a)DNAの電気泳動;検体からDNAを抽出しアガロースゲルで電気泳動し観察した。 b)TUNEL染色;検体をパラフィン包埋、薄切切片を作成した。検体中のDNA断端にbiotin-16-dUTPをterminal transferaseの活性により付加し,biotin標識を免組織学的に発色を行った。 c)形態学的観察;検体を電検樹脂に包埋後,超薄切切片を作成し,トルイジンブルー染色を行い観察を行った。 3.Fas及びFasLの発現の検討a)mRNAレベルの発現の検討 Northern blot分析 検体から抽出したtotal RNAを通常の方法で32Pにて標識したFas,FasLのcDNAプローブを用いてNorthern blot分析を施行した。 in situ hybridization T-Tダイマー化したFasあるいはFasLのoligoprobeを用いてnon-Rlのin situ hybridizationを行った。 b)蛋白レベルの発現の検討 Western blot分析 検体からを抽出した蛋白を抗Fas血清,抗FasL血清を用いてWestern blot分析を行った。 免疫染色 パラフィン切片を,一次抗体(抗Fas血清,抗FasL血清),二次抗体としてHRP標識したヤギ抗ウサギIgGF(ab’)2を用いて免疫組織学的に検討した。 実験結果1)虚血再灌流マウス腎臓でのアポトーシス DNAラダーパターンが観察され,その強度は再灌流時間が伸びるに従って増強し,再灌流24時間の時点でピークが見られた。TUNEL染色の結果,再灌流12時間の時点では皮質部分の遠位尿細管にTUNEL陽性細胞が豊富に見られた。再灌流24時間の時点ではouter medullaの部分の遠位尿細管に豊富にTUNEL陽性細胞が見られた。TUNEL陽性細胞の定量的な分析結果,TUNEL陽性細胞は主に遠位尿細管に見られ,その数のピークは再灌流12時間に見られた(下図参考)。 腎臓の形態学的観察では,遠位尿細管には核のクロマチンの凝集と細胞質の萎縮を伴ったアポトーシス細胞の存在が確認され,近位尿細管には細胞質の空胞変性を伴ったネクローシス細胞が多く観察された。 2)FasとFasLのmRNAの発現 Norhtern blot分析により,FasのmRNAの量は再灌流6〜24時間の時間帯で著明に増加が見られ,その後減少が見られた。FasL mRNAの発現は再灌流時間が伸びるに従って増強し,ほぼ再灌流6時間の時点でプラトーに達し,その後再灌流36時間の時点で急激に減弱していた。in situ hybridizationによりFas mRNAとFasL mRNAの発現は再灌流6-24時間の腎臓の皮質及びouter medullaの遠位尿細管細胞に見られた。Fas mRNAの発現はouter medullaの遠位尿細管により強く見られ,FasL mRNAの発現は皮質部分の遠位尿細管に強く発現が見られた。 3)FasとFasLの蛋白レベルの発現 Western blotによる解析によりFasは45kDaのFasLは31kDaにそれぞれのbandを形成し,それぞれの発現量は再灌流時間が延長するにしたがって増強し,再灌流12時間の時点でプラトーに達した。免疫染色の結果Fasは再灌流12時間の皮質部分の遠位尿細管に発現が見られるようになり,その後outer medullaの遠位尿細管に有意に陽性となっていた。一方FasLは再灌流6〜24時間の皮質部の遠位尿細管に有意に発現が見られた。 4)Fasに対する中和抗体によるブロック実験 抗P2血清はマウスFasの細胞外の部位に対して作成した血清で,抗P2血清を投与した群のDNAラダーパターンはほぼ完全に消失し,TUNEL陽性細胞の数も有意に減少が見られた。 考察 アポトーシスの研究での最も興味深い面は,アポトーシスが特異的な遺伝子の発現を含めた能動的な過程であるため,外部から故意に制御可能である点である。今回の研究によって,遠位尿細管のアポトーシスが虚血再灌流により誘導され,この過程がFas-FasL系列によって媒介されていることが示された。さらにこのアポトーシスの過程がin vivoにおいてFas,FasLの相互作用を抑えることで阻害することが出来た。今回の研究はin vivoにおいてアポトーシス細胞死を制御する一つの新しいアプローチを示したものと思われる。 今回の結果からouter medullaの部位の遠位尿細管で合成されたFasLは遊離型へと変換され,周囲のFas陽性の尿細管細胞のアポトーシスを誘導していると考えられた。その理由としては,膜結合型FasLは遊離型に変換されることが指摘されている。一方,in situ hybridizationによりFasL mRNAはouter rmedullaの部位の遠位尿細管に発現が見られているが,免疫染色にてはFasLの蛋白はouter rmedullaの遠位尿細管の発現は確認出来なかった。FasLの細胞外の部位ではなく,細胞質内の部位を認識している抗P5血清が,免疫染色において遊離型FasLを認識出来ないためであると考えられる。つまり,in situ hybridiaztionのみにて見られているouter medullaの部位のFasLの発現は遊離型のFasLを検出していると考えられ,このouter medullaに発現している遊離型のFasLが血流などの経路を経て周囲の遠位尿細管の細胞表面に発現しているFasに結合し,アポトーシスを誘導していると判断された。 虚血再灌流のストレスに対する遠位尿細管と近位尿細管の反応の違いは非常に明白に見られたが,その機序は現時点では十分に説明することが出来ないが,これまでの報告から,この相違はouter medullaの部位の血流の回復の遅れが原因であるとの報告と,ヘンレの太い上行脚と近位尿細管の間の低酸素による細胞障害ストレスに対する反応の相違が原因であるとの報告がある。 虚血再灌流の刺激がどのようにしてFasの発現の誘導するかは現時点では不明である。この問題を解決するためにも,虚血再灌流のストレスに対する尿細管セグメントごとの反応の相違を理解する上にも,Fas,FasLをコードする遺伝子の転写調節レベルでの研究が必要である。しかしながら,Fasをコードする遺伝子の転写レベルでの調節機構はIL-6の発現蛋白がFasをコードする遺伝子を刺激することが分かっている以外は全く理解されていない。 現在,臓器移植は治癒不可能な疾患の治療として有用な治療法であり,移植臓器の障害の軽減は様々な臨床分野で精力的に研究されている。移植腎の障害は,移植時の虚血再灌流による腎組織障害と,急性あるいは慢性の拒絶反応による障害である。最近の研究によりアポトーシスは虚血再灌流による腎臓の組織障害のみならず,急性の拒絶反応にも関連していることが指摘され,この過程でおいてもFas-FasL系の関与が示唆されている。抗Fas血清投与によるアポトーシスの抑制は,虚血再灌流のみならず,拒絶反応においても,将来的に腎移植時に見られる腎組織障害を減弱させる一つの新しい手法となり得ると思われる。 結論 虚血再灌流により生じる遠位尿細管のアポトーシスはFas/FasL系により誘導されていることが示され,これを選択的に抑制する方法としてFasに対する中和抗体の投与による療法を提示し,その効果を報告した。 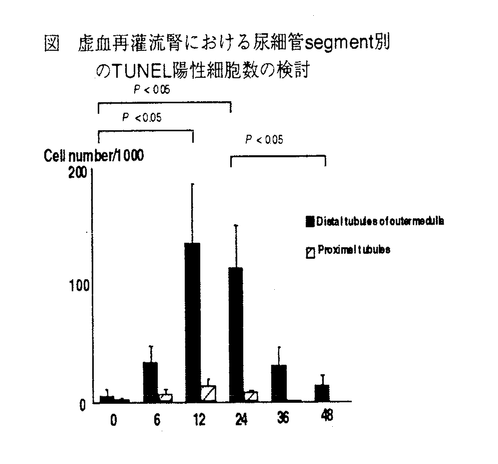 図 虚血再灌流腎における尿細管segment別のTUNEL陽性細胞数の検討 図 虚血再灌流腎における尿細管segment別のTUNEL陽性細胞数の検討 |