強力な発癌プロモーターである12-O-tetradecanoylphorbol-13-acetate(TPA)は細胞の増殖、分化に特徴的に作用する生理活性物質であり、その作用機序の解明は発癌のみならず生命現象の理解に大いに有用である。TPAタイプ発癌プロモーターであるteleocidin B-4はTPAと同等の活性を示し、官能基も少なくより単純な構造であることから活性発現に必須な共通要素の探索の上で有利な化合物である。テレオシジン類は室温でアミドがシスのtwistとトランスのsofaの2種のコンフォメーションをとっており、活性発現に必須な共通要素の特定が困難であったが、当教室でデザイン、合成されたテレオシジンのtwist型mimicであるbenzolactam(BL)V8-310(1)がテレオシジンの高い活性を再現し、活性発現に関与する極性官能基の立体配位について新たな知見をもたらした。  一方、疎水性側鎖も活性に非常に大きな影響を及ぼす。TPAの長鎖エステルの欠如した母核のホルボールには発癌プロモーション活性が全くなくなってしまい、またBL類においても側鎖を持たない母核のBL-V8(2)の活性は低く、アルキル基を有する1が種々のアッセイ系において約300倍もの活性の上昇を示したことからも、疎水性基が活性に決定的な役割を果たしていることが明らかである。薬物による活性発現を考える際、水素結合等の親水性相互作用だけでなく疎水性相互作用による受容体の結合における安定化も含めた総合的評価が必要であると考え、私は側鎖部の異なるBL類を合成し、TPAタイプ発癌プロモーションの初期過程とされているprotein kinasc Cへの結合と、生物活性は培養細胞の分化作用としてのHL60細胞の増殖抑制の系で評価を行い、得られた結果から系による疎水性基の異なる効果を見出した。さらに遺伝子転写段階での作用を評価しうる新しい評価系を構築し、TPAタイプ発癌プロモーターの活性発現機構の新たな側面を見出したので以下報告する。 9位疎水基体の合成 まずBL9位に種々側鎖を持つ化合物を検討することとした。合成スキームを示す。4-Methyl-3-nitroanilineを出発原料とし、Sandmeyer反応によるBr化、ラジカル的Br化の後マロン酸とのカップリングにより3を得た。続いて3を脱炭酸、保護基の付け替え、還元により4を得た。4に対し、別途D-valineより導いた(R)-triflate(5)を反応させて得た閉環前駆体(6)を活性エステル法により閉環、N-メチル化して7を得た。中間体7に対して末端アルキンとのHeck反応、還元により直鎖アルキル基を、シクロアルケンから環状アルキル基を導入した。アダマンチルメチル基はメチレンアダマンタンから、エステル体はプロパルギルアルコールとのHeck反応、還元の後エステル化を行うことにより得た。 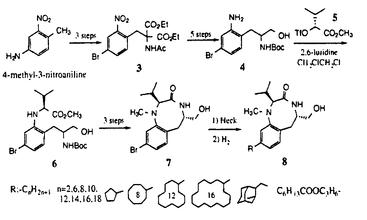 生物活性 合成した化合物についてヒト急性前骨髄球性白血病細胞株HL60を用いた増殖抑制により活性評価を行った。直鎖アルキル体はHL60の系においては炭素数の増加に従って活性は上昇し、炭素数12で活性は最大となり、さらに伸ばしていくと活性は徐々に減少していく。一方、発癌プロモーターの標的蛋白の一つであるprotein kinase C(PKC)結合能は、炭素数6〜14の間では活性に差はほとんど見られず、PKCに結合する際の疎水性側鎖部の構造的認識の甘いことが示唆される。しかしその前後で結合能は顕著に減少し、特に炭素数16及び18ではほぼ完全に消失することは特徴的である。シクロアルキル基ではHL60系で炭素数16まで活性は大幅に上昇した。かさだかいアダマンチルメチル基でも活性は上昇するが、これらは同炭素数の直鎖アルキル基と比較すると活性がやや低下し、疎水性基が固まった形よりも伸びた形状をとるほうが活性発現に有利であることが理解できる。これらの環状疎水性基を持つものでもPKC結合能は、HL60での活性とは異なり、ほぼ同等の活性を示した。またこれらは直鎖アルキル基と差がなく、一定範囲の疎水性基であれば活性にほとんど影響を及ぼさない。親水性官能基であるエステルを導入すると同じ長さの疎水性基に比べ、HL60系でもPKC結合能も約1/10に低下した。  BL類の活性発現に要求される疎水性領域は、テレオシジン類の構造活性相関から類推してBL2位から9位に渡る範囲に及ぶと推測される。2位から炭素数10の疎水基を持つBLC10は1に比べてHL60系で活性が約1/10に減少はするが、2位イソプロピル体(2)に比べ約30倍と十分な活性を保持している。そこで2位に疎水性基として直鎖アルキル基、分岐アルキル基、環状アルキル基を持つBL類について検討を行った。  合成 母核はL-phenylalaninolを出発原料とし、3stepでニトロベンゼン誘導体(9)に導いた。アミノ基の保護を付け替えた後、接触還元によりアニリン体(10)とした。またこれをN-ホルミル化後還元してN-メチルアニリン体(11)とした。直鎖アルキル体は11と別途合成したトリフレート(12)をカップリングさせ、上記の方法により閉環し目的化合物(16)を得た。分岐、環状アルキル体は11と12のカップリングが困難であったため、10と12をカップリングし、閉環した後N-メチル化することにより目的化合物(16)へ導いた。  生物活性 2位疎水基体も9位疎水基体と同様にHL60系では炭素数に従って順次活性が変化し、直鎖アルキルでは炭素数14で最大となる。PKC結合能はC8からC14まで結合活性に変化は少なく、それ以上に伸ばすとやはり結合能は著しく減少し、この化合物群においても疎水性基は異によって異なる役割を持つことが示唆された。また、これらの化合物はHL60系での活性に比べPKC結合能が強く、特にC66はHL60系では1の1/10の活性なのに対しPKC結合能は1より強いものであった。ここで得られた結果からも、細胞で見られる生物作用がPKCに必ずしも依存しているわけではないことが示唆される。ここに合成した強い活性を示す化合物はTPAやテレオシジンとともにPKCに結合するものの、HL60細胞分化、増殖への効果はそれによっては説明できない。  核内レセプターと発癌プロモーター 発癌プロモーターがリガンドである可能性を考え、リガンド未知の核内受容体のリガンド探索の一環として、ROR(RAR-related orphan receptor)及び応答遺伝子として3コビーのROR応答配列(RORE)をチミジンキナーゼ(TK)プロモーター.ルシフェラーゼ遺伝子の上流に組み込んだ(RORE)3TKLUCをCOS-1細胞に一過性に発現させ、薬物の影響を検討する系を構築した。この評価系ではRORはリガンドが無い状態でも構成的に転写を活性化しているが、ここにTPAやBL類を添加したところ著しく転写活性が増強された。このTPA等の効果はROR非存在下でも起こるがROR存在でより明確になる。  図表 図表 この活性がTPAタイプ発癌プロモーターに一般に見られる現象であったことから、合成したBL類についてこの系にて活性評価を行った。  9位疎水基体、2位疎水基体ともPKC結合能よりもHL60系における結果とよく対応していた。行ってきた3種の活性評価についての相関図を下に示す。  図表 図表 左がHL60細胞増殖抑制能とPKC結合能の相関である。PKC結合能については10 MまでEC50に達しなかった化合物もあり、またそれを除いても相関はそれほど良くないものであった。それに対し、右のHL60細胞増殖抑制能とROR-TKプロモーターに対する転写活性化能はR=0.85とかなり良い相関を示している。また、右の図からそれぞれの系でのEC50の濃度領域がよく一致しているのも注目すべき点である。これまでの所、発癌プロモーターのプロモーション活性とHL60細胞増殖抑制能の間には良い相関が示されており、ROR-TKプロモーター系での活性評価は、発癌という遺伝子疾患における発癌プロモーターの遺伝子転写段階での作用を簡便に見ることができる点で有用な評価系であると考えている。 MまでEC50に達しなかった化合物もあり、またそれを除いても相関はそれほど良くないものであった。それに対し、右のHL60細胞増殖抑制能とROR-TKプロモーターに対する転写活性化能はR=0.85とかなり良い相関を示している。また、右の図からそれぞれの系でのEC50の濃度領域がよく一致しているのも注目すべき点である。これまでの所、発癌プロモーターのプロモーション活性とHL60細胞増殖抑制能の間には良い相関が示されており、ROR-TKプロモーター系での活性評価は、発癌という遺伝子疾患における発癌プロモーターの遺伝子転写段階での作用を簡便に見ることができる点で有用な評価系であると考えている。 ROR-TKプロモーター系でのTPAの作用機序の解析 TPAによる転写活性化の作用機序を検討することとした。まず、TPAの活性発現の初期過程とされているPKCの効果について、PKC阻害剤の与える影響を検討した。スタウロスポリン、H-7、カルフォスチンCといったPKC阻害剤と共存させると、H-7ではTPAによる増強が阻害されたが、スタウロスポリンにおいては逆にTPAの効果がさらに増強した。TPAの作用にPKC以外の経路の関与する可能性があることが伺われた。さらにTPAによる活性発現を担う転写因子とされているAP-1(Junホモダイマー、Jun/Fosヘテロダイマー)を発現させたところ、Jun、Jun/Fos導入によってもTPAの効果に何ら影響を与えなかったことからこのTPAの活性はAP-1以外の因子によるものであることが示唆された。  図表 図表 以上、私はBL類の疎水性基の活性に及ぼす影響を、3種の異なる系での活性評価により検討を行い以下の知見を得た。1)HL60系及びROR-TKプロモーター系においては、疎水性置換基の位置に関わらず活性が最大となる炭素数が存在し、その前後で活性は徐々に低下した。2)PKC結合能においては一定範囲内の長さの疎水性基では活性に差は見られず、それ以上になると活性は顕著に減少した。3)BL2位疎水基体はPKC結合能と比較して、HL60系及びROR-TKプロモーター系での活性が低かった。4)ROR-TKプロモーター系での結果はHL60系の結果との間に良い相関を示し、ROR-TKプロモター系がTPAタイプ発癌プロモーターの活性評価に有効であることが示された。 ROR-TKプロモーターに対する転写活性化の系でのTPAによる活性化は、その分子メカニズムは課題として残っているが、少なくともPKC及びAP-1に依存しない現象であるという部分において非常に興味深い結果であり、発癌プロモーターの活性発現機構の解明において新たな端緒をもたらすものと考えている。 |