| 内容要旨 | | 序論 パーキンソン病は黒質線条体ドーパミン神経系を中心とするモノアミン神経変性疾患であり、その発症原因は未だ不明である。ヒトに対するパーキンソニズム発症物質1-methyl-4-phenyl-1,2,3,6-tetrahydropyridine(MPTP)の発見以来、パーキンソン病の発症原因物質として様々な化合物が検索されている。我々は1,2,3,4-tetrahydroisoquinoline(TIQ)骨格を有する化合物群を内在性物質として動物の脳中より検索してきており、その内の数種がパーキンソン病の発症に関与している可能性を示唆しているが、単独で発症物質となり得るような化合物は見出されていない。現在のところ、未知の化合物も含めた多種類の内因性神経毒が協同的に作用してパーキンソン病の発症に関わっているという考え方が有力である。 新たなパーキンソン病関連TIQ類の探索を目的として、二つのTIQ誘導体、1-(3’,4’-dihydroxybenzyl)-1,2,3,4-tetrahydroisoquinoline(3’,4’DHBnTIQ)及び1-benzyl-6,7-dihydroxy-1,2,3,4-tetrahydroisoquinoline(6,7DHBnTIQ)を分子設計した(Fig.1)。この化合物は分子内にドーパミン構造を有しており、ドーパミン神経に強く作用することが期待される。本研究では、これらが、内在性パーキンソン病発症物質候補となり得るかどうか検討し、さらにその活性発現に関わる作用機構について検討した。 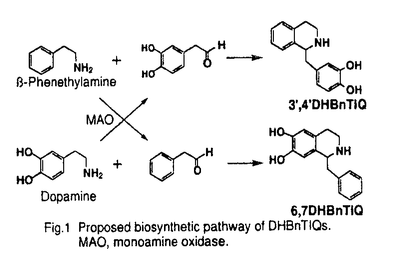 Fig.1 Proposed biosynthetic pathway of DHBnTIQs. MAO,monoamine oxidase. 1.DHBnTIQ類の内在性の検討 Fig.1 Proposed biosynthetic pathway of DHBnTIQs. MAO,monoamine oxidase. 1.DHBnTIQ類の内在性の検討 Fig.1に示すように、二つのDHBnTIQ類は -phenethylamineとdopamineが相手のMAO代謝物と縮合することにより生成すると考えられ、内在性物質であることが予想される。無水ヘプタフルオロ酪酸による誘導化、高分解能GC/SIM法によりマウス脳内からDHBnTIQ類の検出を試みた。Fig.2に示すように、m/z328.057、751.999のピークが合成標品と一致する保持時間に観察され、3’,4’DHBnTIQ、6,7DHBnTIQが内在性物質であることが示された。 -phenethylamineとdopamineが相手のMAO代謝物と縮合することにより生成すると考えられ、内在性物質であることが予想される。無水ヘプタフルオロ酪酸による誘導化、高分解能GC/SIM法によりマウス脳内からDHBnTIQ類の検出を試みた。Fig.2に示すように、m/z328.057、751.999のピークが合成標品と一致する保持時間に観察され、3’,4’DHBnTIQ、6,7DHBnTIQが内在性物質であることが示された。  Fig.2 High resoiution GC/SIM chromatogram of 3’,4’DHBnTIQ-triHFB (left) and 6,7DHBnTIQ-triHFB(right)。HFB;heptafluorobutyryl. 2.DHBnTIQ類の毒性の検討 Fig.2 High resoiution GC/SIM chromatogram of 3’,4’DHBnTIQ-triHFB (left) and 6,7DHBnTIQ-triHFB(right)。HFB;heptafluorobutyryl. 2.DHBnTIQ類の毒性の検討 DHBnTIQ類の細胞毒性、パーキンソニズム誘発活性を検討した。 中脳初代培養細胞を用いてDHBnTIQの細胞毒性を調べた。DHBnTIQを細胞に24時間暴露した後、MTT assayにより550nmの吸光度から細胞生存率を測定した。3’,4’DHBnTIQは濃度依存的な毒性を示し、100 M添加時に約80%生存率が減少した。6,7DHBnTIQは500 M添加時に約80%生存率が減少した。6,7DHBnTIQは500 Mでも毒性を示さなかった(Fig.3)。 Mでも毒性を示さなかった(Fig.3)。 各DHBnTIQをC57BLマウスに投与すると、急性的に自発的運動量の減少を引き起こした。次に、化合物を1日2回、5日間連続投与し、2日間休薬後ポールテスト、オープンフィールドテストを行ってパーキンソニズムの発現を検討した。ポールテストは、垂直に立てた棒の先端にマウスを上向きに掴まらせ、下を向くまでの時間(Tturn)、地面に到達するまでの時間(TLA)から寡動の発現を評価する行動薬理試験である。3’,4’DHBnTIQはポールテストにおいてTturn、TLAを延長させ、オープンフィールドテストにおいて自発的運動量を減少させた。これはパーキンソン病治療薬L-DOPAの投与により回復した。6,7DHBnTIQはいずれの試験においても対照群と差がなかった。 以上より、3’,4’DHBnTIQがパーキンソン病発症物質候補となり得ることが示唆される。  Table 1 Chronic effects of DHBnTIQs. 3.3’,4’DHBnTIQの代謝物の検索 Table 1 Chronic effects of DHBnTIQs. 3.3’,4’DHBnTIQの代謝物の検索 パーキンソニズム誘発物質MPTPは、1-methyl-4-phenylpyridinium(MPP+)に代謝されることで、より高活性になることが知られている。3’,4’DHBnTIQについて代謝活性化の可能性を検討する目的で、酸化体(1-(3’,4’-dihydroxybenzyl)-isoquinoline;3’,4’DHBnIQ)、N-メチル体(1-(3’,4’-dihydroxybenzyl)-2-methyl-1,2,3,4-tetrahydroisoquinoline;2Me3’,4’DHBnTIQ)、N-メチル酸化体(1-(3’,4’-dihydroxybenzyl)-2-methylisoquinolinium;2Me3’,4’DHBnIQ+)、3’-O-メチル体(1-(4’-hydroxy-3’-methoxybenzyl)-1,2,3,4-tetrahydroisoquinoline;3’,4’MHBnTIQ)への変換を検討した。In vivo、in vitroにおいて検索したところ、代謝物として3’,4’MHBnTIQのみが検出され、このO-メチル化はS3画分に存在するカテコール-O-メチルトランスフェラーゼ(COMT)によるものであることが明らかとなった。 3’,4’DHBnTIQ類縁化合物について中脳初代培養細胞に対する毒性を調べたところ、3’,4’DHBnIQが弱い毒性を示したが、それ以外は毒性を示さなかった(Fig.3)。 3’,4’DHBnTIQのCOMT代謝物3’,4’MHBnTIQの毒性が低いことから、この過程は不活性化として働いていると考えられる。 3’,4’DHBnTIQは、他のパーキンソニズム誘発物質群(MPTP、salsolinol、 -carboline類)とは異なり、酸化、N-メチル化といった代謝活性化を受けないことが示唆された。 -carboline類)とは異なり、酸化、N-メチル化といった代謝活性化を受けないことが示唆された。 4.DHBnTIQ類の作用機構の検討 In vitroの実験系においてDHBnTIQの作用点、作用機構を検討した。 <ドーパミン受容体に対する親和性> ドーパミンD1、D2受容体に対するDHBnTIQの親和性を調べたところ、IC50=10-6〜10-4M程度の親和性を示した。両者を比較すると6,7DHBnTIQの方が親和性が高い。DHBnTIQ類は弱いD2アンタゴニストとして作用しており、この作用は急性的な自発的運動量の減少を引き起こす原因となっていると考えられる。 <ドーパミントランスポーター(DAT)を介した細胞内への取り込み> 線条体シナプトゾームを用い、DHBnTIQ類のドーパミン神経細胞内への取り込みについて調べたところ、3’,4’DHBnTIQが最も活性が高かった(Table 2)。また、TIQ骨格の酸化によるVmax値の減少、N-メチル化によるKm値の上昇、3’-OHのメチル化による活性の消失が観察された。 3’,4’DHBnTIQの取り込みにはカテコール骨格とN原子の周りの立体的、電子的環境が重要であることが示唆される。 3’,4’DHBnTIQ類縁化合物について、細胞内への取り込まれ易さ(Table 2)と細胞毒性の強さ(Fig.3)には正の相関が認められた。また、培養細胞系において、3’,4’DHBnTIQの細胞毒性はドーパミントランスポーター阻害剤GBR12909の添加により抑制された(Fig.4)。以上のことは毒性の発現にドーパミントランスポーターを介した取り込みが関与していることを強く示唆している。  Fig.3 Toxicity of DHBnTIQ derivatives for mesencephalic culture. Fig.3 Toxicity of DHBnTIQ derivatives for mesencephalic culture. Table 2 Kinetic parameters of striatal transport of 3’,4’DHBnTIQ derivatives and 6,7DHBnTIQ by dopamine transporter Table 2 Kinetic parameters of striatal transport of 3’,4’DHBnTIQ derivatives and 6,7DHBnTIQ by dopamine transporter 培養細胞に対する3’,4’DHBnTIQの毒性は、COMT阻害剤Ro41-0960の添加によって抑制された(Fig.4)。これは、COMTが3’,4’DHBnTIQの活性化にも関わっていることを示唆している。3’,4’DHBnTIQが細胞外で3’,4’MHBnTIQに代謝されると、ドーパミントランスポーターによって細胞内に取り込まれにくくなるため毒性が発現しなくなるが、細胞内でのO-メチル化は3’,4’DHBnTIQの活性化に働いている可能性が考えられる。  Fig.4 Effect of inhibitor of dopamine transporter and COMT on 3’,4’DHBnTIQ-induced neurotoxicity Fig.4 Effect of inhibitor of dopamine transporter and COMT on 3’,4’DHBnTIQ-induced neurotoxicity <ミトコンドリア呼吸鎖阻害活性> ミトコンドリア呼吸鎖に対する阻害活性を調べた。3’,4’DHBnTIQ、6,7DHBnTIQは強いcomplex I阻害活性を示した(IC50=80、75 M)。 M)。 3’,4’DHBnTIQはドーパミントランスポーター、ミトコンドリア呼吸鎖に対して作用して毒性を発現していることが示唆された。 結論 以上より、3’,4’DHBnTIQの生体内挙動について、Fig.5のようなスキームが考えられる。 3’,4’DHBnTIQはドーパミントランスポーターの基質となり、ドーパミン神経細胞内に能動的に輸送される。細胞内に取り込まれた3’,4’DHBnTIQはミトコンドリア呼吸鎖を阻害して細胞毒性を発現し、パーキンソニズムを誘発する。3’,4’DHBnTIQはCOMTによってO-メチル化を受けるが、この過程は細胞外では不活性か、細胞内では活性化に働いている可能性が考えられる。  Fig.5 Proposed action of 3’,4’DHBnTIQ in dopaminergic synapse. Fig.5 Proposed action of 3’,4’DHBnTIQ in dopaminergic synapse. 内在性神経毒によるパーキンソン病の発症に、ドーパミントランスポーター、COMTが重要な役割を果たしている可能性が示唆され、パーキンソン病治療を考える上でも興味深いと思われる。 |
| 審査要旨 | | 1-Methyl-4-phenyl-1,2,3,6-tetrahydropyridine(MPTP)がヒトに対してパーキンソニズムを引き起こすことが発見されて以来、パーキンソン病の発症原因として低分子化合物が注目されるようになった。本研究では1,2,3,4-tetrahydroisoquinoline(TIQ)誘導体に関するこれまでの検討をふまえて、新たなTIQ誘導体(1-(3’,4’-dihydroxybenzyl)-1,2,3,4-tetrahydroisoquinoline(3’,4’DHBnTIQ)、1-benzyl-6,7-dihydroxy-1,2,3,4-tetrahydroisoquinoline(6,7DHBnTIQ))を合成し、その作用を薬理学的、生化学的実験により明らかにした。 内在性 C57BLマウス脳内よりDHBnTIQの検出を試みた。高分解能GC-SIM法を用いて検討を行ったところ、標品と同じ保持時間にピークが検出され、3’,4’DHBnTIQ、6,7DHBnTIQが脳内に存在することが明らかにされた。DHBnTIQ類はフェネチルアミンとドーパミンが、モノアミン酸化酵素による代謝物と縮合することで生成すると考えられ、内在性アミンとして生体内に存在することが示された。 神経毒性 胎生16日齢のラット中脳腹側部をDMEM培地中で培養し、DHBnTIQによる細胞死の発現を検討した。3’,4’DHBnTIQは100 M添加で顕著な毒性を示したが、6,7DHBnTIQは毒性を示さなかった。 M添加で顕著な毒性を示したが、6,7DHBnTIQは毒性を示さなかった。 DHBnTIQをC57BLマウスに1日2回、5日間投与してパーキンソニズムの発現を検討した。6,7DHBnTIQ投与マウスは異常が認められなかったが、3’,4’DHBnTIQ投与マウスにはパーキンソニズムが発現した。 3’,4’DHBnTIQは神経毒性を有し、パーキンソン病発症物質の候補化合物であることを明らかにした。 脳内代謝 3’,4’DHBnTIQの酸化体、N-、O-メチル化体を合成し、3’,4’DHBnTIQからこれらの化合物への脳内における代謝を調べた。In vivo系、in vitro系で検討したところ、O-メチル化体のみ代謝物として検出された。この代謝は脳内可溶性画分に存在するカテコール-O-メチルトランスフェラーゼ(COMT)によるものであることを明らかにした。 作用機構 ラット、マウスの脳ホモジネートを用いて、in vitro系におけるDHBnTIQ類の活性(ドーパミントランスポーターによる細胞内輸送、ミトコンドリア呼吸鎖に対する阻害活性)を調べた。DHBnTIQ類はドーパミントランスポーターの基質となって細胞内に取り込まれること、ミトコンドリア呼吸鎖のcomplex Iを阻害することを示した。 3’,4’DHBnTIQの類縁体を用いてドーパミントランスポーターによる細胞内取り込み、中脳培養細胞に対する毒性を調べ、構造活性相関を行った。細胞内取り込み活性と毒性発現の間には正の相関が認められ、3’,4’DHBnTIQの毒性発現にドーパミントランスポーターを介した細胞内への輸送が必要であることが示された。 3’,4’DHBnTIQの毒性に対するドーパミントランスポーター、COMTの阻害剤の効果を中脳培養細胞系において調べた。いずれの阻害剤も3’,4’DHBnTIQ毒性を抑制したことから、毒性発現にはドーパミントランスポーター、COMTによる輸送、代謝過程が必要であることが示唆された。 以上より、DHBnTIQ類が新規内在性アミンであり、3’,4’DHBnTIQはパーキンソン病発症の候補物質であることを示した。また、その作用にはドーパミントランスポーターを介した細胞内への輸送、COMTによる代謝、ミトコンドリア呼吸鎖の阻害が関わっていることを明らかにした。 本研究は、神経毒性を有する化合物を分子設計・合成してその作用を詳細に検討し、パーキンソニズムを誘発する作用機構を提唱したものである。神経化学の分野に有用な知見をもたらし、神経変性疾患の解明に貢献するものであると考えられ、博士(薬学)の学位に十分値するものと認定した。 |