近年、DNAの塩基配列を認識し、切断するDNA切断分子の研究が行われている。これら低分子化合物の開発は医療、遺伝子工学等での応用と共に、反応場であるDNAの性質に関する知見をもたらすので重要である。当研究室では天然のDNA切断酵素にない活性を有し、更にその切断活性を光で制御可能なDNA切断分子を合成し、DNAとの相互作用様式を解析している。化合物のデザインはDNAの5’-GPy-3’配列を特異的に切断する抗腫瘍性抗生物質bleomycinをモデルとしている。bleomycinはいくつかの機能部位から構成されており、oligothiazole環でDNAを認識し、錯体部位でDNAを切断するとの報告があった。そこで我々はDNA結合部位にoligothiazole環を有し、光照射によりp-nitrobenzamide基(pNoBz)がDNAの糖鎖を切断する人工DNA切断分子(pNoBz-oligothiazole誘導体:図1)を合成し解析を行ったところ、これら誘導体はthiazole環の数に依存した塩基配列特異的DNA切断活性を有すること、即ち1a及び2aは水素引き抜き反応によりある特定の5塩基配列を認識し切断したのに対し、3aは5’側の5’-GpG-3’配列を特異的に切断する結果が当研究室の四ノ宮らの研究及び論文提出者の修士課程からの研究により判明している。  図1 thiazole誘導体 図1 thiazole誘導体 そこで、pNoBz基のDNA切断活性を再検討すべく図2に示すnitro誘導体0aおよび0aPhを合成し解析した結果、これら芳香族ニトロ化合物はDNAに対する化合物の濃度(r値)が低いとき、水素引き抜き反応によりA/T-richな配列を選択的に切断することが判明した。なお、この配列選択性は1aおよび2aのものとほぼ一致した。このことは、0a及び0aPhがDNAのminor grooveに結合し、切断活性を示すことを意味しており、更にoligothiazole環が1a及び2aにおける塩基配列認識には積極的に関わっていないことを示唆する。r値をさらに高くすると、0a及び0aPhは5’-GG-3’配列の5’側のguanineを選択的に切断した。この5’-GG-3’切断活性はピペリジン処理により大きく加速される特徴を示し、また0aはguanineを酸化生成物imidazoloneとすることがHPLC解析により同定された。以上の結果により0a及び0aPhによる5’-GG-3’選択的切断メカニズムはguanineからpNoBzへの電子移動反応による酸化的DNA切断であることが判明した。これはpNoBz基の新規DNA切断ルートを発見したことを意味する。  図2 nitro誘導体 図2 nitro誘導体 次にpNoBz基が有する二種類の切断ルートの決定要因をbuffer中の塩濃度を変化させ解析した。通常の実験条件での塩濃度は20〜50mMであり、低いr値において0aは水素引き抜き反応によりDNAのA/T-richな配列を切断する。塩濃度を高くすると図3に示すように0aの切断ルートは水素引き抜き反応(5’-AAATA-3’配列選択的切断)から電子移動反応(5’-GG-3’配列選択的切断)へと切り替わった。すなわち、塩濃度で切断メカニズムを制御可能なDNA切断分子の開発に成功した。これは以下に示す塩の効果に起因するものと考えている。一つは電子移動により生じたion pairが塩の存在により溶媒和・離散し易くなり、逆電子移動反応が起こりにくくなることによる効果である。もう一つはDNAの minor grooveへの0aの結合を不安定化し、競合ルートである水素引き抜き反応を阻害することによる効果である。よって、1a及び2aについても、この二条件が二つの反応ルートを選択する鍵になっていると考えられる。以上の結果から、3aにおいて発見された新しい塩基配列特異的切断は、pNoBz基由来の電子移動反応によるものである可能性が得られた。 そこで他のoligothiazole誘導体0a、1a及び2aと異なり3aが低塩濃度でも、電子移動反応によりDNAを切断する機構を解明するために、考え得る3aの切断メカニズムを検討したところ、図4に示す二つの経路が示唆された。これらルートの共通点はterthiazole環からpNoBzへ電子移動が起こり、次にguanineからterthiazole radical cationへ電子移動が起こりguanineが酸化されるところである。 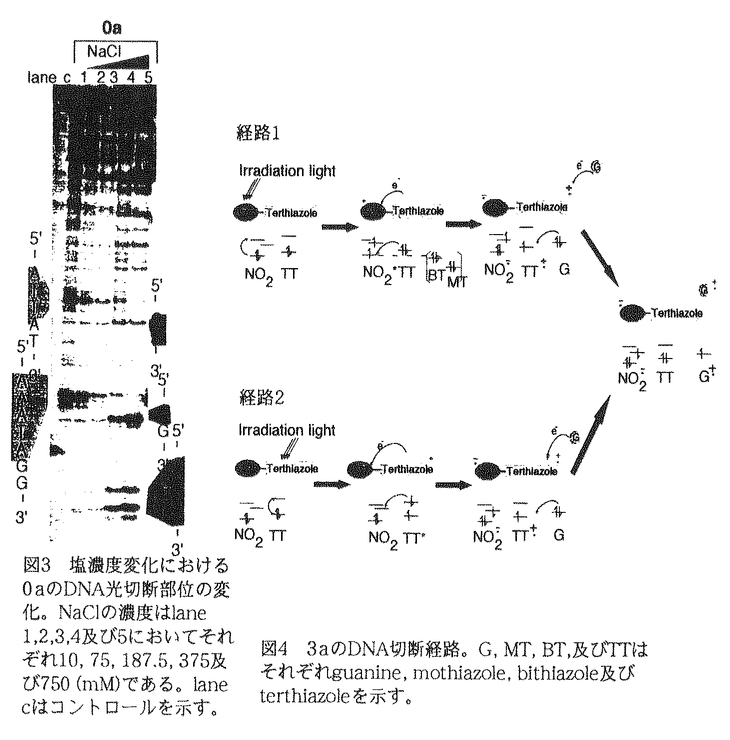 図表図3 塩濃度変化における0aのDNA光切断部位の変化。NaClの濃度はlane1,2,3,4及び5においてそれぞれ10,75,187.5,375及び750(mM)である。lane cはコントロールを示す。 / 図4 3aのDNA切断経路。G,MT,BT,及びTTはそれぞれguanine,mothiazole,bithiazole及びterthiazoleを示す。 図表図3 塩濃度変化における0aのDNA光切断部位の変化。NaClの濃度はlane1,2,3,4及び5においてそれぞれ10,75,187.5,375及び750(mM)である。lane cはコントロールを示す。 / 図4 3aのDNA切断経路。G,MT,BT,及びTTはそれぞれguanine,mothiazole,bithiazole及びterthiazoleを示す。 経路1ではpNoBz基が、経路2ではterthiazole環がそれぞれphotosensitizerとなる点で両者は異なる。これらの励起の種類とモル吸光係数を考慮した結果、経路2の可能性がより高いとの仮説をたて、その検証をおこなった。方法としては経路2のみでDNA切断活性を示すモデル化合物(図1)を用いた。p-cyanobenzamide基(pCyBz)は電子受容体としての性質を有する点ではpNoBzと同様であるが、吸収波長が異なるために光励起されない点で異なる。よってpCyBzを導入したモデル化合物(pCyBz-oligothiazole誘導体)が3aと同様の切断活性を示せば経路2の存在を証明することが可能である。0b〜3bを合成し、解析を行ったところ2b及び3bは5’-GpG-3’配列の5’側のguanineを電子移動反応により酸化する活性を示し、一方で0b及び1bはDNA切断活性を示さなかった。これにより3aは2b及び3b同様経路2によりguanineを酸化的に切断することが証明された。pNoBz-oligothiazole誘導体によるDNA切断がthiazole環の数に依存するのは、thiazole部位の吸収波長がthiazole環の数によって異なることに起因するのである。 また、3aのDNAに対する親和性と塩基配列選択性を高めるために、DNAのminor groove binderである抗生物質netropsinの構成単位であるN-methylpyrrolecarboxamideを導入したハイブリッド化合物pNoBz-terthiazole-N-methylpyrrolecarboxamide(3c)(図5)を合成し解析したところ、3cは3aより約5倍DNAに対する親和性が高く、DNAを二重鎖切断する活性も有することが明らかになった。  図5 ハイブリッド化合物 図5 ハイブリッド化合物 論文提出者は光切断分子に広く用いられている芳香族ニトロ化合物であるpNoBz基には第二の切断ルートが存在することを発見し、更にその複数存在する切断ルートを塩濃度により切り替え可能な新規化合物及びoligothiazole環を第一、pCyBzを第二増感剤とする5’-GG-3’選択的DNA切断分子の開発に成功した。 |