伝達性海綿状脳症(transmissible spongiform encephalopathy)又はプリオン病と呼ばれる疾患には、ヒツジのscrapie、ウシのbovine spongiform encephalopathy、ヒトのCrutzfeldt-Jakob diseaseなどが含まれる。本疾患では、脳内に神経細胞の空胞変性、プロテアーゼ抵抗性異常型プリオン蛋白質(scrapie isoform of prion protein:PrPSc)の沈着が観察される。このPrPScは、宿主細胞が産生している正常細胞型プリオン蛋白質(normal cellular prion protein;PrPC)の構造異性体であり、本疾患の伝達・発症に重要な働きをしていると考えられている。現在までに得られている多くの研究成果から、本疾患はPrPScが鋳型となりPrPCをPrPScに構造変換することで発症するとするプリオン仮説が多くの研究者によって支持されている。プリオン蛋白質遺伝子欠損マウス(PrP0/0マウス)を用いた感染実験では本疾患の伝達が成立しないことも、この仮説を強く支持しており、本疾患の伝達・発症機序を考える上でPrPCは重要である。 長年PrPCの正常機能について多くの研究者が興味を持ってきた。PrP0/0マウスを用いた解析により、海馬におけるシナプスの機能や、小脳プルキンエ細胞の維持、概日活動周期や睡眠の制御、神経細胞死の抑制などへの関与が報告されているが、PrPCの機能を完全に知るには至っていない。 PrPCは肝臓を除く多くの組織で産生が確認されているが、PrPCの機能解析には、産生量が多いことや疾患との関係から神経細胞を用いた解析が主流であった。本研究では、免疫担当細胞を用いてPrPCの解析を行うこととした。これは神経細胞と比較して解析方法が多数開発されており、細胞の成熟過程やサイトカイン・ケモカインなどの産生物に関して多くの情報が蓄積されていることなどから、機能の解析を進める上で有用な細胞群であると考えた為である。さらに、成熟リンパ球欠損マウスを用いた腹腔からの感染実験では本疾患の伝達が成立しなかったことから、腹腔からの本疾患の伝達に免疫担当細胞が関与していることが示唆されている。そこで、本研究では免疫担当細胞表面上のPrPCの産生を詳細に解析することを目的とした。さらに、その結果からPrPCの免疫担当細胞の正常機能について検討を加えることにした。 第一章では、PrP0/0マウスと野生型マウス(C57BL/6マウス)を用いて、免疫担当細胞におけるPrPCの産生について検討した。PrPCがglycosylphosphatidyl inositol anchorで細胞膜表面上に存在することが知られていることから、抗プリオン蛋白質モノクローナル抗体(6H4)を用いてflow cytometerで解析を試みた。本研究では、成体マウスの第一次免疫組織(胸腺、骨髄)、第二次免疫組織(脾臓、腸管リンパ組織)および成体マウス末梢血細胞群、腹腔内細胞群、さらに胎仔肝臓、胎仔胸腺に存在する細胞群に着目した。その結果、第一次免疫組織細胞中に、有為にPrPCの産生が認められた。胸腺はT細胞の分化増殖器官であり、存在する細胞の大多数が分化過程にあるT細胞である。骨髄には、すべての血液細胞に分化しうる細胞である多能性幹細胞を含む様々な未成熟細胞が含まれている。一方、第二次免疫組織・末梢血細胞群・腹腔内細胞群でのPrPCの有為な産生は認められなかった。つまり、脾臓の成熟したT細胞・B細胞、濾胞性樹状細胞、脾臓マクロファージ、 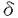 型T細胞受容体を持つ 型T細胞受容体を持つ 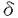 T細胞などの小腸絨毛上皮細胞間リンパ球、末梢血細胞群の顆粒球・末梢血マクロファージ・末梢血リンパ球、腹腔内細胞群の腹腔マクロファージ、B-1b細胞でのPrPCの産生は検出限界以下であった。胎仔肝臓では胎仔齢17.0日でPrPCの産生が観察されたのを最高に、以後減少した。胎仔胸腺では胎仔齢15.0日以後PrPCの産生が減少するのが観察された。 T細胞などの小腸絨毛上皮細胞間リンパ球、末梢血細胞群の顆粒球・末梢血マクロファージ・末梢血リンパ球、腹腔内細胞群の腹腔マクロファージ、B-1b細胞でのPrPCの産生は検出限界以下であった。胎仔肝臓では胎仔齢17.0日でPrPCの産生が観察されたのを最高に、以後減少した。胎仔胸腺では胎仔齢15.0日以後PrPCの産生が減少するのが観察された。 本研究で得られた結果から、第一次免疫組織である胸腺・骨髄に存在する細胞で有為に高いPrPCの産生が確認されたのに対して、分化したリンパ球が存在する脾臓・腸管リンパ器官に存在する細胞及び末梢血細胞群においてPrPCの産生が低くなっていることが興味深い。このことは、少なくともリンパ球の分化過程において成熟が進むに連れてPrPCの産生が減少することを示している。胎仔肝臓及び胎仔胸腺細胞の解析結果もこの事を支持している。 第二章では、PrPCの産生変動の時期を検討することで、PrPCの機能を考える上で重要な情報を得られるものと考え、リンパ球の分化・増殖とPrPCの産生変動についてflow cytometerを用いて詳細に検討した。 骨髄でリンパ幹細胞からT細胞へと分化が進んだT前駆細胞は胸腺へと移行し、成熟T細胞へと分化することが知られている。CD4・CD8を細胞表面マーカーとして胸腺細胞の細胞分画を行うと、T細胞の分化はCD4-CD8-からCD4+CD8+細胞を経て、CD4+CD8-またはCD4-CD8+細胞へと進んでいく。この時、各細胞画分におけるPrPCの産生を検討するとCD4-CD8-細胞に有為な産生が認められた。このことは、T細胞の分化が進むとPrPCの産生が減少することを示している。さらに、CD4-CD8-細胞をCD3を指標に分画するとCD4-CD8-CD3+より未熟なCD4-CD8-CD3-細胞でPrPCの産生が確認された。CD4-CD8-CD3-細胞はCD25+細胞やCD44+細胞を含むが、これらの細胞画分にPrPCの産生が確認された。 さらに、未分化な細胞について検討するために、骨髄細胞をCD34、CD117(c-kit)、B220を指標に分画した。c-kitは幹細胞およびT細胞分化細胞表面マーカーで、c-kit+細胞にPrPCの産生が見られた。一方、B細胞に分化したことを示すB220+細胞ではPrPCの産生が見られなかった。さらに、マウスにおいてCD34+細胞は骨髄細胞の2.5%を占めるが、PrPCの産生は検出限界以下であり、このことはヒトのCD34+細胞でPrPCの産生が検出されるとする報告とは異なる。ヒトでは多能性幹細胞はCD34+細胞であることが示されているのに対して、マウスではc-kit+Sca-1+Lin-の内、CD34-またはCD34lowに存在するとする報告があった。本研究の知見は、PrPCはリンパ幹細胞を経てB細胞へと分化が進むと減少しT細胞へと分化が進むと産生が増加することを示唆しているだけでなく、PrPCが多能性幹細胞を研究する上で有効な細胞表面マーカーであることを示している。 また、マイトジェン刺激に対する反応性を検討する為に、T細胞特異的マイトジェンとしてコンカナバリンA(Con A)を、B細胞特異的マイトジェンとしてLPSを用い、脾細胞を3日間刺激した。その結果、Con A刺激時に有為にPrPCの産生増加が認められたが、LPS刺激では認められなかった。 以上の結果から、PrPCは多能性幹細胞からCD4-CD8-CD3-細胞へと分化していく過程で産生された後、急速に減少することに加え、マイトジェン刺激時の幼若化と共に増加することが示された。 これまでの結果から、PrPCの機能はB細胞ではなくT細胞と関連している可能性があると考えられた。そこで第三章では、PrPCの正常機能について検討する為に、T細胞でのPrPCの産生増加時期に着目した。この時期は、IL-2R(CD25)が産生増加する時期でもあり自己産生IL-2の産生増加も考えられた。そこでPrPCがIL-2の産生に関係するのではないかと仮説をたて、IL-2 mRNA転写量を指標に検討した。IL-2 mRNA転写時にはCu2+が必要であることが知られていることから、PrP0/0マウスとC57BL/6マウスから脾細胞を回収し、Cu2+特異的キレート剤存在下で2日間培養し、細胞内及び培養液中のCu2+を減少させた。この細胞をCon A存在下で2日間培養後、培養液中にCu2+を添加し、その時のIL-2 mRNA転写量を検討した。その結果、C57BL/6マウス由来細胞に比べてPrP0/0マウス由来細胞はCu2+添加4時間後にIL-2 mRNA転写の遅延が確認された。このことは、PrPCの存在がIL-2 mRNAの転写に影響を与えていることを示している。IL-2 mRNAの転写時のPrPCの影響が、細胞内及び培養液中のCu2+を減少した時に出ること、PrPCにはCu2+の結合能があることから、PrPCがCu2+の輸送に関係している可能性がある。これらの知見は、T細胞でのPrPCの正常機能のうちの一つを解明しただけではなく、神経細胞など他の細胞における共通の機能である可能性がある。 本研究では、免疫担当細胞表面上のPrPCの産生を詳細に解析した結果、第一次免疫組織である胸腺・骨髄及び胎児肝細胞・胎児胸腺に含まれる細胞に、PrPCの産生を見いだし、多能性幹細胞からCD4-CD8-CD3-細胞へと分化していく過程でPrPCは産生された後、急速に減少することを発見した。さらにマイトジェン刺激時に脾臓T細胞の幼若化と共に増加することを示した。また、このPrPCの産生がT細胞のIL-2の転写に影響を与えている結果を得ることに成功した。本研究の知見は、PrPCの機能を考える上で重要な発見であると考えられる。 |