生体の免疫系は全身免疫系と粘膜免疫系から構成されている。粘膜免疫系は、消化器系、呼吸器系、泌尿生殖器系などの粘膜面に発達している免疫系である。小腸上皮細胞間リンパ球(IEL)は、(腸管)粘膜免疫系の重要な構成要素の1つであり、その名の通り、小腸の上皮細胞間に存在するリンパ球である。小腸IELは、粘膜免疫系に特異的なsubsetを高率に含んでいることから、近年、精力的に研究が進められてきた。従来のIELに関する研究は、小腸全体のIELを用いたものがほとんどであったが、小腸は縦に長い器官であり、部位によりその組織や機能が異なることが報告されている。このことから、小腸IELについても部位により性質が異なることが推測された。そこで申請者はマウスの小腸を長さにより3等分し、小腸上部、中部、下部から分離されたIELの数とsubset構成について比較検討した。 まず、我々は雌雄のBALB/cマウスを用いて、小腸IELの分布の部位差を検討した。その結果、小腸各部に分布するIELの数、および割合は、雌雄のマウスでほとんど同じであり、上部>中部>下部という傾向を示した。これは、小腸の絨毛の長さと相関した結果だと考えられた。また、IELのsubset構成については、特に小腸上部と下部で大きな差が認められ、中部は上部と下部の中間の傾向を示すことが明らかになった。例えば、  T細胞の割合は小腸下部で高く、逆に、 T細胞の割合は小腸下部で高く、逆に、 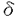 T細胞の割合は小腸上部で高かった。これは、 T細胞の割合は小腸上部で高かった。これは、  T細胞がgerm-freeマウスをconventional化した際に著しく増加すること、および小腸下部の腸内細菌数は上部の約100倍と多いことから、 T細胞がgerm-freeマウスをconventional化した際に著しく増加すること、および小腸下部の腸内細菌数は上部の約100倍と多いことから、  T細胞が腸内細菌による抗原刺激を受け、腸管局所でexpansionした結果である可能性が高いと考えられた。また、 T細胞が腸内細菌による抗原刺激を受け、腸管局所でexpansionした結果である可能性が高いと考えられた。また、  T細胞中のsubset構成では、CD8 T細胞中のsubset構成では、CD8  細胞の割合が小腸上部で高く、CD4細胞とCD4CD8 細胞の割合が小腸上部で高く、CD4細胞とCD4CD8  double positive(DP)細胞の割合が小腸下部で高かった。このうち、CD8 double positive(DP)細胞の割合が小腸下部で高かった。このうち、CD8  細胞は、自己反応性の禁止T細胞レセプター(TCR)を発現する細胞が多いこと、TCR-CD3複合体のシグナル伝達分子として、通常のCD3 細胞は、自己反応性の禁止T細胞レセプター(TCR)を発現する細胞が多いこと、TCR-CD3複合体のシグナル伝達分子として、通常のCD3 鎖の代わりにFcR 鎖の代わりにFcR 鎖をhomodimer、あるいはheterodimerとして用いていること、その成熟がIL-2R 鎖をhomodimer、あるいはheterodimerとして用いていること、その成熟がIL-2R に依存性であることなどから、非胸腺由来のsubsetであると考えられている。一方、CD4CD8 に依存性であることなどから、非胸腺由来のsubsetであると考えられている。一方、CD4CD8  DP細胞については、胸腺で成熟したCD4細胞が腸管にmigrateし、局所で腸内細菌抗原を認識してCD8 DP細胞については、胸腺で成熟したCD4細胞が腸管にmigrateし、局所で腸内細菌抗原を認識してCD8  分子を発現し、CD4CD8 分子を発現し、CD4CD8  DP細胞になるという説が一般的である。つまり、CD4細胞とCD4CD8 DP細胞になるという説が一般的である。つまり、CD4細胞とCD4CD8  DP細胞は、胸腺由来の同じlineageに属するsubsetであると考えられる。このことから、 DP細胞は、胸腺由来の同じlineageに属するsubsetであると考えられる。このことから、  T細胞中における各subsetの部位差は、非胸腺由来のsubsetと胸腺由来のsubsetの分布が部位により異なるために生じていると考えられた。一方、 T細胞中における各subsetの部位差は、非胸腺由来のsubsetと胸腺由来のsubsetの分布が部位により異なるために生じていると考えられた。一方、 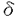 T細胞中のsubset構成には部位差は認められなかった。このようなIELの部位差は、雌雄のマウスでほとんど同じように認められ、性差はないものと考えられた。 T細胞中のsubset構成には部位差は認められなかった。このようなIELの部位差は、雌雄のマウスでほとんど同じように認められ、性差はないものと考えられた。 次に、前述のBALB/cに加え、C3H/He、およびC57BL/6の計3種の近交系の雄マウスを用いて、小腸IELの分布の部位差を検討した。その結果、小腸IELの総数には系統により大きな違いが見られるものの、小腸各部に分布するIELの割合についてはほとんど差が認められなかった。また、IELのsubset構成についても、各subsetの占める割合は系統により異なるものの、全体的な傾向としては、前述のBALB/cマウスの結果とほぼ同様の結果が得られた。これらの結果から、小腸IELの部位による差は、マウスの性や系統によらずに認められる、マウスに普遍的な生物学的現象であることが明らかになった。 上記2実験の結果から、マウスの小腸におけるIELの部位差は、胸腺由来のsubsetと非胸腺由来のsubsetの割合が小腸の部位により異なるために生じると推測され、胸腺の重要性が示唆された。そこで、小腸IELの部位差に与える胸腺の影響について、胸腺を欠損するnu/nuマウスと胸腺を有するnu/+マウス(ともに背景はBALB/c)を用いて検討した。nu/+マウスは、nu/nuマウスを用いた実験の対照群として頻用されているが、その性質は正常(+/+)マウスと完全には同じではないことが知られている。そのため、前述のBALB/cマウスの結果とも比較検討した。その結果、nu/nuマウス、nu/+マウスともに、BALB/cマウスに比べてIELの総数は約5〜6分の1に減少していた。nu/nuマウス、nu/+マウスはともに骨髄幹細胞数の減少を示すことが報告されており、IELの減少は骨髄幹細胞数の減少による二次的な影響によるものと考えられた。また、小腸各部に分布するIELの割合は、特に小腸下部で著しく減少していた。IELのsubset構成については、nu/+マウスではBALB/cマウスほど顕著ではないものの、概ね類似した部位差が認められた。一方、nu/nuマウスでは個体差が非常に大きいため、IELの部位差は明らかではなかった。また、nu/nuマウスではTCR-CD3複合体の発現率が40%程度と低く、IELの成熟が阻害されていた。一方、nu/+マウス、BALB/cマウスでは、TCR-CD3複合体の発現率は90%以上であった。このことは、IELの分化(胸腺内分化、胸腺外分化とも)における胸腺の重要性を示唆するものと考えられた。IELは、胸腺由来の細胞群と非胸腺由来の細胞群に大別される。胸腺由来の細胞群はさらに、胸腺内でのみ分化する細胞群と、胸腺で分化した後、胸腺外でさらに分化する細胞群に分けられ、非胸腺由来の細胞群は、胸腺由来の因子、あるいは胸腺由来の細胞群が産生するサイトカイン類に依存性に分化する細胞群と完全に胸腺非依存性に分化する細胞群に分けられる。本実験で、nu/nuマウスでもすべてのT細胞subsetが認められた。しかし、nu/nuマウスでは、IELの部位差はまったく見られなかったことから、完全に胸腺非依存性に分化する細胞群に関しては部位差がないことが明らかとなった。また、  T細胞subsetの中で、大部分のCD8 T細胞subsetの中で、大部分のCD8  細胞は非胸腺由来であり、大部分のCD4細胞とCD4CD8 細胞は非胸腺由来であり、大部分のCD4細胞とCD4CD8  細胞は胸腺由来であることから、小腸IELの部位差には胸腺が非常に重要であること、小腸IELの部位差は、主に胸腺依存性の 細胞は胸腺由来であることから、小腸IELの部位差には胸腺が非常に重要であること、小腸IELの部位差は、主に胸腺依存性の  T細胞subsetの腸管へのmigration、あるいは局所でのexpansionに、小腸の部位による差があるために生じることが明らかになった。 T細胞subsetの腸管へのmigration、あるいは局所でのexpansionに、小腸の部位による差があるために生じることが明らかになった。 小腸IELの数およびsubset構成に、腸内細菌が大きく関与することはよく知られている。前述したように、小腸下部の腸内細菌数は上部の約100倍で、また、  T細胞の認識する抗原として腸内細菌は特に重要である。そこで、germ-free(GF)のBALB/cマウスとspecific pathogen free(SPF)のBALB/cマウスを用いて、小腸IELの分布の部位差を検討した。その結果、GFマウスではSPFマウスに比べてIELの総数が7分の1以下に減少していた。特に、小腸下部に分布するIELの割合は、上部、中部に比べ激減しており,腸内細菌がIELの腸管局所でのexpansionに大きく関与していることが確認された。一方、IELのsubset構成については、GFマウスとSPFマウスで概ね類似しているものの、いくつかの相違も見られた。例えば、GFマウスのIELのTCR-CD3複合体の発現率は、上部、中部に比べて下部で低いのに対し、SPFマウスでは逆に下部で高くなっており、IELのTCR-CD3複合体の発現に腸内細菌が関与することが示された。しかし、GFマウスでもSPFマウスでも、TCRの発現パターンは小腸下部で T細胞の認識する抗原として腸内細菌は特に重要である。そこで、germ-free(GF)のBALB/cマウスとspecific pathogen free(SPF)のBALB/cマウスを用いて、小腸IELの分布の部位差を検討した。その結果、GFマウスではSPFマウスに比べてIELの総数が7分の1以下に減少していた。特に、小腸下部に分布するIELの割合は、上部、中部に比べ激減しており,腸内細菌がIELの腸管局所でのexpansionに大きく関与していることが確認された。一方、IELのsubset構成については、GFマウスとSPFマウスで概ね類似しているものの、いくつかの相違も見られた。例えば、GFマウスのIELのTCR-CD3複合体の発現率は、上部、中部に比べて下部で低いのに対し、SPFマウスでは逆に下部で高くなっており、IELのTCR-CD3複合体の発現に腸内細菌が関与することが示された。しかし、GFマウスでもSPFマウスでも、TCRの発現パターンは小腸下部で  T細胞の割合が高く、小腸上部で T細胞の割合が高く、小腸上部で 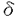 T細胞の割合が高いという同様の傾向を示した。また、 T細胞の割合が高いという同様の傾向を示した。また、  T細胞中のsubset構成についても、GFマウスでは腸内細菌依存性に胸腺外分化するCD4CD8 T細胞中のsubset構成についても、GFマウスでは腸内細菌依存性に胸腺外分化するCD4CD8  細胞はほとんど見られないものの、小腸上部で非胸腺由来のCD8 細胞はほとんど見られないものの、小腸上部で非胸腺由来のCD8  細胞の割合が高く、小腸下部で胸腺由来のCD4細胞とCD4CD8 細胞の割合が高く、小腸下部で胸腺由来のCD4細胞とCD4CD8  細胞の割合が高いという傾向は、GFマウスとSPFマウスに共通して認められた。こうしたことから、腸内細菌はIELのlocal expansionやTCR-CD3複合体の発現、CD4+ 細胞の割合が高いという傾向は、GFマウスとSPFマウスに共通して認められた。こうしたことから、腸内細菌はIELのlocal expansionやTCR-CD3複合体の発現、CD4+  T細胞の局所でのCD8 T細胞の局所でのCD8  分子の発現などに大きな影響を与えるものの、IELの部位差を決定する主要な要因ではないと考えられた。 分子の発現などに大きな影響を与えるものの、IELの部位差を決定する主要な要因ではないと考えられた。 上述した本研究の結果から、小腸におけるIELの部位差はマウスの性や系統によらず認められるマウスに普遍的な現象であること、部位差の発現には胸腺依存性の  T細胞が大きく関与していること、部位差は腸内細菌などの影響により外因性に誘導されるのではなく、内因性要因によって決定されていると考えられることなどが明らかになった。本研究の成果は、腸管粘膜免疫系のより一層の機能の解明に資するところ大であり、今後病態下におけるIELの動態を解析する上での基礎資料としても非常に重要である。 T細胞が大きく関与していること、部位差は腸内細菌などの影響により外因性に誘導されるのではなく、内因性要因によって決定されていると考えられることなどが明らかになった。本研究の成果は、腸管粘膜免疫系のより一層の機能の解明に資するところ大であり、今後病態下におけるIELの動態を解析する上での基礎資料としても非常に重要である。 |