インターフェロン・タウ(IFN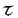 )は反芻動物の胚の栄養膜細胞から着床前後に特異的に分泌されるサイトカインであり、妊娠の成立に重要な役割を果たしている。この遺伝子発現の機構を解析することにより時期・空間特異的な遺伝子発現制御機構だけでなく、着床期における転写因子、細胞内情報伝達分子の動態が明らかとなる。本研究では、これらの背景からIFN )は反芻動物の胚の栄養膜細胞から着床前後に特異的に分泌されるサイトカインであり、妊娠の成立に重要な役割を果たしている。この遺伝子発現の機構を解析することにより時期・空間特異的な遺伝子発現制御機構だけでなく、着床期における転写因子、細胞内情報伝達分子の動態が明らかとなる。本研究では、これらの背景からIFN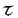 遺伝子発現を制御する5’上流域の解析を行った。 遺伝子発現を制御する5’上流域の解析を行った。 これまでの研究からIFN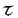 遺伝子の発現はGM-CSFやPMAにより増大することがわかっている。始めに、IFN 遺伝子の発現はGM-CSFやPMAにより増大することがわかっている。始めに、IFN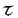 遺伝子上流域をCAT遺伝子に接続したプラスミドを作成し、4種類の細胞に導入し、PMAで処理後に転写活性を測定した。その結果、JEG3と293ではPMAにより転写活性は増大するが、HeLaやVeroでは変化がみられなかった。そこでPMAからのシグナル伝達にどのような転写因子が関与しているかどうかをしらべるために、JEG3とHeLa用いて、数種の転写因子の発現プラスミドと共に細胞に導入し転写活性を測定した。その結果、両細胞でc-Junにより転写活性は増大したが、IFN 遺伝子上流域をCAT遺伝子に接続したプラスミドを作成し、4種類の細胞に導入し、PMAで処理後に転写活性を測定した。その結果、JEG3と293ではPMAにより転写活性は増大するが、HeLaやVeroでは変化がみられなかった。そこでPMAからのシグナル伝達にどのような転写因子が関与しているかどうかをしらべるために、JEG3とHeLa用いて、数種の転写因子の発現プラスミドと共に細胞に導入し転写活性を測定した。その結果、両細胞でc-Junにより転写活性は増大したが、IFN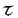 は他のIFNの遺伝子発現を制御しているIRFでは制御されなかった。このことからIFN は他のIFNの遺伝子発現を制御しているIRFでは制御されなかった。このことからIFN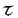 の転写はプロテインキナーゼCからAP-1を介したシグナル伝達系により制御される可能性が示唆された。 の転写はプロテインキナーゼCからAP-1を介したシグナル伝達系により制御される可能性が示唆された。 次に、IFN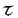 遺伝子上流域のDeletionプラスミドを作成しJEG3に導入し、転写活性を測定した。その結果、上流-654から-555baseまでにエンハンサー領域が存在することが示唆された。次にそのエンハンサー配列に変異を導入し転写活性を測定して、エンハンサーの中心部が明らかとなった。そこでこの配列に対するプローブを準備しゲルシフトアッセイによりタンパク質の結合能を調べた。その結果、AP-1とGATA配列を認識して結合する蛋白質が存在することが示唆された。さらにスーパーシフト法によりエンハンサー領域にAP-1が結合することが明らかとなった。次にGATA-1,2,3のIFN 遺伝子上流域のDeletionプラスミドを作成しJEG3に導入し、転写活性を測定した。その結果、上流-654から-555baseまでにエンハンサー領域が存在することが示唆された。次にそのエンハンサー配列に変異を導入し転写活性を測定して、エンハンサーの中心部が明らかとなった。そこでこの配列に対するプローブを準備しゲルシフトアッセイによりタンパク質の結合能を調べた。その結果、AP-1とGATA配列を認識して結合する蛋白質が存在することが示唆された。さらにスーパーシフト法によりエンハンサー領域にAP-1が結合することが明らかとなった。次にGATA-1,2,3のIFN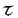 の転写に対する影響を調べたところGATA-1,2,3では変化はなかった。これらの結果から、Ap-1はIFN の転写に対する影響を調べたところGATA-1,2,3では変化はなかった。これらの結果から、Ap-1はIFN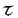 遺伝子の上流域に結合することにより直接的にIFN 遺伝子の上流域に結合することにより直接的にIFN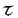 の転写に関与していることがわかった。またGATA-1,2,3は単一ではIFN の転写に関与していることがわかった。またGATA-1,2,3は単一ではIFN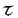 遺伝子の転写因子には成り得ず、他のファクターと協調するか、他のGATA配列を認識する蛋白質により転写を実現していると考えられる。 遺伝子の転写因子には成り得ず、他のファクターと協調するか、他のGATA配列を認識する蛋白質により転写を実現していると考えられる。 次に、サイレンサーを詳細に検討した。CATアッセイにより転写抑制領域の配列がエンハンサーの上流と下流に存在することが示唆された。次にHeLaおよびJEG3からの核抽出液を用いてゲルシフトアッセイを行ったところ、この配列には両細胞の核タンパク質が結合する事が示された。さらに、IFN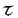 遺伝子発現が異なる時期のヒツジ胚から抽出した核タンパク質を用いたところ、両者で結合パターンに違いがみられた。以上の結果より、この領域は何らかの核タンパク質が結合して転写を抑制する領域である可能性が示唆された。このことがらIFN 遺伝子発現が異なる時期のヒツジ胚から抽出した核タンパク質を用いたところ、両者で結合パターンに違いがみられた。以上の結果より、この領域は何らかの核タンパク質が結合して転写を抑制する領域である可能性が示唆された。このことがらIFN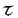 遺伝子の時期特異的発現には転写抑制因子と活性化因子の両者により成り立っていると考えられる。 遺伝子の時期特異的発現には転写抑制因子と活性化因子の両者により成り立っていると考えられる。 続いて細胞特異性な遺伝子発現を決定する転写制御領域を明らかにするために、JEG3とHeLaを用いて転写制御領域の解析を行った。ルシフェラーゼアッセイによりエンハンサー領域が細胞特異的な転写活性に重要な役割を果たしていることがわかった。次にエンハンサー領域の活性の中心部に詳細に変異を導入し、そのエンハンサー領域を検討したところ、エンハンサー領域は主に3ヵ所(AP-1サイトとGATA様配列、未知の配列)に分けられた。そこでこの部位に対するタンパク質の結合を調べたところ、AP-1サイトと未知のサイトにはJEG3とHeLaでタンパク質の結合に違いはみられなかったのに対し、GATA様配列に結合するタンパク質の結合様式に関して、両細胞間で違いがみられた。このことからエンハンサー領域に結合する因子のうち、GATA様配列に結合する因子がこの細胞間の転写活性の違いに関与している可能性が示唆された。また着床期のヒツジの胚の栄養膜細胞の核タンパク質でもJEG3の場合と同様なタンパク質の結合が確認されたことからエンハンサー領域は生体においても機能している可能性が示唆された。 以上要約すると、本研究ではIFN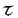 遺伝子上流域の解析を行い、遺伝子発現を制御する領域を同定した。これは着床期に特異的に発現するIFN 遺伝子上流域の解析を行い、遺伝子発現を制御する領域を同定した。これは着床期に特異的に発現するIFN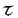 遺伝子の発現制御機構に新しい知見をもたらしたものであり、学術上重要な発見である。口頭試問も適切であり、よって審査委員一同は、本論文が博士(獣医学)の学位論文として価値あるものと認めた。 遺伝子の発現制御機構に新しい知見をもたらしたものであり、学術上重要な発見である。口頭試問も適切であり、よって審査委員一同は、本論文が博士(獣医学)の学位論文として価値あるものと認めた。 |