| 1.はじめに 1997年のWHOの報告によると、B型肝炎による死亡者は年に120万人にのぼっており、その対策は世界中でいまだ重要な問題である。効果的なワクチンの存在にもかかわらず慢性的にB型肝炎ウイルス(hepatitis B virus:HBV)に感染した患者には完全に効果的な抗ウイルス療法が確立されていない。インターフェロン(IFN)の4〜6カ月投与ではせいぜい25〜40%にHBe抗原の持続陰性化が認められるのみであり、満足の行く成績とは言いがたい。HBV DNAは、複製の際にRNA中間体(RNAintermediate)を介して逆転写(reverse transcription)されることから、逆転写酵素阻害剤(reverse transcriptase inhibitors)の使用は、非常に有望である。 本論文では、これら逆転写酵素阻害剤のB型肝炎ウイルスに対する治療効果と、近年臨床的に問題となっている、逆転写酵素阻害剤であるlamivudineに耐性を示すB型肝炎ウイルスについての基礎研究を行った。 2.逆転写酵素阻害剤(Reverse Transcriptase inhibitor) 一般に逆転写酵素阻害剤にはヌクレオシド系(lamivudine,adefovir,lobucavir and penciclovirなど)と、非ヌクレオシド系(Nevirapineなど)に分類できる。 A.Lamivudine:B型肝炎ウイルスに対しlamivudine(3TC)は強い抗ウイルス活性を有する.最近、米国のFood&Drug Administration(FDA)はB型慢性肝炎に対する経口抗ウイルス薬としてlamivudineを認可した。初期の治験(12週間)では100mg/日の投与により90%以上にHBV DNAの増殖抑制が見られた。さらに12-18ケ月の投与では肝組織像の改善が60%の症例に見られ、またHBeAg陽性からHBeAb陽性へとセロコンバージョンした症例が16%に見られた。しかしながら、治療後にはHBV DNAの増加に伴いALTの再燃がみられており、アジア地区の検討では投与症例の20%、欧米での検討では5%に認められた。これら再燃の機序は充分明らかになっていないが、本邦では重篤な投与終了後の副作用としての報告もあるため、今後保険認可後、臨床の現場での使用にあたってはこの点に充分注意する必要がある。また、肝組織での炎症所見の改善も認められていることが報告されてきている。しかしながら、lamivudineの長期投与を受けたB型慢性肝炎患者の14-39%にlamivudine耐性ウイルスの出現が報告されており問題となっている。 B.Adefovir:近年さまざまな新しい抗ウイルス薬が開発されてきており、lamivudine抵抗性B型肝炎ウイルスに対するそれらの作用を評価することは大変重要である。Adefovir(PMEA)は、ヌクレオシドアナログの一つでヒト免疫不全ウィルス(HIV)、ヘルペスウイルス、B型肝炎ウイルスなどのいくつかのウイルスに対し、in vitroで抗ウイルス活性があることが知られている。現在PMEAのプロドラッグであるAdefovir dipivoxil(経口抗ウイルス薬)の臨床治験が米国で進行中である。 C.Lobucavir:Lobucavirも、やはりヌクレオシドアナログで、Ganciclovirと同じ逆転写酵素阻害作用をもち、in vitroでヘルペスウイルス、B型肝炎ウイルスなどのいくつかのウイルスに抗ウイルス活性がある。現在,B型慢性肝炎患者における、その抗ウイルス効果と安全性の検討のため、米国で第I相/第II相試験が進行中である。 D.Penciclovir:Penciclovirはヘルペスウイルス、水痘ウイルス、EBウイルスにおいて抗ウイルス効果が認められており、B型肝炎ウイルスに対しても、抗ウイルス活性が示された。最近、penciclovirのプロドラッグであるfamciclovir(経口抗ウイルス薬)が肝臓移植後のB型肝炎ウイルス再感染予防に有効であることが示された。 E.Nevirapine:非ヌクレオシド系(Non-Nucleoside Reverse Transcriptase Inhibitor:NNRTI)逆転写酵素阻害剤として、nevirapineがあげられる。Nevirapineは、in vitroにおいてHIV-1の逆転写酵素に対し強い阻害作用を示し、ヌクレオシド系薬剤にnevirapineを組み合わせた治療法は従来の治療法では、治療不能なHIV患者に認可されている。これらの各種逆転写酵素阻害剤の基礎的検討および今後の臨床的応用は現在緒についたところである。 3.Lamivudine耐性B型肝炎ウイルス。 Lamivudine耐性ウイルスは,B型肝炎ウイルスDNA polymeraseのreverse transcriptase活性中心であるTyr,Met,Asp,Asp motif(YMDD motif)の変異を有する。我々はsite-directed mutagenesisによりこの部分にmutationを導入することでMetをVal(M552V),Leu(M552L),Ile(M552I),Ala(M552A),Lys(M552K),Thr(M552T),Arg(M552R)に置換した変異B型肝炎ウイルスDNAを作成し,そのウイルス複製能を検討したところ.Val,Leu,Ile,Ala置換による変異B型肝炎ウイルスDNAには複製能が認められたが,Lys,Thr,Arg置換による変異B型肝炎ウイルスDNAには複製能が認められなかった.これら,複製可能なcloneに対し,逆転写酵素阻害剤であるlamivudineを作用させたところ、Val,Ile置換による変異B型肝炎ウイルスDNAのみがlamivudine耐性であることが判明した.B型肝炎ウイルスDNA polymeraseのYMDD motifにおける1アミノ酸置換はB型肝炎ウイルスの複製能に著しく影響し,しかもlamivudine感受性を規定していることが明らかとなった。 4.逆転写酵素阻害剤の野生株B型肝炎ウイルス対する作用。 全長HBV DNAをヒト肝癌細胞にtransfectionし複製する系を用いて,野生株B型肝炎ウイルスに対する新たな逆転写酵素阻害剤であるadefovir,lobucavir,penciclovir と nevirapineの抗ウイルス効果を比較検討した。 HBV DNAをヒト肝癌細胞Huh7にtransfectionし,培養液に各逆転写酵素阻害剤を加え、HBVの複製をSouthern blot hybridizationにて検討した。具体的には、逆転写酵素阻害剤の効果は、B型肝炎ウイルスDNAのsingle-stranded band(複製中間体)を用いて解析した。 Lamivudine,adefovir,lobucavir存在下では、野生株の複製中間体は消失したが,penciclovirとnevirapineではこれら複製中間体は減弱しなかった。すなわち、in vitroにおいて、lamivudine,adefovir,lobucavirは野生株B型肝炎ウイルスに対し抗ウイルス効果を示したが、penciclovir,nevirapineには抗ウイルス効果は認められなかった。これらの結果は、各逆転写酵素阻害剤の臨床治験におけるHBV DNA量の減少パターンと非常によく相関している。 5.Lamivudine耐性B型肝炎ウイルスに対する逆転写酵素阻害剤の効果。 Lamivudine耐性HBVのうち、もっとも頻度の高い変異はM552I,M552VおよびL528M/M552Vであることがわかっている。われわれはlamivudine耐性B型肝炎ウイルスに対する抗ウイルス効果を上記のin vitro感染系を用いて検討した。Lamivudine投与により野生株では複製中間体であるsingle-stranded bandが消失したが,lamivudine耐性株においてはsingle-stranded bandは減弱せず,lamivudine耐性が確認された。Lamivudine耐性株に新たな逆転写酵素阻害剤であるadefovir(PMEA)及びlobucavirを作用させ,lamivudine耐性株がadefovirとlobucavirに感受性であることを見出した。Table1は逆転写酵素阻害剤存在下でのB型肝炎ウイルスの複製の結果をまとめたものである。また同じ濃度で用いた場合,adefovirはlobucavirより強い抗ウイルス効果を有した。Lamivudine耐性株は野生株に比し,よりadefovir,lobucavir抵抗性であり,野生株より高濃度のadefovir,lobucavir投与が必要な可能性がある。 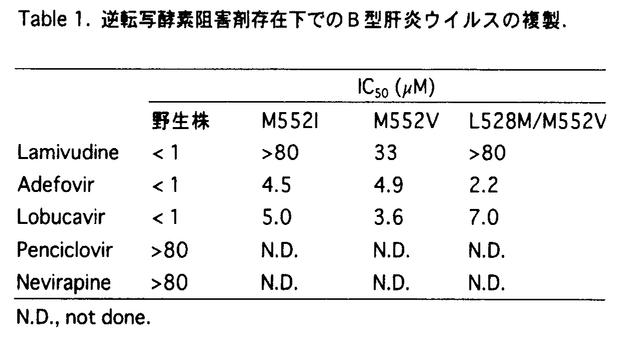 Table1.逆転写酵素阻害剤存在下でのB型肝炎ウイルスの複製.6.おわりに. Table1.逆転写酵素阻害剤存在下でのB型肝炎ウイルスの複製.6.おわりに. Lamivudine耐性株の高い発生率が報告され、lamivudine単独療治ではB型肝炎の根治には、不十分であると思われる。有効なB型肝炎治療には、lamivudine耐性HBV出現を防止することが必要である。Lamivudine耐性株はadefovirとlobucavirに感受性があると考えられるため、adefovirもしくはlobucavirの単独療治あるいはlamivudineとadefovirもしくはlobucavirの併用療法によりlamivudine耐性株出現を防止しうる可能性が示唆された。 |