学位論文要旨
| No | 115431 | |
| 著者(漢字) | 飯倉,元保 | |
| 著者(英字) | ||
| 著者(カナ) | イイクラ,モトヤス | |
| 標題(和) | アレルギー性炎症における免疫グロブリンの新知見 : 分泌型IgAによる好塩基球活性化機構と好酸球の高親和性IgE受容体発現調節 | |
| 標題(洋) | ||
| 報告番号 | 115431 | |
| 報告番号 | 甲15431 | |
| 学位授与日 | 2000.03.29 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(医学) | |
| 学位記番号 | 博医第1617号 | |
| 研究科 | 医学系研究科 | |
| 専攻 | 内科学専攻 | |
| 論文審査委員 | ||
| 内容要旨 | 気管支喘息を代表とするアレルギー疾患は、主としてGell & Coombs分類でのI型アレルギー反応に属している。I型アレルギー反応は、抗原曝露後数分で出現する即時型反応と、数時間後に出現する遅発型反応の二相性反応を呈することがしばしばである。即時型反応では、IgEの架橋により活性化されたマスト細胞の遊離するメディエーターが、平滑筋収縮などを起こし、喘鳴などの臨床症状を惹起する。一方、遅発型反応では、エフェクター細胞である好酸球または好塩基球が、流血中より炎症局所に浸潤し、炎症病態(アレルギー性炎症)を形成している。アレルギー性炎症細胞である好塩基球は、その表面に発現している高親和性IgE受容体(Fc ビーズを担体として固相化したslgAは約15%、プレートを担体としたslgAは約50%というIgE刺激に匹敵する強力なヒスタミン遊離を誘導した。特筆すべきことは、slgAによる脱顆粒にはIL-3による前処置が必須であった。IL-3は5pMという低濃度にて有意なpriming効果を示した。また、IL-3とその受容体の 固相化した単量体IgA、二量体IgA、slgA Fab部分の刺激は全く脱顆粒を起こさなかった。一方、slgAの(Fc)2SC(secretory component)部分刺激ではslgA刺激と同等の脱顆粒が認められ、(Fc2)SC部分が重要であると考えられたが、flow cytometryによる解析では好塩基球上にIgAのFc部分の受容体であるCD89は全く認められなかった。またslgAを固相化したプレートを抗SC抗体で前処置することにより、好塩基球ヒスタミン遊離は約24%に抑制された。これらより、slgA依存性好塩基球脱顆粒ではSCの関与が示唆された。 slgAによる好塩基球脱顆粒は、Fc 可溶性slgAは好塩基球脱顆粒を起こさず、slgA依存性好塩基球脱顆粒には、固相化が必須であると考えられた。加えて、cytochalasin Bの前処置でslgA依存性脱顆粒は完全に抑制された。これらから、細胞接着がslgAによる好塩基球脱顆粒には重要であると考えられた。接着分子の役割を検討するために、 slgAによる好塩基球活性化の臨床的な意義を明らかにするため、喘息患者、健常人の好塩基球でslgAによるヒスタミン遊離を比較検討した。喘息患者10人中4人で、IL-3 primingなしで、slgA刺激にて明らかなヒスタミン遊離が認められ、Th2細胞由来のIL-3、IL-5などにより流血中の好塩基球がprimingされ、ヒスタミン遊離を起こしやすい状態にあると推測された。喘息患者10人のみに絞った検討では、slgA刺激による好塩基球ヒスタミン遊離の感度と喘息患者の罹病期間に正相関が認められ、臨床的にもslgA依存性好塩基球脱顆粒の重要性が示唆された。 健常人好酸球をIgE(1 好酸球上に発現したFc I型アレルギー反応の遷延化、難治化には、臨床的に遅発相が重要である。遅発相では、組織に流入した炎症細胞である好塩基球や好酸球がエフェクター機能を発揮しており、その活性化と制御機構の解明は新たな治療法の開発に直結する重要な課題である。 本研究にて、アレルギー性炎症の場である気道や消化管などの粘膜組織で最も豊富な免疫グロブリンであるslgAがアレルギー性炎症細胞である好塩基球を活性化し、メディエーター遊離をIgEと同程度強力に誘導することを明らかにした。slgAによる好塩基球脱顆粒にはIL-3によるprimingが必須であった。流血中より炎症局所に流入した好塩基球は、生体内でもアレルギー性炎症の場で選択的に産生されるIL-3、IL-5などのcytokine でprimingされていると考えられる。in vitroのslgAによる好塩基球活性化機構は、in vivoでの気道や消化管などの粘膜でのアレルギー性炎症の遷延化において重要な役割を果たしているものと考えられた。SCが直接好塩基球に結合するかどうかは現在検討中であり、好塩基球上のslgA/SCの受容体の同定、およびそのクローニングは、アレルギー疾患のみならず、粘膜免疫の理解に大いに役立つと考えられる。 IL-4とIgEにより健常人好酸球上にもFc slgAによる好塩基球活性化やIgEによる好酸球活性化といった、従来の観点にとらわれない新しい視点からアレルギー性炎症を捉えることにより、アレルギー疾患の更なる病態解明、新しい治療法の発見に繋がるものと期待される。 | |
| 審査要旨 | 本研究は、アレルギー性炎症における免疫グロブリンの未知の作用を明らかにするため、分泌型IgA(sIgA)による好塩基球活性化とIgE、IL-4による好酸球上の高親和性IgE受容体発現調節を検討したものであり、下記の結果を得ている。 1.固相化slgAは約50%というIgE刺激に匹敵する強力なヒスタミン遊離を誘導した。slgAによる脱顆粒にはIL-3による前処置が必須であった。IL-5あるいはGM-CSFもIL-3と同様に強いpriming効果を示した。固相化slgAは、preformed mediatorであるヒスタミン遊離のみではなく、newly synthesized mediatorであるロイコトリエンC4の遊離も誘導した。 2.固相化した単量体IgA、二量体IgA、slgAFab部分の刺激は全く脱顆粒を起こさなかった。一方、slgAの(Fc)2SC(secretory component)部分刺激はslgA刺激と同等の好塩基球脱顆粒を誘導し、slgAの(Fc)2SC部分が重要であると考えられた。 3.slgAによる好塩基球脱顆粒は、細胞外Ca2+とMg2+の両イオンに依存していた。G蛋白阻害作用を持つ百日咳毒素(PTX)の前処置により濃度依存性にslgA依存性遊離の抑制が認められ、slgA依存性好塩基球脱顆粒にはPTX感受性G蛋白が重要であることが明らかになった。wortmanninはslgAによるヒスタミン遊離を完全に抑制し、phosphatidylinositol 3-kinaseの重要性が示唆された。 4.可溶性slgAは好塩基球脱顆粒を起こさず、cytochalasin B前処置でslgA依存性脱顆粒は完全に抑制され、細胞接着がslgAによる好塩基球脱顆粒には重要であると考えられた。接着分子である 5.喘息患者、健常人の好塩基球でslgAによるヒスタミン遊離を比較検討した。喘息患者10人中4人で、IL-3 primingなしで、slgA刺激にて明らかなヒスタミン遊離が認められた。喘息患者群では、slgAによるヒスタミン遊離の感度と罹病期間に相関が認められ、臨床的にもslgA依存性好塩基球脱顆粒の重要性が示唆された。 6.健常人好酸球をIgE(1 7.IgE、IL-4の存在下、非存在下にて7日間培養した好酸球に、Fc 以上、本論文はアレルギー性炎症の場である気道や消化管などの粘膜組織で最も豊富な免疫グロブリンであるslgAがアレルギー性炎症細胞である好塩基球を活性化し、メディエーター遊離をIgEと同程度強力に誘導することを明らかにした。IL-4とIgEにより健常人好酸球上にもFc | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/54760 |
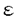 RI)を介する刺激で活性化され、種々のメディエーターを遊離する。しかしながら,IgE以外の免疫グロブリンで強力な好塩基球活性化を誘導するものは知られていない。本研究第一章では、喘息の炎症の場である気道内で最も豊富に存在する免疫グロブリンである分泌型IgA(slgA)に着目し、その好塩基球活性化作用を検討した。一方、アレルギー性炎症でもう一つのエフェクター細胞である好酸球は、IgA及びIgGクラスの免疫グロブリンにより脱顆粒を起こすことが知られているが、IgEによる好酸球活性化、特にFc
RI)を介する刺激で活性化され、種々のメディエーターを遊離する。しかしながら,IgE以外の免疫グロブリンで強力な好塩基球活性化を誘導するものは知られていない。本研究第一章では、喘息の炎症の場である気道内で最も豊富に存在する免疫グロブリンである分泌型IgA(slgA)に着目し、その好塩基球活性化作用を検討した。一方、アレルギー性炎症でもう一つのエフェクター細胞である好酸球は、IgA及びIgGクラスの免疫グロブリンにより脱顆粒を起こすことが知られているが、IgEによる好酸球活性化、特にFc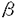 鎖が共通であるIL-5或いはGM-CSFによる前処置でも明らかな遊離が誘導され、primingには高親和性IL-3受容体の
鎖が共通であるIL-5或いはGM-CSFによる前処置でも明らかな遊離が誘導され、primingには高親和性IL-3受容体の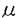 g/ml)、IL-4(10ng/ml)の存在下、非存在下にて培養し、細胞表面へのFc
g/ml)、IL-4(10ng/ml)の存在下、非存在下にて培養し、細胞表面へのFc