学位論文要旨
| No | 115487 | |
| 著者(漢字) | 澤田,大介 | |
| 著者(英字) | ||
| 著者(カナ) | サワダ,ダイスケ | |
| 標題(和) | 多機能不斉触媒を活用する光学活性Epothilone類の全合成 | |
| 標題(洋) | ||
| 報告番号 | 115487 | |
| 報告番号 | 甲15487 | |
| 学位授与日 | 2000.03.29 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(薬学) | |
| 学位記番号 | 博薬第903号 | |
| 研究科 | 薬学系研究科 | |
| 専攻 | ||
| 論文審査委員 | ||
| 内容要旨 | Epothilone類(A:1,B:2)はmyxobacteriaであるgenus Sorangiumから単離され1996年にHofleらにより構造決定された天然物である。これらはTaxolと同様の作用機序で抗ガン活性を発現することが知られており、臨床応用が期待されている。近年、Danishefsky,Nicolaou,Schinzer,Lernerらによって相次いで全合成が報告されたが、単純な化学触媒を用いる触媒的不斉合成は報告されていなかった。そこで筆者は、Epothilone類の医薬化学研究の一環として、当研究室で開発された多機能不斉触媒を用いてEpothilone類の触媒的不斉合成を達成すべく研究に着手した。 Epothilone A,Bを2つのフラグメントに分割し、Epothilone Aはfragment AとCから、Epothilone Bはfragment BとCから合成することとした。すなわち、それぞれのフラグメントを鈴木クロスカップリング後、ラクトン化により16員環を構築することとした。チアゾール環を含むfragment A,Bは、ルイス酸-ルイス塩基複合不斉触媒を用いた、触媒的不斉シアノシリル化反応を鍵工程として合成することとした。フラグメントCはエノン9に対し、多機能複合不斉触媒を用いた、触媒的不斉エポキシ化反応を行い14へ変換した後の直接的触媒的不斉アルドール反応を鍵工程として合成することとした(Scheme 1)。  文献既知のアルデヒド1に対し2をリガンドとして、触媒的不斉シアノシリル化反応を行ったところ触媒量5mol%で収率97%、不斉収率99%にてシアノヒドリン3を得ることができた。これをアルデヒド4へと変換後、トリメチルシリルアセチレンの付加を行い、パラジウムを用いて還元的に水酸基を除去し、5を得た。5に対しヒドロチタネーションを行い、酸処理にてcis-アルケンへと導き、トリメチルシリル基をヨウ素へと変換後(6)、シリル基の脱保護を行い、続いてアセチルで保護しフラグメントAを合成した(Scheme 2)。  フラグメントAの場合と同様に、触媒的不斉シアノシリル化反応を鍵工程として得られる中間体4をメチルエノールエーテルに導き、酢酸水銀で処理することにより一炭素増炭したアルデヒド7へと変換した。さらにWittig反応によってZ-ビニルヨウ素体8を合成し、続く変換によってフラグメントBを合成した。(Scheme 3)  ネオペンチルグリコールを原料として、5工程で9に導いた。これに対し、触媒的不斉エポキシ化反応を試みたが、隣接する四級炭素の立体障害のため収率、不斉収率ともに十分な結果が得られなかった。そこで、ラセミ体のまま合成を進め、後の直接的触媒的不斉アルドール反応による触媒的分割を行うこととした。9を過酸化水素水を用いてエポキシ化し、カルボニル基をメチルオキシムへと変換した。これに対し、銅試薬を用いてエポキシの開環を行い、ラネーニッケルによる還元と続く酸処理によって11へと変換した。11をLHMDSを塩基としてアリル化を行ったところ、立体選択的にアリル基の導入された12を得た。続いて立体選択的還元を行い、ジオールをアセトナイド13として保護し、ベンジル基の脱保護、酸化により、アルドール反応の原料となるアルデヒド体14に導いた(Scheme 4)。  ケトン体としてアセトフェノンを用い、触媒量20mol%で不斉アルドール反応を行ったところ、触媒支配で反応は進行しジアステレオマー15、16をそれぞれ収率30%(89%ee)、29%(88%ee)で与えた。望みのジアステレオマー15を、17をリガンドとして用いたバイアービリガー反応にて、エステル体18へと変換し、アセトナイドの除去、TBS基によるトリオールの選択的保護、酸化によりフラグメントCを合成した(Scheme 5)。  フラグメントCを超音波下、9-BBNを用いてヒドロホウ素化を行い、続いてPdCl2(dppf)を触媒とし、塩基としてリン酸カリウムを用いてフラグメントAとの鈴木クロスカップリングを行ったところ、収率50%でカップリング体が得られた。続いてアセチル基とフェニルエステル部位を同時に水酸化ナトリウム水溶液にて加水分解を行い19へと導いた。これを文献既知の方法に従い、山口法によってラクトン化を行い、TBS基の除去、最後に3,3-ジメチルジオキシランによってエポキシ化を行いEpothilone A(1)の合成に成功した(Scheme 6)。  Epothilone Aと同様の条件でフラグメントBとCの鈴木クロスカップリング反応を行ったところ、収率37%でカップリング体が得られた。以下同様にEpothilone B(2)を合成した。  筆者は当研究室で開発した多機能不斉触媒を活用した不斉シアノシリル化反応及び不斉アルドール反応を用いてすべての絶対配置を制御したエポシロン類の触媒的不斉合成を達成した。現在、収率の向上と更なる効率的合成法及び医薬化学への展開を検討中である。 | |
| 審査要旨 | Epothilone類(A:1,B:2)はmyxobacteriaであるgenus Sorangiumから単離され1996年にHofleらにより構造決定された天然物である。これらはTaxolと同様の作用機序で抗ガン活性を発現することが知られており、臨床応用が期待されている。近年、Danishefsky,Nicolaou,Schinzer,Lernerらによって相次いで全合成が報告されたが、単純な化学触媒を用いる触媒的不斉合成は報告されていなかった。そこで澤田大介は,Epothilone類の医薬化学研究の一環として、柴崎研究室で開発された多機能不斉触媒を用いてEpothilone類の触媒的不斉合成を達成すべく研究に着手した。 Epothilone A,Bを2つのフラグメントに分割し、Epothilone Aはfragment AとCから、Epothilone Bはfragment BとCから合成することとした(Scheme 1)。  文献既知の1に対し2をリガンドとして、触媒的不斉シアノシリル化反応を行ったところ触媒量5mol%で収率97%、不斉収率99%にて3を得ることができた。これをフラグメントAに変換した(Scheme 2)。  フラグメントAの場合と同様に、触媒的不斉シアノシリル化反応を鍵工程として得られる中間体4を用いてフラグメントBに変換した(Scheme 3)。  ネオペンチルグリコールを原料として、5工程で9に導いた。これに対し、触媒的不斉エポキシ化反応を試みたが、隣接する四級炭素の立体障害のため収率、不斉収率ともに十分な結果が得られなかった。そこで、ラセミ体のまま合成を進め、後の直接的触媒的不斉アルドール反応による触媒的分割を行うこととした。スキーム4のルートでアルドール反応の原料となるアルデヒド体14を得た(Scheme 4)。  ケトン体としてアセトフェノンを用い、触媒量20mol%で不斉アルドール反応を行ったところ、触媒支配で反応は進行しジアステレオマー15、16をそれぞれ収率30%(89%ee)、29%(88%ee)で与えた。望みのジアステレオマー15を、17をリガンドとして用いたバイアーピリガー反応にて、エステル体18へと変換し、アセトナイドの除去、TBS基によるトリオールの選択的保護、酸化によりフラグメントCを合成した(Scheme 5)。 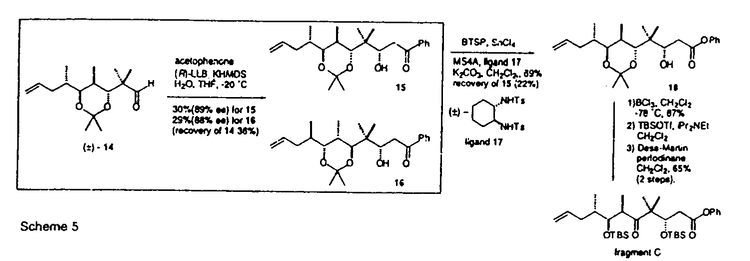 スキーム6のルートでエポシロンAを合成した。  スキーム7のルートでエポシロンBを合成した。  以上、澤田大介は柴崎研究室で開発した多機能不斉触媒を活用した不斉シアノシリル化反応及び不斉アルドール反応を用いてすべての絶対配置を制御したエポシロン類の触媒的不斉合成を達成した。本研究は医薬化学的に重要な成果であり、博士(薬学)に相当すると判断した。 | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/54775 |