学位論文要旨
| No | 124786 | |
| 著者(漢字) | 柴田,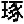 磨 磨 | |
| 著者(英字) | ||
| 著者(カナ) | シバタ,タクマ | |
| 標題(和) | Toll-like receptor (TLR)会合分子であるPRotein Associated with Tlr4 (PRAT4A)の免疫応答制御における役割 | |
| 標題(洋) | ||
| 報告番号 | 124786 | |
| 報告番号 | 甲24786 | |
| 学位授与日 | 2009.03.23 | |
| 学位種別 | 課程博士 | |
| 学位種類 | 博士(医学) | |
| 学位記番号 | 博医第3206号 | |
| 研究科 | 医学系研究科 | |
| 専攻 | 病因・病理学専攻 | |
| 論文審査委員 | ||
| 内容要旨 | 免疫システムは自己から非自己を見分けて排除する役割を担っており、多細胞生物が生命を維持する為に必須のシステムである。全ての多細胞生物は免疫システムを有し、脊椎動物では獲得免疫と自然免疫の両輪により免疫システムが構成される。自然免疫応答は病原体レセプターを用いて侵入抗原を認識し、サイトカイン(IL6、IL-12p40、TNF-αなど)やケモカイン(RANTESなど)の産生、および補助刺激分子リガンド(CD86)の発現上昇を引き起こす。その結果、適切な自然免疫応答および獲得免疫応答が誘導され、侵入病原体は排除されることとなる。 細胞膜に分布するToll Like Receptor(TLR)ファミリーは最初に発見された病原体レセプターであり、細胞外の様々な病原体構造や自己因子(TLRリガンド)を各々のTLRが特異的に認識している。これまでにTLRは様々な病原体に対する感染防御において必須であることが判明している。更に、TLRが自己免疫疾患の発症、創傷治癒、腫瘍の転移などの生体内における広範な免疫現象に関与していることも判明してきている。これらの知見は、多くの疾患におけるTLRをターゲットとした治療の可能性を示唆している。しかし、TLRのリガンド認識機構には未だ不明な点が多く、TLRを介した免疫応答を正確に制御する為にもTLRのリガンド認識を制御する機構を正確に理解していくことが求められる。 最近の研究より、TLRのリガンド認識には様々なアクセサリー分子(MD-2, CD14, UNC93B, HMGB-1, gp96など)が必要であることが判明してきた。アクセサリー分子は様々な機能によりTLRを制御しており、これら分子の解析および機能同定がTLRを介した免疫応答に対する理解を飛躍的に進展させると考えられる。 本論文において、私はTLR4のアクセサリー分子として発見されたPRotein Associated with Tlr4 ( PRAT4A)が複数のTLRの免疫応答を統合的に制御する分子であることをPRAT4Aノックアウトマウスの解析を通じて明らかにする。 PRAT4Aノックアウト(PRAT4A KO)マウスより得られた骨髄由来樹状細胞(BM-DC)、骨髄由来マクロファージ(BM-Mφ)、脾臓B細胞、マウス胚線維芽細胞(MEF)では、細胞表面に分布するTLR4、TLR1、TLR2およびTLR関連分子であるRP105の細胞表面発現が消失または減少していた。TLRファミリー以外の分子の細胞表面発現には全く影響が認められなかった。一部のPRAT4A KO細胞では、TLR2、TLR4、およびRP105の細胞表面分布が残存することより、TLRの細胞表面への移行はPRAT4Aを含めた複数の分子により制御されていると考えられる。 これらの現象に伴い、PRAT4A KO BM-DC、BM-MφおよびMEFでは、細胞表面TLR(TLR1/2, TLR2/6, TLR4)のリガンド刺激に伴うサイトカイン産生などが消失、もしくは顕著に低下していた。また、PRAT4A KO脾臓B細胞においても、それらリガンド刺激により誘導されるB細胞増殖やCD86の発現上昇が顕著に抑制されていた。この事実は、細胞表面TLRの細胞表面における分布がリガンド認識において重要であることを示している。 一方、TLR1やTLR4の細胞表面発現が完全に消失しているPRAT4A KO細胞において、これらのTLRリガンドに対する一部の免疫応答が残存もしくは全く影響を受けないという現象が認められた。この事実は、細胞表面がリガンド認識の場であると考えられている細胞表面TLRが細胞内でもリガンドを認識し得ることを強く示唆するものである。特に細胞表面におけるTLR4の分布が消失しているPRAT4A KO BM-Mφの解析より、マクロファージの細胞内TLR4は特にTRIF依存的な免疫応答を選択的に活性化することが強く示唆された。 細胞表面TLRの免疫応答に加え、全てのPRAT4A KO 細胞では細胞内TLR(TLR7, TLR9)の免疫応答も完全に消失していた。細胞内に分布するTLR9も小胞体からリソソームへ移行することが知られており、この細胞内移行がリガンド認識に必須である。RAW細胞を用いてPRAT4A欠損がTLR9の細胞内移行に与える影響を解析したところ、PRAT4AノックダウンによりGFP標識TLR9(TLR9GFP)の小胞体からリガンド認識の場であるリソソームへの移行が消失し、TLR9GFPがリガンドと出会うことが出来なくなっていた。この結果は、細胞表面TLRに加えて細胞内TLRの細胞内移行にもPRAT4Aが必須であることを示している。一方、BM-DCやBM-Mφにおいて、TLR3リガンドに対する免疫応答はPRAT4A欠損による影響を受けていなかった。 以上のin vitroの結果より、複数のTLRにおける免疫応答がPRAT4Aにより統合的に制御されていることが示された。実際の病原体は複数のTLRリガンドを有しており、PRAT4Aの欠損は病原体に対する免疫応答を顕著に消失させることが予測された。Heat-killed Mycobacterium tuberculosisやHeat-killed Escherichia coliに対するPRAT4A KO BM-DCの応答性を解析した結果、全てのサイトカイン産生は有意に低下していた。一方、これらバクテリアにより誘導される共刺激分子リガンドの誘導、即ち樹状細胞の成熟は全く影響を受けていなかった。またOVAをM.tuberculosis含有フロイント完全アジュバントと共にPRAT4A KO骨髄キメラマウスの皮下に接種したところ、OVAに対する免疫応答は認められたものの、TLRを介して誘導されるTh1偏向の免疫応答が選択的に消失していた。これらの結果は、PRAT4Aが主にサイトカイン産生のバランスを制御することで獲得免疫応答の質を変化させていることを示唆している。 更に、PRAT4AのmRNAレベルでの発現量は、様々なTLRリガンド刺激に伴って顕著に減少していた。この事実は、TLRの免疫応答がPRAT4Aの発現量の変化により制御されている可能性を強く示唆するものである。実際、PRAT4A KOキメラマウスはLPSで誘導されるエンドトキシンショックに対して完全に抵抗性であり、PRAT4Aの消失が生体内における過剰な免疫応答を抑制し得ることが示された。 以上の結果より、PRAT4AはTLRの細胞内分布を制御する分子であり、TLR3を除く複数のTLR(TLR1/2、2/6、4、5、7、9)の免疫応答に必須の分子であることが判明した。またPRAT4Aの欠損に伴うTLR応答の変化は生体内における自然免疫応答および獲得免疫応答に多大な影響を与えることが示され、TLRを介した免疫応答におけるPRAT4Aの重要性が明らかとなった。 | |
| 審査要旨 | 本研究は、Toll Like Receptor(TLR)ファミリーによる病原体因子の認識においてTLRアクセサリー分子であるPRotein Associated with Tlr4 ( PRAT4A)が果す役割を解析したものである。PRAT4A遺伝子欠損マウスの解析を通じ、下記に示すような結果を得ている。 1.PRAT4Aを欠損した骨髄由来樹状細胞(BM-DC)、骨髄由来マクロファージ(BM-Mφ)、脾臓B細胞、およびマウス胚線維芽細胞(MEF)では、細胞表面における複数のTLR(TLR1, TLR2, TLR4, RP105)の発現量が消失または減少していた。この結果は、PRAT4AがTLRの細胞表面への分布を制御する分子であることを示している。一方、PRAT4Aの欠損細胞でもTLRの細胞表面分布が残存するという現象が認められ、PRAT4Aと同様にTLRの細胞表面への移行を制御する分子機構の存在が示唆された。 2.PRAT4Aを欠損したBM-Mφ、BM-DCおよびMEFでは、細胞表面に分布するTLR(TLR4, TLR1/2, TLR2.6)のリガンド刺激に伴うサイトカイン産生が消失または顕著に減少していた。この現象は、PRAT4Aの欠損によりこれらTLRの細胞表面への分布が障害されたことに起因すると考えられ、細胞表面がリガンド認識および応答の場として重要であることが示している。一方、一部のPRAT4A欠損細胞においてはTLR1やTLR4の細胞表面分布が消失していたにも関わらず、CD40やCD86の発現上昇などはほとんど影響を受けていなかった。この事実は、細胞表面がリガンド認識の場であると考えられている細胞表面TLRが細胞内でもリガンド認識を行っていることを強く示唆するものである。 3.Balb/cバックグラウンドのBM-Mφでは、PRAT4Aの欠損によりTLR4の細胞表面分布がほとんど消失していた。同細胞では、細胞表面に分布するTLR4により誘導されることが知られるMyD88経路依存的なサイトカイン産生(TNF-α、IL-6)およびTRIF経路依存的なIFN-β産生の誘導が消失もしくは顕著に減少していた。一方、TRIF経路依存的なRANTESの産生やCD40の発現上昇の誘導はコントロール細胞と同様に誘導された。この結果は、細胞内に分布するTLR4がリガンドを認識する機能を有すること、および細胞内TLR4がTRIF依存的経路を選択的に活性化し得ることを強く示唆するものである。 4.PRAT4Aを欠損した全ての細胞では、細胞内に分布するTLR7およびTLR9のリガンド刺激に伴う免疫応答が完全に消失していた。PRAT4AをノックダウンしたRAW細胞を用いた解析より、PRAT4AはTLR9の小胞体からリガンド認識・応答の場であるリソソームへの移行を制御する分子であることが示された。一方、PRAT4Aを欠損したBM-DCおよびBM-Mφにおいて、同じく細胞内に分布するTLR3のリガンド認識は全く影響を受けなかった。 5.実際の免疫応答は複数のTLRリガンドを有する病原体に対するものである。PRAT4Aを欠損したBM-DCのHeat-killed Escherichia coli やHeat-killed Mycobacterium tuberculosisに対する免疫応答を解析した結果、サイトカイン産生はが顕著に減弱していた。一方、共刺激分子リガンドの誘導、即ち樹状細胞の成熟は全く影響を受けていなかった。またPRAT4A ノックアウトマウスより作製した骨髄キメラマウスにOVAをフロイント完全アジュバントと共に免疫したところ、TLRを介して誘導されるTh1偏向の免疫応答のみが選択的に消失していた。これらの結果は、PRAT4Aの欠損により獲得免疫応答自体が消失するのではなく、PRAT4Aの欠損に伴うサイトカイン産生の障害が獲得免疫応答の質を変化させ得ることを示している。 6.PRAT4AのmRNAレベルでの発現量は、様々なTLRリガンド刺激に伴って顕著に低下する。この事実は、TLRによる免疫応答がPRAT4Aの発現量の変化により制御されている可能性を強く示唆するものである。実際、PRAT4A KOキメラマウスはLPSで誘導されるエンドトキシンショックに対して完全に抵抗性であり、PRAT4Aの消失が生体における過剰な免疫応答を抑制し得ることが示された。 以上、本研究は複数のTLRの細胞内分布がTLRアクセサリー分子であるPRAT4Aにより統合的に制御されること、またその結果として認められたTLRの細胞内分布の変化がTLR応答に与える影響を示したものであり、リガンド認識におけるTLRの細胞内分布の重要性を明らかにしている。またPRAT4Aの欠損に伴うTLR応答の変化が生体内の自然免疫応答および獲得免疫応答に多大な影響を与えることを示し、TLRを介した免疫応答におけるTLRアクセサリー分子の重要性を明確に示している。本研究はTLRのリガンド認識機構の理解に重要な貢献をなすものであり、学位の授与に値すると考えられる。 | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/51366 |