本研究は臓器移植の際の拒絶や骨髄移植のGVH反応に重要な役割を演じているHLAクラスI抗原のうち、血清学的に同定できないためその発現と機能が明らかでなかったHLA-Cブランク抗原の発現と機能の解析を試みたものであり、下記の結果を得ている。 1.HLA-B51にリンクしたCブランク抗原遺伝子(Cb-1)をB細胞株LKT2(A2/A2,B51/B51,C-/-)よりクローニングし、HLA-A24,B52,DR2にリンクしたCブランク抗原遺伝子(Cb-2)を正常人Tm由来の末梢血リンパ球(A11/A24,B52/B52,Cw7/-)よりクローニングした。 クローニングした2つのCブランク抗原遺伝子の1次構造を他の報告されているCローカス遺伝子と比較したところCb-1とCw1の間のアミノ酸の相同性が最も高かった。これらの分子の間に5つのアミノ酸残基の置換がpeptide binding cleftの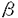 シート上のfloorに局在して見られた。このことは抗Cw1抗体(Cb-1を認識しない)はfloor上のアミノ酸残基の置換によって生じた二次的な変化を認識することを示唆している。一方Cb-2はCw2.2に最も近く全部で9つの置換が見られた。 シート上のfloorに局在して見られた。このことは抗Cw1抗体(Cb-1を認識しない)はfloor上のアミノ酸残基の置換によって生じた二次的な変化を認識することを示唆している。一方Cb-2はCw2.2に最も近く全部で9つの置換が見られた。 2.これらの遺伝子の細胞表面上での発現を見るために、マウスL細胞とHLA-Cw4のみを発現しているヒトのB細胞株Hmy2CIRに遺伝子移入しこれらの遺伝子産物を細胞表面上に発現させた。両方の遺伝子産物はこれらの細胞表面上に安定して発現したことから、HLA-Cブランク抗原は細胞表面上に発現しているが、それを検出する有効な抗血清ができない可能性が示唆された。 3.さらにヒトB細胞株Hmy2CIRに発現させたHLA-Cブランク抗原を用いてこれらの抗原に対する特異的なCTLクローンを作成し、これらを用いてCb-1およびCb-2抗原を解析した。Cb-1およびCb-2特異的なCTLクローンはHLA-Cブランク遺伝子を持った人からのEBウィルスでトランスフォームしたB細胞とPHAで誘導したT細胞を殺傷することが出来た。さらにPHAで誘導したT細胞に対するこれらのCTLクローンの反応性はHLAクラスIの共通部位を認識する単クローン抗体W6/32によって阻止された。これらの結果はHLA-Cブランク遺伝子を持った人のリンパ球表面上にHLA-Cブランク抗原が発現している事、そしてCb-1とCb-2抗原が共に抗体とCTLクローンによって検出できる事を示している。 4.次にこれらのクローンのアロ特異性を明らかにするためにHLA-Cローカスにアロ特異性を持った細胞のパネルを用いて検索した。抗Cb-1CTLクローンは他のCローカス抗原に対して交差反応性を示さずCb-1特異的であった。またB51とリンクしたCブランク抗原を持っている6つのパネル細胞のうち4つの細胞のみがこのCTLクローンにより殺傷されることから、B51とリンクしたCブランク抗原はいくつかある可能性が示唆された。一方、Cb-2抗原を認識するCTLクローンはいくつかのCローカス抗原と交差反応性を示したが、A24,B52,DR2のハプロタイプを持った5つのパネル細胞すべてを溶解する事より、このハプロタイプを持ったC抗原は1つの抗原である可能性が示唆された。 5.次に末梢血リンパ球上のCブランク抗原がアロ特異的なCTLを誘導出来るかどうか検討した。これら2つのCブランンク抗原を持っていない正常人末梢血リンパ球を応答細胞として用い、LKT2またはTmの末梢血リンパ球を刺激細胞としてCb-1またはCb-2を発現しているHmy2CIR細胞に対してCTL活性を調べたところどちらの抗原に対しても有効なCTL活性が誘導出来た。さらにHLA-Cブランク抗原を持った細胞に対する障害活性が、HLA-B51またはB52を持った細胞に対するものと同程度であることからアロ特異的CTLを誘導するHLA-Cブランク抗原の能力はHLA-B抗原よりも低くはないことが示された。 以上、本論文は血清学的に同定できない2つのHLA-Cブランク抗原が細胞表面上とヒト末梢血リンパ球上に発現しており、CTLはこれらのHLA-Cブランク抗原を認識できることを示した。そしてこれら2つのHLA-Cブランク抗原が生体内でアロ抗原として働いており、臓器移植の際の拒絶や骨髄移植のGVH反応にかかわっている可能性を示唆した。本研究はこれまで明らかでなかったHLA-Cブランク抗原の発現とアロ抗原としての機能を明らかにして臓器移植や骨髄移植の際のHLA-C抗原のタイピングの重要性を示し、移植医療に重要な貢献をなすと考えられ、学位の授与に値するものと考えられる。 |