本論文は、有用な生理活性を有する海産天然物スチポルジオンの合成を目的として、研究を行ったものであって三章よりなる。  第一章では(一)-スチポルジオン(1)の全合成の前段階として、鍵となる反応の検討を行なう目的でラセミ体で14位に水酸基を持たない(±)-14-デオキシスチポルジオン(2)の合成を検討し、その合成について述べている。第二章では、(一)-スチポルジオン(1)の合成、及び絶対立体配置の決定について述べている。第三章では(一)-スチポルジオン合成の合成法の改良を行ない、中間体である2環性化合物(3)の合成において工程数の短縮、収率の向上に成功したことについて述べている。  第一章では(±)-14-デオキシスチポルジオンの合成について述べる。 スチポルジオン(1)は1979年、W.Fenical等により、西カリブ海に繁殖する褐藻[Stypopdium zonale(Lamouroux)Papenfuss]より単離された化合物で強い魚毒活性及びウニの卵割阻害活性を示す化合物である。スチポルジオンはその分子内にオキシスピロ炭素を有しているだけでなくo-キノン構造も有しており、構造上、非常にユニークな海洋天然物である。筆者はその生理活性と構造に興味を持ち、また合成例がないことよりスチポルジオンの合成研究に着手した。 (一)-スチポルジオシ(1)の合成に際し、出発原料として2,2-ジメチル-1,3-シクロヘキサンジオン(4)のパン酵母による不斉還元で容易に得られるキラルな(S)-3-ヒドロキシ-2,2-ジメチルシクロヘキサノン(5)を用いて行うことを計画した。しかしながら3環性テルペン部分の構築方法及びスピロベンゾフラン部分の構築方法等、いくつか鍵となる反応があり、その成否いかんでは全合成に到達できない可能性がある。  そこでこれらの鍵となる反応を予め検討する必要があると考え、まずモデルでの検討を行なうことにした。そのモデルとしてはできるだけ天然物に近く、また前述の鍵となる反応を含む必要があった。そこでラセミ体でかつ14位に水酸基のない(±)-14デオキシスチポルジオン[(±)-(2)]がモデルとしてもっとも適当と考えその合成研究に着手した。  以下、実際の合成について述べる。ケトエステル体(6)を出発原料として、2工程でエステル体(7)を得た。次にエステル基を還元、メタンスルホニル化、ブロム化の3工程でブロム体(8)へと変換後、アセト酢酸メチルのジアニオンによるアルキル化、塩化第二スズによる閉環反応を行ない3環性化合物(10)へと導いた。次いで(10)に対し(6)から(8)への変換と同様の操作を行ないアリルブロミド体(11)へと変換した。 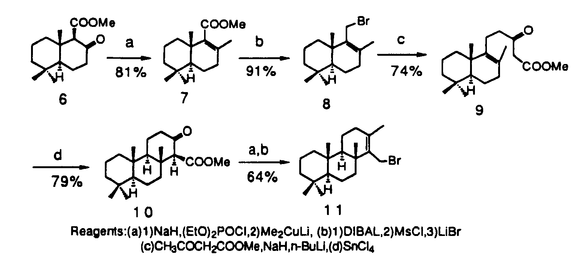 次いで有機銅試薬を用いた芳香環部分とのカップリング反応を行い(12)とした後,アリル位の酸化を行ない(13a)とした。さらに三臭化ホウ素によるMOM基の除去と分子内マイケル付加反応によるo-スピロベンゾフラン環の形成反応を行い(14)及び(13b)を得た。一部未閉環のヒドロキノン体(13b)は塩酸で処理することにより(14)と(13b)の混合物へと変換できた。ついでチオアセタール化,ラネーニッケルよる脱硫反応後,フレミー塩[(KSO3)2NO]でo-キノンへと酸化して目的の(±)-14-デオキシスチポルジオシ(2)を得ることができた。  第2章では(一)-スチポルジオンの合成について述べる。 (S)-3-ヒドロキシ-2,2-ジメチルシクロヘキサノン(5)を出発原料として森らの方法に従い,16工程で2環性化合物(15)へと変換した。次いでモデル化合物(±)-(2)の合成の時と同様に3環性ケトエステル体(16)へと導いた。エステル部分をアルコールに変換の後,(±)-(2)の合成の時と同様にアリルブロミドとして芳香環部分とのカップリルグを試みたが目的物は得られなかった。そこでアセチル化後,パラジウム(0)触媒を用いた有機スズ化合物とのカップリング反応を試みたところ高収率で(18)を得ることができた。ついで第一章と同様にアリル位の酸化を行なうとベンジル基のベンゾイル基への酸化も進行し(19)が得られた。三臭化ホウ素による脱保護,閉環反応は(±)-(2)の合成の時とほぼ同様に進行し(20)が得られた。最後にチオアセタール化,ラネーニッケルによる脱硫反応,水素化アルミニウムリチウムによるベンゾイル基の除去,フレミー塩による酸化を行い目的の(一)-スチポルジオンの(1)の最初の全合成に成功した。また比旋光度の比較により絶対立体配置が(1)式のようであることを決定することができた。  第3章では(一)-スチポルジオン合成の中間体である2環性化合物(30)の別途合成について述べる。(一)-スチポルジオンの合成の際、森らの方法に従い(S)-3-ヒドロキシ-2,2-ジメチルシクロヘキサノン(5)から中間体である2環性化合物(15)を合成した。しかしながら工程数が長く、また収率が低い(16工程、2%)ためその合成検討を行った。その結果,下記に示すようにグリニャール反応による炭素鎖の導入,ケトエステルの塩化第二スズによる閉環を利用したルートで工程数を2行程減らし(12工程)、通算収率も約3倍以上(6.7%)に上げることができた。  以上,この一連の合成研究で得た知見は天然物化学,合成化学への寄与とともに重要な医薬品等の開発への一歩となることが期待される。 |