| 内容要旨 | | I.研究の背景 劇症肝炎では凝固亢進状態と肝マクロファージ(M )の活性化が特異的な病態と推定される。そこで,本症に特徴的な広汎肝壊死の成立機序を,肝類洞壁細胞に注目して検討した。 )の活性化が特異的な病態と推定される。そこで,本症に特徴的な広汎肝壊死の成立機序を,肝類洞壁細胞に注目して検討した。 II.クッバー(K)細胞及び肝M の活性状態を生体内で評価する方法の開発 の活性状態を生体内で評価する方法の開発 K細胞や肝M の活性化は,responsive stageから,細胞障害性を有するprimed stageへと段階的に進行し,また,その活性状態は小葉内域や壊死巣との関連でheterogeneityが存在すると考えられる。従って,広汎肝壊死におけるこれら細胞の役割を明確にするためには,in situで活性段階も考慮した検討が必要となる。そこで,in vitroでのM の活性化は,responsive stageから,細胞障害性を有するprimed stageへと段階的に進行し,また,その活性状態は小葉内域や壊死巣との関連でheterogeneityが存在すると考えられる。従って,広汎肝壊死におけるこれら細胞の役割を明確にするためには,in situで活性段階も考慮した検討が必要となる。そこで,in vitroでのM 機能評価に用いられているnitro blue tetrazolium (NBT)による活性酸素産生能測定法を応用し,新たな方法の開発を試みた。 機能評価に用いられているnitro blue tetrazolium (NBT)による活性酸素産生能測定法を応用し,新たな方法の開発を試みた。 1)方法 実験1:ラットに四塩化炭素を経口投与またはCorynebacterium parvum加熱死菌を静注し,NBT肝灌流を施行した。実験2:同様に処置したラットから肝M を単離し,phorbol myristate acetate(PMA)刺激による活性酸素産生能を測定した。 を単離し,phorbol myristate acetate(PMA)刺激による活性酸素産生能を測定した。 2)成績 実験1:正常肝,四塩化炭素投与肝,死菌投与肝ともホルマザン沈着が観察された類洞壁細胞は非特異的エステラーゼ染色陽性であり,K細胞ないし肝M であると同定された。PMAを添加しないNBT肝灌流では,全群肝類洞壁細胞に沈着は認められなかった。PMAを添加すると,正常肝では門脈域周囲から中間帯のK細胞に軽度の,四塩化炭素投与肝では中心静脈域壊死巣内の,死菌投与肝では肝全体のM であると同定された。PMAを添加しないNBT肝灌流では,全群肝類洞壁細胞に沈着は認められなかった。PMAを添加すると,正常肝では門脈域周囲から中間帯のK細胞に軽度の,四塩化炭素投与肝では中心静脈域壊死巣内の,死菌投与肝では肝全体のM に著明な沈着が観察された。PMAに加えてCu(Lys)2を添加すると,全群沈着は消失した。SODを添加すると,四塩化炭素投与肝における沈着は非添加の際と変わりなかったが,死菌投与肝では軽減した。実験2:NBT還元法では,四塩化炭素投与肝,死菌投与肝ともM に著明な沈着が観察された。PMAに加えてCu(Lys)2を添加すると,全群沈着は消失した。SODを添加すると,四塩化炭素投与肝における沈着は非添加の際と変わりなかったが,死菌投与肝では軽減した。実験2:NBT還元法では,四塩化炭素投与肝,死菌投与肝ともM の活性酸素産生能は正常肝K細胞に比し上昇していたが,両群間での差は認められなかった。化学発光法では,四塩化炭素投与肝M の活性酸素産生能は正常肝K細胞に比し上昇していたが,両群間での差は認められなかった。化学発光法では,四塩化炭素投与肝M と正常肝K細胞で活性酸素産生能に差は見られなかったが,死菌投与肝M と正常肝K細胞で活性酸素産生能に差は見られなかったが,死菌投与肝M では著明に上昇していた。 では著明に上昇していた。 3)考案 四塩化炭素障害肝におけるM の活性化は壊死の結果であり,これらはresponsive stageの浸出性M の活性化は壊死の結果であり,これらはresponsive stageの浸出性M に相当する。一方,死菌投与後の肝M に相当する。一方,死菌投与後の肝M は,excitationを起こすと腫瘍細胞障害性を有することから,primed stageまで活性化していると推定された。そこで,これら活性段階が明らかな肝M は,excitationを起こすと腫瘍細胞障害性を有することから,primed stageまで活性化していると推定された。そこで,これら活性段階が明らかな肝M を対象に検討を行なった。 を対象に検討を行なった。 NBT肝灌流後のホルマザン沈着は,非特異的エステラーゼ染色陽性の類洞壁細胞でPMA添加時にのみ観察されたこと,及び細胞膜透過性の活性酸素除去剤であるCu(Lys)2を更に添加すると消失したことから,K細胞や肝M におけるrespiratory burstを反映していると考えられた。細胞膜非透過性の活性酸素除去剤であるSODを添加した場合の沈着の変化から,四塩化炭素投与後及び死菌投与後の肝M におけるrespiratory burstを反映していると考えられた。細胞膜非透過性の活性酸素除去剤であるSODを添加した場合の沈着の変化から,四塩化炭素投与後及び死菌投与後の肝M は,それぞれ食胞膜における細胞内,形質膜における細胞外への活性酸素産生能が亢進していると考えられた。前者はresponsive stageにおける貪食能,後者はprimed stageにおける分泌能の亢進を反映していると推定された。これは,細胞外へ分泌された活性酸素を検出する化学発光法では,死菌投与肝M は,それぞれ食胞膜における細胞内,形質膜における細胞外への活性酸素産生能が亢進していると考えられた。前者はresponsive stageにおける貪食能,後者はprimed stageにおける分泌能の亢進を反映していると推定された。これは,細胞外へ分泌された活性酸素を検出する化学発光法では,死菌投与肝M における活性酸素産生能のみが亢進していたin vitroの成績と一致した所見である。以上より,NBT肝灌流により,肝M における活性酸素産生能のみが亢進していたin vitroの成績と一致した所見である。以上より,NBT肝灌流により,肝M の活性段階をin situで判定可能と考えられた。 の活性段階をin situで判定可能と考えられた。 III.各種ラット肝病態における肝M の活性状態 の活性状態 肝病態下では肝M の機能が変化するが,これらが新たな病態を惹起する可能性がある。特に,primed stageの肝M の機能が変化するが,これらが新たな病態を惹起する可能性がある。特に,primed stageの肝M は各種因子の産生能が亢進しているだけに注目される。そこで,代表的な肝病態モデルを対象に,primingの惹起因子につき検討した。 は各種因子の産生能が亢進しているだけに注目される。そこで,代表的な肝病態モデルを対象に,primingの惹起因子につき検討した。 1)方法 ラットで以下の処置を行ない,PMA添加NBT肝灌流を施行した。肝M 内ホルマザン沈着の程度は,正常肝門脈域K細胞を1度,四塩化炭素投与肝壊死巣内及び死菌投与肝のM 内ホルマザン沈着の程度は,正常肝門脈域K細胞を1度,四塩化炭素投与肝壊死巣内及び死菌投与肝のM をそれぞれ3,5度として半定量的に分類した。実験1:Dimethylnitrosamineを腹腔内投与した。Gum arabicはその3日前より連日腹腔内投与を続けた。実験2:Atraumatic clampを用いて左外側葉,中葉への肝血流を30分間遮断した。実験3:70%肝部分切除術を施行した。実験4:ブタ血清を週2回,12週間腹腔内投与した。実験5:Lieberの方法でエタノール含有飼料による対飼育を6週間行なった。実験6:黄疸発症及び未発症のLECラットを対象とした。 をそれぞれ3,5度として半定量的に分類した。実験1:Dimethylnitrosamineを腹腔内投与した。Gum arabicはその3日前より連日腹腔内投与を続けた。実験2:Atraumatic clampを用いて左外側葉,中葉への肝血流を30分間遮断した。実験3:70%肝部分切除術を施行した。実験4:ブタ血清を週2回,12週間腹腔内投与した。実験5:Lieberの方法でエタノール含有飼料による対飼育を6週間行なった。実験6:黄疸発症及び未発症のLECラットを対象とした。 2)成績 実験1:Dimethylnitrosamine投与肝の壊死巣内肝M には3度のホルマザン沈着が観察されたが,gum arabic投与を行なった群では壊死巣内に淡明化した大型M には3度のホルマザン沈着が観察されたが,gum arabic投与を行なった群では壊死巣内に淡明化した大型M が集簇し,これらは沈着が認められなかった。実験2:血流遮断解除30分後の肝では壊死像は認められず,肝全体のK細胞に1度の沈着が観察された。実験3:70%肝部分切除24〜72時間後には,肝全体のM が集簇し,これらは沈着が認められなかった。実験2:血流遮断解除30分後の肝では壊死像は認められず,肝全体のK細胞に1度の沈着が観察された。実験3:70%肝部分切除24〜72時間後には,肝全体のM で4〜5度の沈着が観察された。これらでSODを添加したNBT肝灌流を行うと,沈着は2度まで軽減した。実験4:肝は門脈-肝静脈間及び肝静脈相互間が線維束で連絡し,線維束内M で4〜5度の沈着が観察された。これらでSODを添加したNBT肝灌流を行うと,沈着は2度まで軽減した。実験4:肝は門脈-肝静脈間及び肝静脈相互間が線維束で連絡し,線維束内M に1度の沈着が観察された。実験5:エタノール含有飼料で飼育したラットでは,門脈域周囲から中間帯で2度,中心静脈域で1度の沈着を有するM に1度の沈着が観察された。実験5:エタノール含有飼料で飼育したラットでは,門脈域周囲から中間帯で2度,中心静脈域で1度の沈着を有するM が観察された。実験6:尿中ビリルビン陽性LECラットでは,肝細胞の巨核化と巣状壊死巣が観察され,肝M が観察された。実験6:尿中ビリルビン陽性LECラットでは,肝細胞の巨核化と巣状壊死巣が観察され,肝M の沈着は壊死部で3度,非壊死部で1度であった。ビリルビン陰性ラットでは,門脈域周囲から中間帯の肝M の沈着は壊死部で3度,非壊死部で1度であった。ビリルビン陰性ラットでは,門脈域周囲から中間帯の肝M に1〜2度の沈着が観察された。 に1〜2度の沈着が観察された。 3)考案 壊死,再生,線維化及び循環障害など肝における代表的な病態及びアルコール摂取が肝M 機能に与える影響を検討した。壊死巣内やアルコール投与後の肝M 機能に与える影響を検討した。壊死巣内やアルコール投与後の肝M は活性化していたが,その活性段階はresponsive stageであった。線維化の過程や循環障害によっては,肝M は活性化していたが,その活性段階はresponsive stageであった。線維化の過程や循環障害によっては,肝M の活性段階は変わらなかった。しかし,70%肝部分切除後は,死菌投与後と同様に肝M の活性段階は変わらなかった。しかし,70%肝部分切除後は,死菌投与後と同様に肝M がprimed stageまで活性化しており,excitationを生じた場合は肝障害が惹起されると考えられた。なお,gum arabicを前投与すると,肝壊死巣には活性段階が低下した肝M がprimed stageまで活性化しており,excitationを生じた場合は肝障害が惹起されると考えられた。なお,gum arabicを前投与すると,肝壊死巣には活性段階が低下した肝M が集簇することから,この高分子多糖体はin vivoで肝M が集簇することから,この高分子多糖体はin vivoで肝M 機能を抑制する際に有用であると考えられた。 機能を抑制する際に有用であると考えられた。 III.肝M の活性化に起因するラット広汎肝壊死モデルの作製 の活性化に起因するラット広汎肝壊死モデルの作製 死菌を投与したラットでは,肝M がprimed stageまで活性化しており,エンドトキシン(LPS)を静注すると通常は肝障害を惹起しない少量でも広汎肝壊死が誘発される。肝部分切除後の肝M がprimed stageまで活性化しており,エンドトキシン(LPS)を静注すると通常は肝障害を惹起しない少量でも広汎肝壊死が誘発される。肝部分切除後の肝M も同様に活性化していることから,LPS静注により同様の肝障害が成立すると想定し,新しい広汎肝壊死モデルの作製を試みた。 も同様に活性化していることから,LPS静注により同様の肝障害が成立すると想定し,新しい広汎肝壊死モデルの作製を試みた。 1)方法 実験1:ラットに70%肝部分切除またはシャム手術を行ない,48時間後にLPSを静注した。12時間後の生存率と死亡ラットの肝組織像を検討した。実験2:同様に処置したラットで,LPS静注5時間後に下大静脈より採血して肝機能を測定,肝は摘出して光顕及び電顕による観察を行なった。実験3:死菌投与7日後のラットにLPSを静注し,肝機能測定と肝の組織学的検索を同様に行った。 2)成績 実験1:肝部分切除後にLPSを投与したラットは50%が死亡したのに対し,生食を投与したラットは全例が生存した。死亡ラットの肝では広汎な出血性凝固壊死巣が観察された。シャム手術を施行したラットは3倍量のLPSを投与したが,死亡例は認められなかった。実験2:肝部分切除後にLPSを投与したラットでは,有意な血清ALT活性上昇とプロトロンビン時間(PT)延長が認められ,肝には中間帯を中心とした凝固壊死巣が観察された。電顕観察では,肝類洞内のM に接したフィブリン沈着と,その近傍における類洞内皮細胞の破壊像が認められた。実験3:死菌を投与したラットでは,肝類洞内へのM に接したフィブリン沈着と,その近傍における類洞内皮細胞の破壊像が認められた。実験3:死菌を投与したラットでは,肝類洞内へのM 浸潤と肉芽腫形成が観察されたが,壊死巣は認められなかった。死菌投与後にLPSを静注すると,血清ALT活性は上昇, PTは延長し,肝には凝固壊死巣が観察された。電顕観察では類洞内皮細胞の破綻と類洞内フィブリン沈着が認められた。 浸潤と肉芽腫形成が観察されたが,壊死巣は認められなかった。死菌投与後にLPSを静注すると,血清ALT活性は上昇, PTは延長し,肝には凝固壊死巣が観察された。電顕観察では類洞内皮細胞の破綻と類洞内フィブリン沈着が認められた。 3)考案 70%肝部分切除を行なったラットに少量のLPSを静注すると,死歯投与後のラットと同様に広汎肝壊死が誘発された。肝の組織学的検索では,両モデルとも小葉中間帯を中心とした出血性凝固壊死巣が観察され,電顕では類洞内フィブリン沈着と類洞内皮細胞の破壊像が認められた。肝類洞内フィブリン沈着は類洞内皮細胞障害が惹起された場合のみ出現し,微小循環障害から肝壊死の原因となることを,dimetylnitrosamine障害肝における検討から我々は明らかにしている。従って,両モデルとも類洞内凝固に起因する微小循環障害が広汎肝壊死の成立に関与していると推定された。また,肝障害はLPS静注後のみに出現したことから,肝M はexcitationを起こして障害成立に関与すると推定された。 はexcitationを起こして障害成立に関与すると推定された。 V.広汎肝壊死成立における肝微小循環障害の意義と肝M の役割 の役割 70%肝部分切除後ないし死菌投与後に少量のLPSを静注して誘発する広汎肝壊死では,微小循環障害とM のprimingが生じているが,これらと肝障害との関係を明らかにする目的で各種治療実験を施行した。 のprimingが生じているが,これらと肝障害との関係を明らかにする目的で各種治療実験を施行した。 2)方法 ラットに死菌投与または70%肝部分切除を行ない,それぞれ7日,48時間後にLPSを静注した。5時間後に採血して肝機能を測定,肝は摘出して組織学的検索を行った。実験1:アンチトロンビン(AT)III濃縮製剤をLPSと同時に静注した。実験2:LPS静注24時間前に抗ラット好中球ウサギ抗血清を静注した。実験3:死菌投与または肝部分切除の3日前からLPS静注前日まで,gum arabicを連日腹腔内投与した。また,同様にgum arabicを投与したラットでPMA添加NBT肝灌流を施行した。実験4:LPS静注24時間前に塩化ガドリニウムを静注した。 3)成績 実験1:ATIII製剤投与により,死菌投与群,肝部分切除群とも血漿ATIII活性及びトロンビン-ATIII複合体濃度が上昇し,肝障害は改善した。実験2:抗血清投与により両群とも末梢血好中球数は対照の約1%まで低下したが, LPS静注後の肝障害には改善が認められなかった。実験3:Gum arabic投与により,両群ともPMA添加NBT肝灌流後の肝M 内ホルマザン沈着は著減し,LPS静注後の肝障害が軽減した。実験4:死菌投与群では塩化ガドリニウム投与により肝障害が軽減したが,肝部分切除ラットでは改善は認められなかった。 内ホルマザン沈着は著減し,LPS静注後の肝障害が軽減した。実験4:死菌投与群では塩化ガドリニウム投与により肝障害が軽減したが,肝部分切除ラットでは改善は認められなかった。 4)考案 死菌投与後及び肝部分切除後のLPS誘発障害肝モデルでは,血漿トロンビンーATIII複合体濃度は増加しており,抗凝固療法で血漿ATIII活性を100%以上に維持すると,更に上昇が認められた。従って,これらラットは血中に遊離トロンビンが存在し,過凝固状態にあると考えられた。両モデルとも肝障害が抗凝固療法で改善し,更に電顕観察では類洞内フィブリン沈着が認められたことから,この過凝固状態は類洞内凝固から微小循環障害を惹起し,広汎肝壊死の原因になると推定された。 肝類洞内凝固を惹起する細胞としては,先ず好中球に注目した。しかし,抗血清投与で末梢血好中球が枯渇しても肝障害は改善せず,両モデルとも好中球の関与は否定的であった。一方,K細胞や肝M の関与は,gum arabicを過貪食させ活性化を抑制すること,ないし塩化ガドリニウム投与で大型M の関与は,gum arabicを過貪食させ活性化を抑制すること,ないし塩化ガドリニウム投与で大型M を破壊することにより検討した。両モデルともgum arabic投与で肝障害が改善したことから,その成立に肝M を破壊することにより検討した。両モデルともgum arabic投与で肝障害が改善したことから,その成立に肝M が関与するのは明らかである。しかし,塩化ガドリニウムの効果が死菌モデルでのみ観察されたことから,両モデルの肝M が関与するのは明らかである。しかし,塩化ガドリニウムの効果が死菌モデルでのみ観察されたことから,両モデルの肝M の活性状態及び類洞内凝固成立機序には差異があると推定された。 の活性状態及び類洞内凝固成立機序には差異があると推定された。 その後の検討から,両モデルの肝M はともにPMA刺激に対する活性酸素産生が亢進しているが,LPSで刺激した際の産生は死菌投与肝M はともにPMA刺激に対する活性酸素産生が亢進しているが,LPSで刺激した際の産生は死菌投与肝M でのみ高値であることが判明した。また,LPS静注後の血清TNF でのみ高値であることが判明した。また,LPS静注後の血清TNF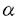 濃度は死菌モデルでのみ著高を示し,抗TNF 濃度は死菌モデルでのみ著高を示し,抗TNF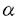 抗体やSODを用いた治療実験もこのモデルでのみ有効であった。更に,凝固の生じ得ない閉鎖肝灌流系で肝M 抗体やSODを用いた治療実験もこのモデルでのみ有効であった。更に,凝固の生じ得ない閉鎖肝灌流系で肝M の標的細胞を検討したところ,死菌投与肝M の標的細胞を検討したところ,死菌投与肝M は肝細胞に対する障害性はないが類洞内皮細胞を破壊することが,部分切除肝M は肝細胞に対する障害性はないが類洞内皮細胞を破壊することが,部分切除肝M は肝細胞のみならず類洞内皮細胞に対する直接障害性も有さないことが明らかとなった。従って,死菌モデルでは,肝M は肝細胞のみならず類洞内皮細胞に対する直接障害性も有さないことが明らかとなった。従って,死菌モデルでは,肝M が放出する障害因子が類洞内皮細胞を直接破壊し,その結果類洞内凝固が惹起され,広汎肝壊死が成立すると考えられた。一方,部分切除肝M が放出する障害因子が類洞内皮細胞を直接破壊し,その結果類洞内凝固が惹起され,広汎肝壊死が成立すると考えられた。一方,部分切除肝M は凝固の惹起因子であるtissue factor活性が著増していた。部分切除肝では,類洞内皮細胞のトロンボモジュリンの発現が正常肝と同様に軽微であることから,このモデルでは肝M は凝固の惹起因子であるtissue factor活性が著増していた。部分切除肝では,類洞内皮細胞のトロンボモジュリンの発現が正常肝と同様に軽微であることから,このモデルでは肝M と類洞内皮細胞間における凝固平衡が破綻する結果類洞内凝固が成立し,二次的に類洞内皮細胞が破壊されると推定している。 と類洞内皮細胞間における凝固平衡が破綻する結果類洞内凝固が成立し,二次的に類洞内皮細胞が破壊されると推定している。 VI.肝微小循環障害成立における肝M と類洞内皮細胞間接着の意義 と類洞内皮細胞間接着の意義 LPS誘発肝障害の成立機序は死菌投与後と肝部分切除後では異なるが,活性化肝M と類洞内皮細胞間の相互作用が肝微小循環障害を誘発する点は共通している。そこで,両細胞間の相互作用を接着分子との関連で検討した。 と類洞内皮細胞間の相互作用が肝微小循環障害を誘発する点は共通している。そこで,両細胞間の相互作用を接着分子との関連で検討した。 2)方法 実験1:ラットに死菌投与または70%肝部分切除を行ない,それぞれ7日,48時間後にLPSを静注した。経時的に肝を摘出,ICAM-1及びLFA-1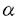 の発現を酵素抗体間接法で検討した。実験2:抗ラットICAM-1及びLFA-1 の発現を酵素抗体間接法で検討した。実験2:抗ラットICAM-1及びLFA-1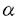 単クロン抗体,または正常マウスIgGを連日腹腔内投与した。4日目に死菌投与ないし9日目に70%肝部分切除を施行し,両群11日目にLPSを静注した。5時間後に肝機能を測定,肝は摘出して組織学的検索を行った。実験3:同様に抗体を投与し,4日目に死菌投与,11日目にPMA添加NBT肝灌流を施行した。 単クロン抗体,または正常マウスIgGを連日腹腔内投与した。4日目に死菌投与ないし9日目に70%肝部分切除を施行し,両群11日目にLPSを静注した。5時間後に肝機能を測定,肝は摘出して組織学的検索を行った。実験3:同様に抗体を投与し,4日目に死菌投与,11日目にPMA添加NBT肝灌流を施行した。 3)成績 実験1:正常肝では,小葉全体の類洞内皮細胞にICAM-1,門脈域周囲のK細胞にLFA-1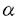 が軽度染色された。死菌投与7日後及び肝部分切除48時間後の肝では,類洞内皮細胞のICAM-1及びM が軽度染色された。死菌投与7日後及び肝部分切除48時間後の肝では,類洞内皮細胞のICAM-1及びM のLFA-1 のLFA-1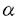 染色性が正常肝に比し強度であり,これらはLPS静注後,肝壊死巣出現に先行して更に増強した。実験2:死菌投与ラットでは,抗体投与で血清ALT活性と凝固系の異常及び組織学的肝障害の程度が軽減したが,肝部分切除ラットではこれらが増悪した。実験3:抗体投与により,肝重量体重比,肉芽腫数と大きさ及びNBT肝灌流後の肝M 染色性が正常肝に比し強度であり,これらはLPS静注後,肝壊死巣出現に先行して更に増強した。実験2:死菌投与ラットでは,抗体投与で血清ALT活性と凝固系の異常及び組織学的肝障害の程度が軽減したが,肝部分切除ラットではこれらが増悪した。実験3:抗体投与により,肝重量体重比,肉芽腫数と大きさ及びNBT肝灌流後の肝M 内ホルマザン沈着には変化は認められかった。 内ホルマザン沈着には変化は認められかった。 4)考案 両モデルとも,類洞内皮細胞におけるICAM-1及び肝M におけるLFA-1発現が肝壊死出現に先行して高度であったことから,類洞内凝固の成立する時期に肝M におけるLFA-1発現が肝壊死出現に先行して高度であったことから,類洞内凝固の成立する時期に肝M と類洞内皮細胞は接着していると考えられた。一方,肝細胞はICAM-1発現が観察されなかったことから,同時期に肝M と類洞内皮細胞は接着していると考えられた。一方,肝細胞はICAM-1発現が観察されなかったことから,同時期に肝M と接着することはないと推定された。In vivoでは,M と接着することはないと推定された。In vivoでは,M が肝細胞を直接障害することはない。この現象は接着分子発現との関連で捉えることも可能であろう。 が肝細胞を直接障害することはない。この現象は接着分子発現との関連で捉えることも可能であろう。 抗接着分子抗体投与により,死菌モデルでは肝障害が改善したのに対し肝部分切除モデルでは逆に増悪した。抗体投与はM の肝浸潤や活性段階に影響を与えなかったことから,その効果は肝M の肝浸潤や活性段階に影響を与えなかったことから,その効果は肝M -類洞内皮細胞間の接着抑制に起因すると考えられた。死菌モデルでは,両細胞の接着解除で類洞内皮細胞が晒される細胞障害性因子濃度が低くなり,障害が改善すると推定された。一方,肝部分切除モデルでは,M -類洞内皮細胞間の接着抑制に起因すると考えられた。死菌モデルでは,両細胞の接着解除で類洞内皮細胞が晒される細胞障害性因子濃度が低くなり,障害が改善すると推定された。一方,肝部分切除モデルでは,M の凝固活性が上昇して凝固を惹起している可能性があり,抗体投与で肝M の凝固活性が上昇して凝固を惹起している可能性があり,抗体投与で肝M と類洞内皮細胞間の接着が解除されると,類洞内皮細胞に存在する抗凝固系の作用が不十分となり,類洞内凝固が逆に増悪したものと推定された。 と類洞内皮細胞間の接着が解除されると,類洞内皮細胞に存在する抗凝固系の作用が不十分となり,類洞内凝固が逆に増悪したものと推定された。 VII.結語 劇症肝炎に特徴的である広汎肝壊死の成立には活性化肝M により惹起される類洞内皮細胞障害,類洞内凝固が重要であり,この過程は接着分子を介する肝M により惹起される類洞内皮細胞障害,類洞内凝固が重要であり,この過程は接着分子を介する肝M ・類洞内皮細胞間相互作用により調節されていることが明かとなった。 ・類洞内皮細胞間相互作用により調節されていることが明かとなった。 |
| 審査要旨 | | 本研究は,劇症肝炎に特徴的な広汎肝壊死の成立機序を,肝局所の要因に注目して解明することを目的としている。特に,劇症肝炎では凝固亢進状態と肝マクロファージ活性化の存在が特異的病態と推定されることから,肝類洞壁細胞の関与につき各種実験を行ない,下記のの成績を得ている。 1.Phorbl myristate acetate(PMA)とnitro blue tetrazolium(NBT)による肝灌流後の肝マクロファージ内ホルマザン沈着を光顕観察することにより,その活性段階をin situで評価する方法を開発した。 2.各種ラット病態肝でPMA添加NBT肝灌流を施行することにより,Corynebacterium parvum死菌投与後及び70%肝部分切除後の肝マクロファージは細胞障害因子産生能に富んだprimed stageまで活性化していることを明らかにした。 3.肝マクロファージがprimed stageにあるこれらラットでは,正常ラットには肝障害を生じ得ない極少量のエンドトキシンを投与することにより広汎肝壊死が惹起されることを見出した。 4.これら広汎肝壊死モデルでは,類洞内フィブリン沈着が電顕観察され,またアンチトロンビンIII濃縮製剤による抗凝固療法で肝障害が改善することから,肝壊死の原因は類洞内凝固に起因する微小循環障害であることを明かとした。 5.両モデルとも類洞内凝固は類洞内皮細胞障害を伴っていたが,その成立には好中球でなく肝マクロファージが関与することを証明した。その際,エンドトキシン刺激に対するマクロファージの反応性や類洞内凝固を惹起する機序は両モデル間で異なっていことを見いだした。 6.両モデルとも,類洞内凝固成立時には肝マクロファージと類洞内皮細胞は接着分子であるLFA-1,ICAM-1を介して接着していると考えられた。更に,死菌投与モデルではこの接着が類洞内凝固を促進的に,肝部分切除モデルでは抑制的に調節していることを証明した。 以上,本論分は,劇症肝炎に特徴的である広汎肝壊死の成立には活性化肝マクロファージにより惹起される類洞内皮細胞障害,類洞内凝固が重要であり,この過程は接着分子を介する肝マクロファージ・類洞内皮細胞間相互作用により調節されていることを明かにした。劇症肝炎の成立機序に関しては,ウイルス側の要因及び生体の免疫反応に注目した検討が行われてきたが,肝局所の要因に関しては全く未知であった。本研究は,この新たな分野の解明を試みた最初の仕事であり,劇症肝炎の病態解明を介しその治療法確立に際する貢献は大きく,学位の授与に値するものと考えられる。 |