学位論文要旨
| No | 212314 | |
| 著者(漢字) | 大島,章弘 | |
| 著者(英字) | ||
| 著者(カナ) | オオシマ,アキヒロ | |
| 標題(和) | 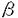 -ガラクトシドーシス : 遺伝子情報と疾病発現 -ガラクトシドーシス : 遺伝子情報と疾病発現 | |
| 標題(洋) | ||
| 報告番号 | 212314 | |
| 報告番号 | 乙12314 | |
| 学位授与日 | 1995.04.26 | |
| 学位種別 | 論文博士 | |
| 学位種類 | 博士(医学) | |
| 学位記番号 | 第12314号 | |
| 研究科 | ||
| 専攻 | ||
| 論文審査委員 | ||
| 内容要旨 | 1群は、ほとんど全く活性を失う変異遺伝子群で、多くの種類の種類の変異で起こり、頻度的にも多い。どのような変異であれ、この群に属する変異遺伝子のホモ接合体とこの群に属する2種の異常を含む複合へテロ接合体の臨床型はGM1ガングリオシドーシス乳児型として表現される。多くの変異遺伝子はこの群に属し、乳児型に収れんされる。 もう1群は、限界閾値以下の残存活性を発現する変異遺伝子群である。この変異群は一般に頻度が低いと考えられ、全く活性のない群とたまたま複合ヘテロ接合体になったときと、血族結婚でホモ接合体になったときに軽症型(幼児型成人型)として表現されると考えられる。 残存活性を有する群の変異遺伝子をまったく活性のない乳児型GM1ガングリオシドーシス細胞に遺伝子導入し、その性質を検討した。残存活性のあるGM1ガングリオシドーシス変異遺伝子発現産物は、プロセシングに障害があった。この異常を患者線維芽細胞で確認した。表1に幼児型及び成人型GM1ガングリオシドーシスとモルキオB病を決定する変異遺伝子のプロセシング障害を示す。遺伝子変異は異なっても、GM1ガングリオシドーシス幼児型変異遺伝子発現産物は保護タンパクとの複合体形成障害を、GM1ガングリオシドーシス成人型変異はリソソームへの輸送障害を認めた。これが、酵素欠損の主要な原因であると考えられる。これに対して、モルキオB病変異遺伝子発現産物はプロセシング障害を認めなかった。酵素活性の主要な部分は、リソソーム内で保護タンパクと高分子複合体を形成していると考えられる。  それぞれの臨床型を決定する変異遺伝子発現産物は、遺伝子上の変異の位置変異は異なっても、共通した分子病理を示すことから、この違いがGM1ガングリオシドーシスとモルキオB病の臨床症状の違いに関係すると考えられた。このことは保護タンパクとの高分子複合体が、ガングリオシドGM1の代謝に重要な役割を持つことを示唆すると思われる。図1に現在までの変異遺伝子発現産物細胞病理と臨床型の対応を示す。 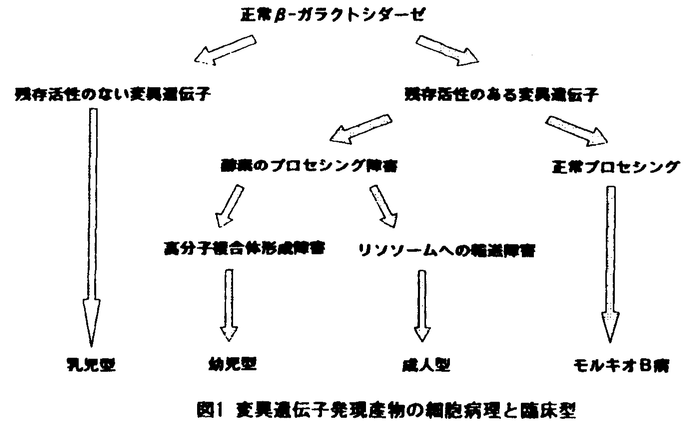 幼児型変異遺伝子をもつ患者線維芽細胞では、その活性低下の機構から予想されるように、ガラクトシアリドーシス細胞と同様、いくつかのプロテアーゼ阻害剤で活性の回復を示した。将来有効なプロセアーゼ阻害剤が開発されれば、幼児型GM1ガングリオシドーシスについては治療の可能性を検討する必要があると思われた。 | |
| 審査要旨 | 本研究は、 1. 2.COS細胞にGP8を遺伝子導入し発現タンパクの解析を行なった。発現タンパクは内因性の 3.GP8の塩基配列をもとに 4.表現型と遺伝子型の相関と変異遺伝子発現産物の残存活性を検討することで、 5.幼児型GM1-ガングリオシドーシスに関係する変異遺伝子(R201H,R201C)発現産物は、共に保護タンパクとの高分子複合体形成障害を認めた。GM1-ガングリオシドーシス成人型に関係する変異遺伝子(I51T,T82M)の発現産物は、共にリソソームへの輸送障害が考えられた。モルキオB病に関係する変異遺伝子(Y83H,W273L)は、プロセシング異常は認めなかったが、分子あたりの活性が低いことが酵素欠損の原因と考えられた。以上より、GM1-ガングリオシドーシスの発病には変異タンパク分子の基質にたいする触媒能のみならず、リソソームへの輸送や保護タンパクとの高分子複合体形成を含んだプロセシングの異常が強く関係することが示された。 以上、本論文は | |
| UTokyo Repositoryリンク | http://hdl.handle.net/2261/53916 |
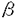 -ガラクトシダーゼ遺伝子本体の異常によりおこる遺伝病としてGM1-ガングリオシドーシスとモルキオB病がある(
-ガラクトシダーゼ遺伝子本体の異常によりおこる遺伝病としてGM1-ガングリオシドーシスとモルキオB病がある(