| はじめに SwinholideAは、1985年Kashmanらにより紅海産の海綿Theonella swinhoeiより抗薗活性を指標として単離され、その構造はモノメリックな22員環マクロライドであると報告された。しかし、1990年に北川らは沖縄産の同種の海綿よりSwinholideAを単離して構造の再検討を行い、このものが1の絶対構造を有することを明らかにした。SwinholideA(1)は特異な44員環構造を持つ2量体マクロライドであり、かつ強い抗腫瘍活性を示すことから合成的にも薬理学的にも興味深い化合物である。さらに近年、1の生合成前駆体と考えられるPre-swinholideA(2)が天然より見い出されたことが報告された。  SwinholideA(1)の構造類似の天然物としては、その同族体であるSwinholideB-Gのほか、八丈島産あるいは沖縄産の海綿より得られたBistheonellide(Misakiaolide)類、陸生の藍藻より単離されたScytophyciaCなどの存在が知られている。 筆者の所属する研究室では多官能性生理活性天然物の合成研究を展開しているが、今回筆者は、Swinholide系天然物の合成研究の一環として、一連の天然物合成に共通な重要中間体3を目標化合物として設定し、このものの立体選択的合成に成功した。  合成計画 逆合成を以下に示す。目標化合物3に相当するAはBとCのジアステレオ選択的アルドール反応により合成でき、BおよびCは、それぞれDとHより変換可能であろう。Dは当研究室で開発された1,3-ポリオールのコンバージェント合成法によってアルデヒドGより得られるケトンFを経てメチル体Eから合成することとした。その際、左右対称なEの保護基をいかに区別して除去するかが問題となる。  C9側鎖の立体選択的構築の検討 まず、目的物3のベンジリデン保護基の妥当性を確認するために、モデル化合物を用いてC9側鎖の立体選択的構築を検討した。すなわち、L-malic acidよりベンジリデン4(3に相当)を合成し、これより得られる , , -不飽和ラクトンSをDIBAH還元,ついでメチル化することによりアセタール6に導いた。これにBF1・Et2Oの存在下、AllylTMSを反応させると求める -不飽和ラクトンSをDIBAH還元,ついでメチル化することによりアセタール6に導いた。これにBF1・Et2Oの存在下、AllylTMSを反応させると求める -アリル体7が単一に生成した。7の立体化学は、アルデヒド8の -アリル体7が単一に生成した。7の立体化学は、アルデヒド8の 位メチレンプロトンとフェネチル基の付け根のプロトン間にNOEが観測されたことによって決定された。 位メチレンプロトンとフェネチル基の付け根のプロトン間にNOEが観測されたことによって決定された。 ついで7位水酸基の導入を検討した。8にエーテル中、AllylMgBrを反応させると、9と10が1:1で生成した。そこでエーテル中、ZnCl2存在下にAllylMgBrを作用させると、求める -アルコール9を優先(9:10=10:3)して得ることができた。一方、アルコール9と10の混合物を一旦ケトン11に酸化し、ついで還元を検討したところ、Za(BH4)2、L-Selectrideいずれの場合も -アルコール9を優先(9:10=10:3)して得ることができた。一方、アルコール9と10の混合物を一旦ケトン11に酸化し、ついで還元を検討したところ、Za(BH4)2、L-Selectrideいずれの場合も -アルコール10が極めて高い立体選択性で生成した。 -アルコール10が極めて高い立体選択性で生成した。   ここで生成した9と10の立体構造は、それぞれ対応するラクトン12と13に導き、そのCDスペクトルが12では負、13では正のコットン効果を示すことによって決定した。 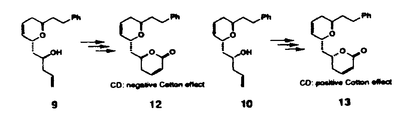 C11-C23部に相当するアルデヒドBの合成 L-Malic acidより数工程で得られるアルデヒド14(2当量)を、トリエチルアミン存在下に1当量のニトロメタンと18時間反応させたところ、目的のアルドール付加体15は15%で得られたにすぎなかった。そこで本反応を超高圧下に行った。即ち、トリエチルアミンの存在下、2当量の14と1当量のニトロメタンを11kbarで反応させたところダブルニトロアルドール反応が進行し、アルドール付加体15を90%という高収率で得ることに成功した。これは複雑な化合物の合成研究における履高圧反応の有用性を示唆するものである。  ニトロアルドール付加体15をケトン16に導いたのち、メタノール中K2CO3で扱うことにより熱力学的に安定なケトン17に異性化した。更にC16位にメチル基等価体を導入するためにエキソメチレン18に導き、ついでハイドロボレーション反応に付したところ目的のアルコール19は24%でしか得られず、ほかにジオール20が48%生成した。  ここで20の生成は、C16位にメチル基等価体を導入しつつ左右の保護基を区別して除去できたことを意味している。そこで我々はこの反応を積極的に利用することとした。即ち、18をジ-p-メトキシベンジリデンアセタール21に変換後、BH3・Me2Sと反応させろと期待通りジオール22を収率88%で単一に得ることができた。22をオキセタン23に導き、その1H-NMRでC15,17位のプロトン間にNOEが観測されたことにより22のC15,16位の相対配置がsyaであることを確定した。  ここで本反応の反応機構を検討すべく、中間体と考えられる24のコンフォメーション解析を行った。24のかわりに25についてStillのMacroModelを用いてMM2計算を行った結果、その最安定コンフォメーションは26であった。従って、上記反応はコンフォメーション27を経て進行し、このときホウ素原子は片方のアセタールの酸素原子とのみキレーションすることができ、ついでハイドライドがそのアセタールだけを選択的に攻撃し、ジオール22が生成したと考えられる。 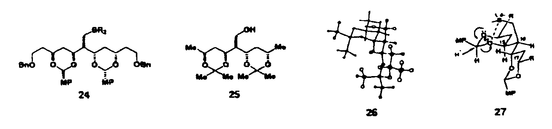 ジオール22をメチル体28としたのちラクトン29に導き、立体選択的メチル化を行い30とし、更にラクトンの還元的開環、1級水酸基の保護によってシリル体31を得た。これをアルデヒド32に導き、Evansの方法に従ってキラルイミド33とのアルドール反応に付すことにより付加体34を単一かつ高収率で合成した。34をエステル35に導いたのち、DIBAH還元とPDC酸化を行ってC11-C23部に相当するアルデヒド36(Bに相当)を得ることに成功した。  C24-C32部に相当するテトラヒドロピラン誘導体Cの合成 D-Threonineより得られるヒドロキシエステル37より、ケトエステル38を経てラクトン39を合成した。39よりケトン40(Hに相当)を得、LiAlH4還元すると求める -アルコールのみが生成し、これをメトキシ体41に変換した。41をBF3・Et2O存在下AllylTMSと反応させると、 -アルコールのみが生成し、これをメトキシ体41に変換した。41をBF3・Et2O存在下AllylTMSと反応させると、 -アリル体42が単一に生成した。これをアルデヒド43としたのちWittig反応で増炭してエステル44を得た。44より酸クロライド45を合成し、これをL-valineより得られるオキサゾリドンのリチウム塩46と反応させることによって高収率でC24-C32部に相当するテトラヒドロビラン誘導体47(Cに相当)が合成できた。 -アリル体42が単一に生成した。これをアルデヒド43としたのちWittig反応で増炭してエステル44を得た。44より酸クロライド45を合成し、これをL-valineより得られるオキサゾリドンのリチウム塩46と反応させることによって高収率でC24-C32部に相当するテトラヒドロビラン誘導体47(Cに相当)が合成できた。   C11-C32部に相当するセグメントAの合成:3の立体選択的合成 以上の様にして合成したアルデヒド36とテトラヒドロビラン誘導体47をジアステレオ選択的アルドール反応によりカップリングさせ、付加体48を単一化合物として得ることに成功した。さらに48よリジオール49を経てジアセトナイド50を合成した。50のキラルイミドを加水分解したのちエステル化、LiAlH4還元を行ってアルコール51を収率良く得た。51より3への変換を種々検討した結果、51を畑らの方法によって2-ビリジルスルフィド52としたのち、ラネーニッケルで脱硫することにより、目標化合物3の合成を達成することができた。  以上、一連のSwinholide系天然物のポリオール部に相当する3をほぼ完全な立体制御のもとに合成することに成功した。このことにより、Swinholide系天然物の「化学」に新しい展開をもたらすことが期待できる。 |