Friedel-Crafts reactionは、発見以来100年以上が経過している。これまでに類似の反応が数多く見つかり、現在ではFriedel-Crafts型反応(FriedelCrafts type reactions)と呼ばれる反応群が形成された。今回私が、反応機構に関する研究を報告するのは、Houben-Hoesch反応、Gattermann反応、及びFriedel-Craftsアシル化反応についてである(scheme1、2)。 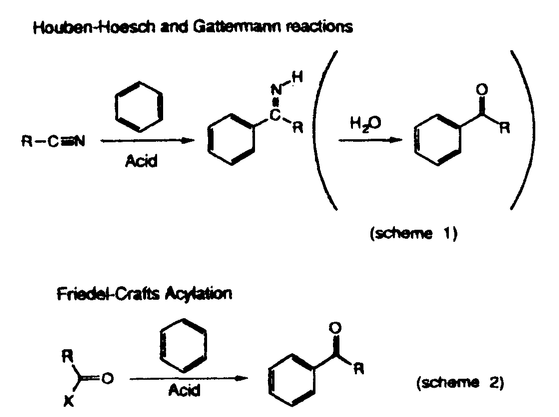 図表scheme 1 / scheme 2 図表scheme 1 / scheme 2 これらの反応に関して、芳香族化合物を求電子的に攻撃する分子種は、プロトン化ニトリル(1)やアシルカチオン(2)と考えられている。しかし(1)や(2)は、ここに示した共鳴構造をとることで、陽電荷が安定化されている。このようなカチオンが、例えばベンゼンのような、活性化されていない芳香環と反応しうるかどうか、疑問が生じる。  また、これまで首藤等により、様々なジカチオンの反応性が調べられている。これらはいずれも強酸中で生じ、ベンゼンに求電子反応するが、対応する化合物のモノカチオンは、共鳴構造で陽電荷が安定化されており、ベンゼンとは全く反応しない。 さらに、Friedel-Crafts型反応で通常用いられるルイス酸は、微量ながら水やプロトン酸を含んでいることが報告されている。ルイス駿とプロトン酸の複合体は、硫酸の1000倍以上の強酸であり、このことはFriedel-Crafts型反応のいくつかにおいて、系の酸度が非常に高いことを示している。 以上から私は、Houben-Hoesh反応、Gattermann反応、さらにFriedel-Craftsアシル化反応においても、ベンゼンなどの活性化されていない芳香族化合物と反応しうる分子種は、ジカチオンではないかという仮説に基づき、反応機構の検討を行うことにした。正確な反応系の酸度を知るため、トリフルオロ酢酸(TFA)、トリフルオロメタンスルホン酸(TFSA)及びSbF5を用いた。 最初に、Gattermann反応とHouben-Hoesh反応について述べる。この反応はこれまで、フェノールなどの、活性化されたベンゼン環では収率よく進行するが、ベンゼンでは低収率であった。超強酸を用いることで、反応は短時間に終了する(scheme 3)。さらに系の酸度を変化させると、酸度の上昇に伴い、反応の加速が観察された。 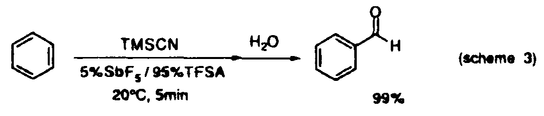 scheme 3 scheme 3 ベンゼンとの反応では、H0=12を越えてから進行し始める。TFSA中(H0=-14.0)では20℃、30分で55%の収率であった。さらに酸度を上げると反応は著しく加速され、5%SbF5/95%TFSA中では20℃、5分間で反応はほぼ終了していた。 これらの結果から、酸度の上昇にともない、分子種が生じて反応が進行することがわかる。他のニトリルのデータから、青酸のpKBH+は-10から-11と推測されるので、H0=-12では青酸の大半がプロトン化されていることになる。ここから上の酸度で反応が進行し始めることから、モノカチオンに、さらにプロトン化することが反応の進行に必要であり、ベンゼンに反応する分子種は青酸のジカチオン(3)であると考えられる。  酸度の上昇に伴う、反応速度の増加の様子をより正確に観測する目的で、4-フェニルブチロニトリルの、分子内Houben-Hoesch反応の速度を、酸度を変化させて測定することにした(scheme 4、Table 1)。表の右端のカラムに反応速度の比を示した。酸度が-10.5から-13.0まで上昇すると反応速度は200倍近く増加している。 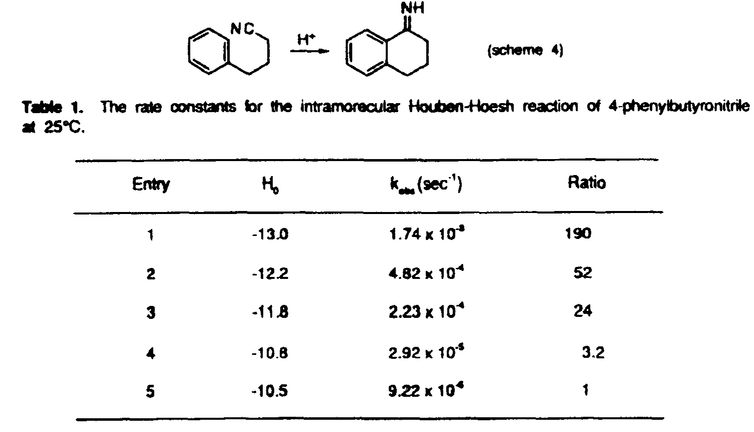 図表scheme 4 / Table 1.The rate constants for the intramorecular Houben-Hoesh reaction of 4-phenylbutyronitrile at 25℃. 図表scheme 4 / Table 1.The rate constants for the intramorecular Houben-Hoesh reaction of 4-phenylbutyronitrile at 25℃. 反応速度の対数を、酸度に対してプロットしてみる(Figure 1)。図のように、直線を引くことができた。このことから、この反応はZucker-Hammettの条件を満たしていることがわかる。すなわち、プロトン化によって分子種が生じる段階が律速段階に関わっており、しかもこの分子種の濃度は、非常に低いはずだ。4-フェニルブチロニトリルのpKBH+から考えて、プロトン化したニトリルを反応種とするには、濃度が高すぎる。真の反応種は、プロトン化ニトリルに、さらにプロトン化されることで生じるのである(scheme 5)。  図表Figure 1.The acidity-rate relationship in the intramolecular Houben-Hoesch reaction of 4-phenylbutyronitrile / scheme 5 図表Figure 1.The acidity-rate relationship in the intramolecular Houben-Hoesch reaction of 4-phenylbutyronitrile / scheme 5 さらに、Friedel-Craftsアシル化反応について同様の調査を行った。ここでは、Olahらによって単離された、アシルカチオン-フルオロアンチモンアニオンの錯体を用いた。  scheme 6 scheme 6 アセチル-アンチモン錯体(6)とベンゼンとの反応では、H0=-10.0より高い酸度で、反応の加速が観測され、H0=-14.0では、反応は短時間でほぼ定量的に進行した。これらの結果は、酸度が-10-12付近から、反応種が生成し始めることを示唆している。Friedel-Craftsアシル化反応も、高い酸度での反応は、ジカチオンによるものと考えられる(scheme 7)。  scheme 7 scheme 7 また、ベンゼンやトルエンは、ゆっくりだがアシルカチオンとも反応する。ただし、ここで注意しなければいけないのは、アシル化の場合、1分子反応が進行すると、1分子のルイス酸-プロトン酸複合体が生成するということだ。従って系の酸度は、反応の進行とともに確実に上昇していく。このような性質によって、最初はモノカチオンだけによる反応も、進行とともに系の酸度が上昇し、やがてジカチオンによる反応が起こって、加速されるはずである。つまり、実際のモノカチオンの反応性は、ここで示した結果よりさらに低いと考えられる(scheme 8)。  scheme 8 scheme 8 以上、Houben-Hoesch反応やGattermann反応、Friedel-Craftsアシル化反応において、ベンゼンを攻撃する主な分子種は、モノカチオンではなく、ジカチオンであることがわかった。ジカチオンのような、反応性の高い求電子体は、近年Olahにより"Superelectrophiles"と名付けられている。その存在が一般に認められたことで、今後この分野の研究はますます発展していくと考えられる。 |