| はじめに 造血器腫瘍においては、高頻度に、染色体転座を含む染色体異常が見いだされるが、染色体転座部位を解析することにより、転座部位に存在して、発癌と密接に関係していると思われる多くの遺伝子が単離されている。特に、リンパ性の白血病においては、その転座部位の片方の染色体上の遺伝子がリンパ球の機能を司る主要な遺伝子である免疫グロブリン遺伝子やT細胞レセプター遺伝子であることが知られており、分子レベルの解析が進んでいる。一方、骨髄性白血病においては、慢性骨髄性白血病のt(9;22)(q34;q11)に於て、BCR-ABLキメラ遺伝子の生成が知られて以来、あまり進展がなかったが、本研究と相前後して、ヒトゲノム解析の進展に伴って新しい技術や方法が開発され、分子レベルの解析が急速に進んでいる。 我々のグループはヒトゲノム解析プロジェクトの一環として、ヒト21番染色体の物理地図(NotI制限酵素地図)を完成させており(図1)、それと平行して、急性骨髄性白血病(AML)のt(8;21)(q22;q22)およびt(16;21)(p11;q22)転座部位の解析を行なってきた(図2)。疾病遺伝子のポジショナルクローニングとしては、染色体転座部位にある遺伝子のクローニングは比較的容易なこととはいえ、既知のDNAマーカーから転座切断点を正確に導きだすのはたやすいことではない。この研究で重要な役割をはたしているのは、21番染色体上の正確なランドマークとなるNotIリンキングクローン(NotI制限酵素認識配列をもつDNA断片)のほとんど完全なセットがあったことと、解析に必要な体細胞雑種が作製できたことである。本研究により、AMLの2つの染色体転座部位に存在する4つの遺伝子が単離、または同定され、発癌機構を解明する上で必要不可欠な手掛かりが得られた。  図表図1.21番染色体長腕の完全なNotI制限酵素地図。地図の横線はNotI制限酵素切断部位を示す。地図の左側にNotIリンキングクローンの名前を、右側にNotI断片の長さと既知のDNAマーカーを示す。 / 図2.t(8;21)およびt(16;21)染色体転座によって派生する染色体の模式図I.t(8;21)(q22;q22)転座の研究 図表図1.21番染色体長腕の完全なNotI制限酵素地図。地図の横線はNotI制限酵素切断部位を示す。地図の左側にNotIリンキングクローンの名前を、右側にNotI断片の長さと既知のDNAマーカーを示す。 / 図2.t(8;21)およびt(16;21)染色体転座によって派生する染色体の模式図I.t(8;21)(q22;q22)転座の研究 t(8;21)転座はAMLのFAB(French-American-British)分類M2タイプの約50%にみられ、AMLの中ではt(15;17)転座と並んで、最も高頻度に見られる染色体転座である。白血病細胞の特徴としては、顆粒球系への分化傾向を持つこと、しばしば性染色体の欠失を伴うこと、比較的寛解(自覚、他覚的な症状がなくなる状態)に導入されやすいことなどが挙げられる。まず、21番染色体の転座部位を検出するために、白血病細胞のDNAをNotI消化したのちパルスフィールドゲル電気泳動(PFGE)で分画し、NotIリンキングクローンをプローブとしてサザンブロット解析を行なったところ、LL263(LL103)クローン(図1参照)によって異常なバンドが検出された。つまりLL263によって特異的な染色体の再構成が検出された。転座部位近傍の制限酵素地図を作成したところ、転座切断点はLL263からセントロメア方向へ13kb以上、100kb以内に位置していることが判明した。その方向性は白血病細胞とマウス細胞とで作製した体細胞雑種からの情報によっている。LL263はCpGアイランドを含んでいることから、LL263そのものが転座部位にまたがる遺伝子のプロモーター領域である可能性が示唆された。 そこで、LL263からセントロメア方向へ染色体ウオーキングし、さらにcDNAライブラリーを検索して切断部位にまたがる遺伝子AML1の単離に成功した。 AML1はショウジョウバエの体節決定遺伝子runt、およびマウスポリオーマウイルスエンハンサー結合因子PEBP2 とホモロジーを有しており、特にRuntドメインにおいて非常に高い相同性がある。AML1はPEBP2 とホモロジーを有しており、特にRuntドメインにおいて非常に高い相同性がある。AML1はPEBP2 Bと相同なヒト遺伝子と考えられる。PEBP2 Bと相同なヒト遺伝子と考えられる。PEBP2 は、特異的塩基配列(PuAC CPuCA)に結合し、PEBP2 は、特異的塩基配列(PuAC CPuCA)に結合し、PEBP2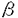 サブユニットとヘテロダイマーを形成することにより、この結合がさらに促進されること、さらにAML1のRuntドメインもPuACCPuCA配列に結合し、PEBP2 サブユニットとヘテロダイマーを形成することにより、この結合がさらに促進されること、さらにAML1のRuntドメインもPuACCPuCA配列に結合し、PEBP2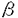 サブコニットにより結合が促進されることが報告されている。 サブコニットにより結合が促進されることが報告されている。 多数の患者サンプルの切断点を詳しく解析すると、AML1上の切断点は全て約25kbのイントロン中にあり、例外は見つからなかった(図3)。この部位はRuntドメインのC末直後であった。ただし、転座部位はイントロン中に散在しており、更にder(8)染色体、der(21)染色体(転座によって生じる派生染色体。図2参照)の切断部位近傍の塩基配列を決定したが、その塩基配列からは転座が非相同的な組換えによって起こることが推定された。次に8番染色体の転座部位については、切断点が限られた領域中にあることから、AML1は8番染色体上の切断部位にある遺伝子とキメラ遺伝子を作っていると推測された。白血病細胞からcDNAライブラリーを作製し、キメラcDNAクローンを単離して、塩基配列を決定したところ、AML1は8番染色体上の遺伝子MTG8とつながってキメラタンパクをコードしていることがわかった。MTG8もZnフィンガードメインを有し、プロリンの多い領域があるなど、転写因子としての性格を示している。AML1-MTG8キメラタンパクの構造はAML1のRuntドメインをそっくり保持し、MTG8のほぼ全域がつながった形となっている(図4)。白血病細胞においてRT-PCRでMTG8-AML1キメラmRNAは検出できないので、der(8)染色体上のAML1-MTG8キメラ遺伝子が癌化に重要な役割を果たしていることが推定された。  図3.AML1の構造とt(8;21)白血病患者における転座切断点。 図3.AML1の構造とt(8;21)白血病患者における転座切断点。 図4.AML1、MTG8およびAML1-MTG8キメラ遺伝子産物の構造。Proはプロリンに富む領域、ZnはZnフィンガー領域を示す。II.t(16;21)(p11;q22)転座部位の解析 図4.AML1、MTG8およびAML1-MTG8キメラ遺伝子産物の構造。Proはプロリンに富む領域、ZnはZnフィンガー領域を示す。II.t(16;21)(p11;q22)転座部位の解析 t(16;21)染色体転座も骨髄性白血病に特異的な転座であるが、この白血病はt(8;21)白血病などと異なり、細胞形態学的に様々な性状を呈し、FAB分類も定まっていない。染色体レベルの解析では21番染色体上の切断部位はt(8;21)転座部位と区別できないが、AML1中には切断部位がないことをPFGEで確かめた。頻度が低く、解析に十分なサンプルを得ることが困難なことなどから、der(16)染色体(図2参照)のみを持つ齧歯類ヒト体細胞雑種を作製した。21番染色体のq22領域に存在するNotIリンキングクローンをプローブとし、雑種細胞のDNAをサザンプロット解析したところ、切断点はLL390とLL42SPの間にあることが示唆された(図1参照)。LL390とLL42SPの間にはetsがん遺伝子ファミリーの一つであるERG遺伝子が存在し、その関与が示唆されたので、雑種細胞DNAを用いてPCR解析を行なったところ、der(16)染色体にはERGの5’部分は存在するがERGの3’部分は検出できず、切断点はERG遺伝子中にあると考えられた。ERG遺伝子を含むゲノミッククローンを単離し、4例の患者のDNAサンプルを用いてサザンブロット解析したところ、切断点は全てERGのETS DNA結合ドメインの直前のイントロン中にあることがわかった(図5)。したがって ERGと16番染色体上の遺伝子との間でキメラ遺伝子を形成している可能性が強く示唆された。ノーザンブロット解析を行なったところ、ERGの5’側のプローブを用いた場合も、ERGの3’側のプローブを用いた場合もキメラmRNAが検出されるが、様々な事実から白血病の責任遺伝子はder(21)染色体(図2参照)上のキメラ遺伝子である可能性が強い。16番染色体上の切断点にまたがる遺伝子はRNA結合活性を有するFUS/TLS遺伝子でることが判明し、白血病細胞ではFUS/TLS-ERGキメラ遺伝子が形成されていることを確かめた。塩基配列から推定されるFUS/TLS-ERGキメラタンパクはFUS/TLSのRNA結合部位がERGのETS DNA結合ドメインに置換した形であった(図6)。FUS/TLSは粘液様脂肪腫における染色体転座に関係する遺伝子であり、Ewing肉腫に関係するEWS遺伝子と類似している。更に、Ewing肉腫ではERGと類似のETSドメインを持つFLI1がEWS-FLI1キメラ遺伝子を、ERGがEWS-ERGキメラ遺伝子を形成していることが知られており、これら固形腫瘍と白血病の形成に機能的な関係があることが推定された。  図5.ERG遺伝子の構造とt(16;21)白血病患者における転座切断点。 図5.ERG遺伝子の構造とt(16;21)白血病患者における転座切断点。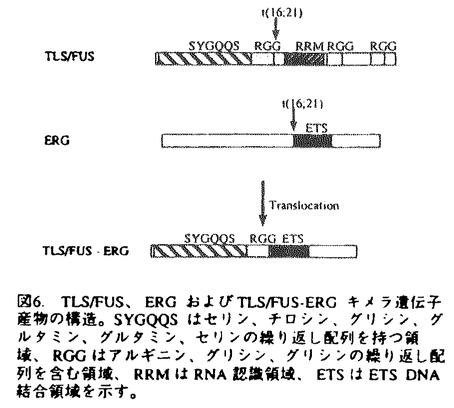 図6.TLS/FUS、ERGおよびTLS/FUS-ERGキメラ遺伝子産物の構造。SYGQQSはセリン、チロシン、グリシン、グルタミン、グルタミン、セリンの繰り返し配列を持つ領域、RGGはアルギニン,グリシン、グリシンの繰り返し配列を含む領域、RRMはRNA認識領域、ETSはETS DNA結合領域を示す。結論 図6.TLS/FUS、ERGおよびTLS/FUS-ERGキメラ遺伝子産物の構造。SYGQQSはセリン、チロシン、グリシン、グルタミン、グルタミン、セリンの繰り返し配列を持つ領域、RGGはアルギニン,グリシン、グリシンの繰り返し配列を含む領域、RRMはRNA認識領域、ETSはETS DNA結合領域を示す。結論 以上のように、21番染色体の物理地図(NotI制限酵素地図)と体細胞雑種を利用した本研究によって白血病における2つの染色体転座部位に存在する4つの遺伝子AML1、MTG8、FUS/TLS、ERGを同定でき、t(8;21)転座の場合にはAML1-MTG8キメラ遺伝子がt(16;21)転座の場合にはFUS/TLS-ERGキメラ遺伝子が生成することが明かとなった。AML1、MTG8共に転写因子と考えられるが、AML1が血球系の細胞の分化に伴って発現するのに対して、MTG8は血球系ではほとんど発現していない。従って、AML1MTG8キメラ遺伝子のコードする異常な転写因子が発現して、分化、増殖に関するAML1本来の機能を妨げるように働く可能性が考えられる。ERGもやはり転写因子として知られているが、FUSと融合することで強く発現し、それが異常な細胞増殖をもたらすようになると推定される。また、etsがん遺伝子ファミリーは本来、トリ白血病ウイルスの癌遺伝子と類似する遺伝子として同定されたもので、従来から多くの研究者がヒト白血病への関与を示唆していたが、本研究により白血病との直接の関係が初めて明確に証明された。 |