生体内で機能を発現するタンパク質は、基本構造が生合成された後、数段階の修飾を経てようやく機能型に変換される場合が多い。食品タンパク質の場合、化学的・物理的修飾等で加工物性等の付与が検討されているが、機能発現が偶発的で、修飾反応の制御が難しい。 本論文は、温和な条件で選択的反応のしやすい酵素を利用した修飾で、食品タンパク質への機能性の付与を検討した成果をまとめたもので、2部から成っている。 第1部では、食品タンパク質を基質にしてプロテアーゼ逆反応を行い、親水性タンパク質に疎水性グループを共有付加させて、強力な界面活性を誘導する研究を行った。タンパク質としては構造既知である s1-カゼインを用い、乳化機能発現とその原因となる機能性構造の解明を試みた。 s1-カゼインを用い、乳化機能発現とその原因となる機能性構造の解明を試みた。 s1-カゼインはサクシニル化によって親水性を増してから使用した。共有結合させる疎水性グループとしてL-ロイシンn-ドデシルエステルを用い、特殊条件下でパパイン修飾することによって20,000ダルトンのマクロペプチドを得ることができた。このものを効率よく得るには、アミノ酸エステルが求核試薬として働き、ペプチジル酵素をアミノ分解する方向に反応を推し進め、加水分解反応を抑える必要があり、高基質濃度、高アミノ酸エステル濃度、pH9、37℃、という異常条件を必要とした。このマクロペプチドは、炭化水素との親和性が高く、コーン油を効率よく乳化することができた。乳化機能発現は水、油の分子の運動性の束縛であることがバルスNMR、ESRの測定から明らかになった。この機能性マクロペプチドを、水-炭化水素の界面で精製したところ、電気泳動的に単一な20,000ダルトンマクロペプチドを得ることができた。反応時にN末端Tyr残基が出現し、C末端付近の構造はTyr-Phe-Leuの順であったことから、反応初期にはPhe146-Tyr146のペプチド結合が解裂し、そのC末端側にL-ロイシンn-ドデシルエステルが共有付加したものと結論した。その場合、Arg1からPhe145までは親水性のアミノ酸が多く、そこに局部的に疎水性の強いドデシル直鎖が付加したために、より明確な両親媒性構造ができあがったと考えられる。 s1-カゼインはサクシニル化によって親水性を増してから使用した。共有結合させる疎水性グループとしてL-ロイシンn-ドデシルエステルを用い、特殊条件下でパパイン修飾することによって20,000ダルトンのマクロペプチドを得ることができた。このものを効率よく得るには、アミノ酸エステルが求核試薬として働き、ペプチジル酵素をアミノ分解する方向に反応を推し進め、加水分解反応を抑える必要があり、高基質濃度、高アミノ酸エステル濃度、pH9、37℃、という異常条件を必要とした。このマクロペプチドは、炭化水素との親和性が高く、コーン油を効率よく乳化することができた。乳化機能発現は水、油の分子の運動性の束縛であることがバルスNMR、ESRの測定から明らかになった。この機能性マクロペプチドを、水-炭化水素の界面で精製したところ、電気泳動的に単一な20,000ダルトンマクロペプチドを得ることができた。反応時にN末端Tyr残基が出現し、C末端付近の構造はTyr-Phe-Leuの順であったことから、反応初期にはPhe146-Tyr146のペプチド結合が解裂し、そのC末端側にL-ロイシンn-ドデシルエステルが共有付加したものと結論した。その場合、Arg1からPhe145までは親水性のアミノ酸が多く、そこに局部的に疎水性の強いドデシル直鎖が付加したために、より明確な両親媒性構造ができあがったと考えられる。 第2部では、トランスグルタミナーゼ(TGase)はペプチド鎖中のグルタミン残基の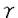 -カルボキシアミド基と各種一級アミンのアシル転移反応を触媒する酵素であり、一級アミンの導入、脱アミド、架橋高分子化の3つの反応機作を持ち、架橋はタンパク質分子内・分子間に -カルボキシアミド基と各種一級アミンのアシル転移反応を触媒する酵素であり、一級アミンの導入、脱アミド、架橋高分子化の3つの反応機作を持ち、架橋はタンパク質分子内・分子間に -( -(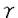 -Glu)Lys(G-Lと略す)の結合の形成を述べている。TGaseは、自然界に広範に存在することが知られているが、産業的に生産することは困難であった。量産化の容易な微生物界からTGaseを産生する菌株をスクリーニングしたところ、Streptoverticillium mobaraenseのvariantと同定された株に、強いTGase産生能があることがわかり、食品用酵素としての利用が可能となった。この微生物起源のTGaseを用い、大豆タンパク質に対し至適条件で反応を行うと各種ゲルの破断強度・変形率が増加した。タンパク質分子間にG-L結合ができ、架橋重合化することによってこのような物性の改質が可能であり、ゲル形成能増強、豆腐の物性改良などが可能となる。 -Glu)Lys(G-Lと略す)の結合の形成を述べている。TGaseは、自然界に広範に存在することが知られているが、産業的に生産することは困難であった。量産化の容易な微生物界からTGaseを産生する菌株をスクリーニングしたところ、Streptoverticillium mobaraenseのvariantと同定された株に、強いTGase産生能があることがわかり、食品用酵素としての利用が可能となった。この微生物起源のTGaseを用い、大豆タンパク質に対し至適条件で反応を行うと各種ゲルの破断強度・変形率が増加した。タンパク質分子間にG-L結合ができ、架橋重合化することによってこのような物性の改質が可能であり、ゲル形成能増強、豆腐の物性改良などが可能となる。 具体的には、スケトウダラ冷凍すり身に対するTGaseの効果を検討した。至適条件で反応を行ったところ、破断強度、変形率とも増加した。食感的には、弾力とコシの強化されたものとなった。これは、G-L結合の増加が原因であると考えられる。次に、市販冷凍すり身8種におけるTGase反応の効果を検討した。各魚種すり身の内在性TGase活性の強さ、鮮度をCa2+-ATPase活性によって測定し、TGaseの添加効果と各種要因の関係を検討した。各魚種すり身に対して、TGaseは、破断強度、変形率を増加させる機能を持っていた。 以上本論文では、通常はタンパク質を分解する「ハサミ」の機能を有するプロテアーゼを用い、その逆反応を行うことにより親水性タンパク質に疎水性グループを共有結合状に導入した。その結果、両親媒性構造が形成し、強力な乳化機能が付与できた。またタンパク質同士を架橋重合化し、「ノリ」の機能を有するTGaseを各種食品タンパク質に応用することによりゲル形成能や弾力の付与が可能であり、ゲル状食品の高付加価値化、資源の有効活用が可能になった。また食品タンパク質のゲル化のメカニズム解明にも寄与するものであり、学術上、応用上貢献するところが少なくない。よって、審査員一同は、申請者に博士(農学)の学位を授与してしかるべきものと判断した。 |