| 内容要旨 | | 薬物代謝研究は薬物の有効性,安全性の解釈,薬理活性代謝物の有無等の検討において有益な情報を与える.我々はジルチアゼム(Dil)とその関連化合物TA-993(TA)の代謝に関して研究した.Dil(図1)は冠血管拡張作用等を有するbenzothiazepine誘導体のCaチャンネル拮抗薬であり,狭心症,不整脈,高血圧症等の治療に広く使われている.Dilの代謝では,これまでに7種の塩基性代謝物が明らかにされていた.本研究では,ヒトにおける主要代謝物を含む未知塩基性代謝物および全く未検討であった酸性代謝物について,マススペクトル(MS)により構造を解析し,代謝経路および種差の検討を行った.次いで,新規酸性代謝物の生成機構についてラット肝細胞分画を用いて検討した.一方,Dilは血小板凝集抑制作用も有する.更に強力な同作用を有するDil関連化合物を探索した結果,TA(図1)が見出され,抗血小板凝集薬として現在開発中である.本研究ではDilの場合と同様にMSを主体にした代謝物の構造解析およびHPLCにより,代謝におけるDilとの相違を明らかにした.また,ラセミ体投与時の各対掌体の代謝について,TAの擬似ラセミ体を用いて検討した.  図1.ジルチアゼム(Dil)およびTA-993(TA)の化学構造 図1.ジルチアゼム(Dil)およびTA-993(TA)の化学構造 Dilの代謝:先ず,Dilとその既知塩基性代謝物およびDilと8-Cl-Dilの安定同位体のpositive ion electron ionization(PIEI)MSにおけるフラグメントイオンの生成経路および構造を解析し,5位側鎖の構造を表すa群イオン,benzothiazepine環の2,3位置換基を含むb群イオン,benzothiazepine環のベンゼン部分を含むc群イオン等がMSによるDilアナログの構造解析に特に重要であることを見出した(図2).これらのイオンのm/z値の変化に注目し,ラット,イヌ,ヒトにおけるDil代謝物の構造を解析した.  図2.PIEI MSにおけるDilアナログの開裂様式とフラグメントイオンの構造 図2.PIEI MSにおけるDilアナログの開裂様式とフラグメントイオンの構造 新規の脂溶性塩基性代謝物としてMA(ヒトにおけるDilの主要代謝物),MB,MC,MDおよびM9,脂溶性酸性代謝物として,Dilの5位側鎖がCH2COOHに変換したA1-A6を推定し(表1),その内MA,MD,A1-A4を同定した.酸性代謝物はラットではA4,イヌおよびヒトではA2が各々多く,塩基性代謝物に関しても種差が見られた.冠血管拡張作用の強さはDil>MA>>MDの順であり,酸性代謝物A1-A4では同作用がなかった.  表1.新規Dil代謝物の構造(R1-R4:図2参照) 表1.新規Dil代謝物の構造(R1-R4:図2参照) Dilの酸性代謝物の生成経路として考えられた5位側鎖の脱アミノ化に,脱アミノ化酵素として知られているP450およびモノアミンオキシダーゼ(MAO)どちらが関与しているかを調べるために,Dilを基質としてラット肝細胞分画(ホモジネート,ミトコンドリア,S3,ミクロソーム)による反応を行った.いずれの画分でもP450の補酵素であるNADPHを添加した場合のみ,酸性代謝物,その前駆体の中性代謝物(アルデヒド体)が生成し,また,ミトコンドリア画分よりミクロソーム画分で多く生成した.更に,酸性,中性代謝物ともミクロソーム画分でのP450阻害剤(SKF 525-A)による阻害が大きく,MAO阻害剤(pargyline,iproniazid)による阻害が小さかったことから,中性代謝物,アルデヒド体の生成に関与する酵素は主としてミクロソームのP450であり,MAOの関与は殆ど無いと結論された. TAの代謝:TAおよび3種の予想代謝物[MB1(deacetyl-TA),MB2(N-monodemethyl-TA),MB3(deacetyl-N-monodemethyl-TA)]の合成標品(2R,3R)では,Dil(2S,3S)と2,3位の配置が異なるが,MSにおける特徴的フラグメントイオン(a群,b群,c群イオン等)の構造および生成経路はDilの場合と同様であることを見出した.そこでDilの場合と同様にこれらの主要イオンに着目したMS解析を主体にして,TAを投与したラット,イヌおよびヒトにおける代謝物の構造を解析した.脂溶性塩基性代謝物(MB)として15種,MB1-MB15の構造(TA,MB1,MB2,MB3各々の8-或いは4’-CH2OH体および8,4’-CH2OH体)を推定し,その内MB1-MB13を同定した.ラットでは4’-CH2OH体,イヌでは8-CH2OH体と8,4’-CH2OH体,ヒトではMB1-MB3と8-CH2OH体が各々多かった.脂溶性酸性代謝物(MA,15種)は,その構造に少なくとも1個のCOOHを有し,5位側鎖の構造により3群[5-(CH2)2NHAc,MAA群;5-CH2COOH,MAC群;5-(CH2)2OH,MAE群]に分けられ,6種(MAA1,MAC1,MAC7,MAE1,MAE4,MAE7)を同定した.酸性代謝物は全体に少なかったが,MAA群代謝物のみラットで特異的に,しかも多量に見出された.ラット,イヌで排泄が多い水溶性代謝物(MAq)の殆どはFAB MS/MSおよびGC/MSにより,5位側鎖に1-3級アミノ基,8位,4’位に1-2個のCOOHを有するアミノカルボン酸型化合物と推定した.22種を見出し,4種(MAq1,MAq3,MAq5,MAq7)を同定した.ラットでは5位側鎖がNHCH3の4’-COOH体と8,4’-COOH体(MAq7,MAq10等),イヌではN(CH2)2の8-COOH体と8,4’-COOH体(MAq1,MAq9等),ヒトではN(CH3)2の8-COOH体(MAq1等)が各々多かった.Dilと異なり,TAでは8位と4’位のCH3の酸化が5位置換基の代謝に優先し,5位側鎖にアミノ基が残ったアミノカルボン酸型水溶性代謝物が多くなったと考えられる.血小板凝集抑制作用は脂溶性塩基性代謝物のみに認められ,MB1,MB3,MB7,MB11等ではTAより強かった. TAはl-cis体(l-体)であるが,その対掌体d-cis体(d-体)との間の代謝の差および代謝における相互作用を検討するために,擬似ラセミ体([14C]TAと13C-d-TAの1:1混合物;p-rac-TA)を調製し,(A)[14C]TA,(B)p-rac-TA,(C)rac-[14C]TAを投与したラットおよびイヌの尿,血漿中未変化体および脂溶性塩基性画分代謝物について比較した.ラット尿の放射能検出HPLCの各クロマトグラムにおいて,(A)および(B)投与時のピークパターンが同様であることからラセミ体投与時のl-体即ちTAの代謝は対掌体(d-体)の影響を受けないこと,また,(A)或いは(B)投与時と(C)投与時ではピークパターンが異なることから対掌体間で代謝が異なることが明らかとなった.しかし,(C)投与時の放射能検出HPLCの各ピークはd-体,l-体の和である.そこで,5位側鎖の13C標識を認識できるイオンa1,a3[m/z58,154(l-体);m/z59,156(d-体)]を用いたGC-マスクロマトグラフィーを行い,p-rac-TA投与時の未変化体,塩基性代謝物についてd-体由来とl-体由来の別々のクロマトグラムを作成し,2つのクロマトグラムの間で各化合物のピークの大きさを比較して対掌体間で代謝が異なることを更に明確に解明した.また,マスクロマトグラム上の各化合物のd-体,l-体由来のピーク面積比から求めた(B)投与時のラットの尿,血漿中各代謝物のd/l比がMB4-MB7(8-CH2OH体)で1より大きい(約3以上)ことからd-体では8-CH3が,MB9-MB11(4’-CH2OH体)で小さい(約0.5以下)ことからl-体では4’-CH3が水酸化を受け易いことを解明した. 以上に述べたように,親薬物(Dil,TA),その安定同位体標識体,予想代謝物等のアナログのマススペクトル(MS)を詳細に解析した結果を利用するMS解析を主体にしてDilおよびTAの代謝物の構造を迅速に解明できた.この手法は薬物の代謝物の迅速な構造解析に有用な方法の一つになると考える.代謝物の構造解明は,いわゆる吸収・排泄試験とともに,薬物代謝研究の土台であり,新薬開発においては勿論,全ての代謝研究に必須である.また,Dilの主要代謝物である酸性代謝物生成に関与する酵素はミクロソームP450であること,DilとTAの代謝における相違は置換基の違いと置換基の代謝の優先性の違いにあること,TAをラセミ体として投与した時,対掌体間で代謝はかなり異なるが,相互作用が無いことを明らかにした.更に進んで,Dil,TAの5位側鎖の酸化,芳香環上の置換基の酸化に関与する酵素,d-体とl-体の代謝における酵素等について,特に最近解明が進んでいるヒトにおけるP450ファミリーの同定等を行えば,臨床における有効性,安全性,薬物相互作用の予測に寄与するであろう.代謝酵素を詳細に調べることは薬物代謝研究の重要な―分野であると考える. |
| 審査要旨 | | 本論文はジルチアゼム(Dil)とその関連化合物TA-993(TA)の代謝に関する研究である.Dil(図1)は冠血管拡張作用等を有するbenzothiazepine誘導体のCaチャンネル拮抗薬であり,狭心症・不整脈・高血圧症等の治療に広く用いられている. 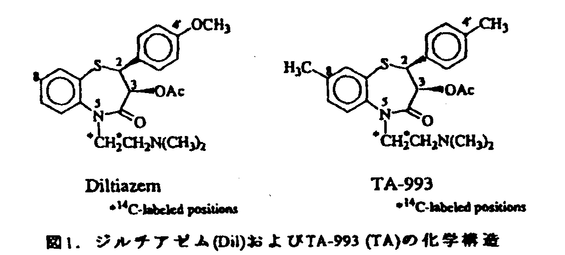 図1.ジルチアゼム(Dil)およびTA-993(TA)の化学構造 図1.ジルチアゼム(Dil)およびTA-993(TA)の化学構造 Dilに関してはこれまでに7種の塩基性代謝物が明らかにされていたが,本研究ではヒトにおける主要代謝物を含む未知塩基性代謝物および全く未検討であった酸性代謝物について,マススペクトル(positive ion electron ionization[PIEI]MS)により新規代謝物の構造を決定した.更に代謝経路および種差の検討,次いで新規代謝物の生成機構についてもラット肝細胞分画を用いて検討した. すなわち新規の脂溶性塩基性代謝物としてMA,MD,A1〜A4を同定し(図2,表1),特にMAはヒトにおける主要代謝物であることを明らかにした.酸性代謝物ではラットではA4,イヌおよびヒトではA2がそれぞれ多く,種差が見られた.  図表表1.新規Dil代謝物の構造(R1-R4:図2参照) 図2.PIEI MSにおけるDilアナログの開裂様式とフラグメントイオンの構造 図表表1.新規Dil代謝物の構造(R1-R4:図2参照) 図2.PIEI MSにおけるDilアナログの開裂様式とフラグメントイオンの構造 冠血管拡張作用の強さはDil>MA>>MDの順であり,酸性代謝物A1〜A4では同作用はなかった.また代謝経路の検討により,Dilの酸性代謝物およびその前駆体である中性代謝物(アルデヒド体)の生成にモノアミンオキシダーゼ(MAO)はほとんど関与してなく,ミクロソームのP-450による5位側鎖の脱アミノ化反応が主たる代謝経路であることを明らかにした. 一方,Dilは血小板凝集抑制作用も有するが,さらに強力な同作用を有するDil関連化合物を探索した結果,TA(図1)を見出した.これは現在抗血小板凝集薬として開発中である.このTAに関しても代謝におけるDilとの相違を明らかにした.更にラセミ体投与時の各対称体の代謝についても検討を加えた. 具体的には脂溶性塩基性代謝物として15種,脂溶性酸性代謝物として6種,水溶性代謝物としては4種の化合物の構造を決定した.ラット,イヌ,ヒト間で大きな種差があることを明らかにした.血小板凝集抑制作用は脂溶性塩基性代謝物のみに認められた.更にTAはl-cis体(l-体)であるが,その対称体d-cis体(d-体)との代謝の差および代謝における相互作用についても検討し有用な知見を得た. 本研究は,以上述べたようにDilおよびTAの代謝物の構造決定を安定同位体標識体を用いてMS解析を主体にして行ったものであるが,このような代謝物の迅速な構造決定法は薬物代謝物の同定法として一般に適用できる有用な方法の一つである.また代謝経路の解析,光学異性体の対称体間での代謝の違いなどの知見は薬物代謝学に寄与するところ大であり,これらの点から博士(薬学)の学位に値するものと認める. |